Просмотр содержимого документа
«Сравнительная характеристика галогенов»

Зайчиков Владимир Васильевич
учитель химии МКОУ «Бодеевская СОШ»
Воронежская область
Лискинский район

Цель: расширить представление об элементах-аналогах Периодической системы на примере подгруппы галогенов
Задачи:
- Познакомить учащихся с историей открытия галогенов
- Сравнить строение атомов галогенов, выявив черты сходства и отличия
- Сравнить физические свойства и химическую активность галогенов
- Дать представление о роли галогенов в организме

Строение галогенов

Открытие фтора
- Фтор( F 2 ) –от греч. «фторос»-
разрушающий
- был открыт в 1866 году
- французским химиком Анри Муассаном
- электролизом смеси жидкого безводного HF и гидродифторида калия KHF 2 в платиновом сосуде:
2HF→H 2 ↑ + F 2 ↑
катод анод
В 1906 году Муассан был удостоен Нобелевской премии за открытие элемента фтора и введение в практику электрической печи, названной его именем

Открытие хлора
- Хлор Cl 2 от греч. «хлорос» -
желто-зеленый
- 1774 год
- Шведский аптекарь Карл Вильгельм Шееле
- «Я поместил смесь черной магнезии с муриевой кислотой в реторту, к горлышку которой присоединил пузырь, лишенный воздуха, и поставил ее на песчаную баню. Пузырь наполнился газом, который имел желто-зеленый цвет и пронзительный запах».
- Уравнение реакции:
MnO 2 + 4HCl Cl 2 + MnCl 2 + 2H 2 O

Открытие брома
- Бром (Br 2 ) от греч. «бромос»-
зловонный
- Был открыт в 1826 году
- Французским химиком (24-летним лаборантом) Антуаном- Жеромом Баларом
- Действием хлором на рассолы соляных болот Франции по реакции:
2NaBr + Cl 2 → 2NaCl + Br 2

Открытие йода
- Йод ( I 2 ) от греч. «иодес» -
фиолетовый
- Был открыт в 1811 году
- Французским химиком-технологом и фармацевтом Бернаром Куртуа в золе морских водорослей
- Уравнение реакции:
2 NaI + H 2 SO 4 → Na 2 SO 4 + I 2

Физические свойства

Физические свойства простых веществ-галогенов
Хлор
Бром
Астат
Йод

Возгонка йода
- Кристаллический йод обладает способностью при нагревании переходить из твердого состояния в газообразное , минуя жидкое ( возгонка ),превращаясь в фиолетовые пары.
- Опыт: возгонка йода
Пары йода

Сравнение физических свойств простых веществ-галогенов
- F 2 светло-желтый газ
- Cl 2 желто-зеленый газ
- Br 2 красно-бурая жидкость
- I 2 темно-серые кристаллы с металлическим блеском
- At 2 черно-синие кристаллы
- Интенсивность цвета усиливается
- Плотность увеличивается
- Температуры плавления и кипения увеличиваются

Химические свойства
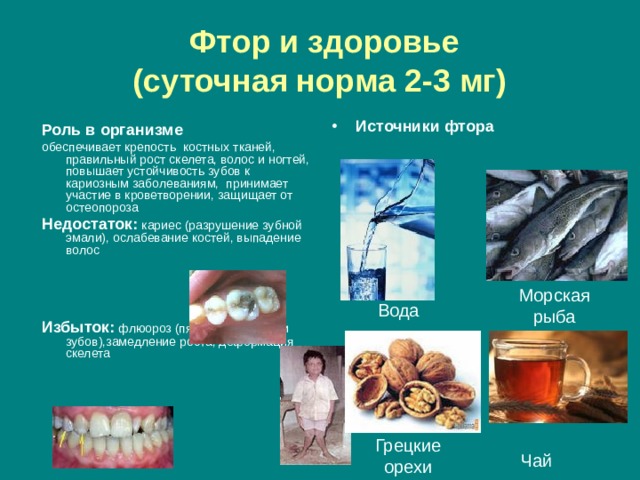
Фтор и здоровье ( суточная норма 2-3 мг)
Роль в организме
обеспечивает крепость костных тканей, правильный рост скелета, волос и ногтей, повышает устойчивость зубов к кариозным заболеваниям, принимает участие в кроветворении, защищает от остеопороза
Недостаток: кариес (разрушение зубной эмали), ослабевание костей, выпадение волос
Избыток: флюороз (пятнистость эмали зубов),замедление роста, деформация скелета
Морская рыба
Вода
Грецкие орехи
Чай

Хлор и здоровье (суточная норма 2г)
- Роль в организме:
- Образование соляной кислоты, поддержание водно-электролитного баланса, выведение шлаков и углекислого газа из организма, расщепление жиров
- Недостаток:
- мышечная слабость, сонливость, вялость, ослабление памяти, потеря аппетита, сухость во рту, выпадение зубов и волос
- Избыток:
- задержка воды в тканях, повышение кровяного давления, боли в голове и груди, диспепсические расстройства, сухой кашель, слезотечение, резь в глазах
Бобовые
Свекла
Поваренная соль
Злаки

Бром и здоровье (суточная норма 0,5-2 мг)
- Роль в организме:
- принимает участие в регуляции деятельности нервной системы, оказывает влияние на функции половых желез, влияет на процессы возбуждения и торможения в головном мозге
- Недостаток:
- бессонница, снижение уровня роста эритроцитов в крови.
- Избыток:
- кожное заболевание – бромодерма, нарушение работы нервной системы, апатия, сонливость, ослабление
- памяти

Йод и здоровье (суточная норма100-200 мкг)
- Роль в организме:
- Участие в синтезе гормонов щитовидной железы, создание патрульных клеток в крови- фагоцитов.
- Избыток:
- гипертиреоз- увеличение обмена веществ учащение пульса, возбудимость
- Недостаток:
- гипотиреоз-снижение функции щитовидной железы( снижение обмена веществ, понижение температуры тела, слабость), базедова болезнь,
умственная
отсталость
Кальмары
Хурма
Томаты
Морская рыба
Морская капуста
Морковь

Тест по теме: «Галогены».


































