Просмотр содержимого документа
«Степень окисления»

Составила учитель химии и
биологии МБОУ Екатерининская
СОШ Братчикова Т.С.

Степень окисления – это условный заряд атомов
химических элементов, вычисленный на основе
предположения, что все соединения состоят из
ионов.

Степень окисления может иметь
положительное, отрицательное и нулевое значение.

Степень окисления ставится над
символом элемента, причем сначала
пишется заряд (+ или -), а затем
пишется число (1, 2, 3).
-
3
+
-
1
1
2
+
S
H
N
Na
3
2

Правила для расчета степени окисления:
1.У атома кислорода с.о. почти всегда равна -2, лишь в соединениях с более электроотрицательнным фтором у атома кислорода с.о. +2 .
2.У атома водорода с.о. почти всегда равна +1. Лишь в соединениях с металлами с.о. атома водорода равна -1.
3.У металлов главных подгрупп с.о. всегда положительная и ее максимальное значение равно номеру группы в ПСХЭ.
4.У свободных атомов и у простых веществ с.о. равна нулю.
5.Суммарная с.о. всех атомов в соединении равна нулю.
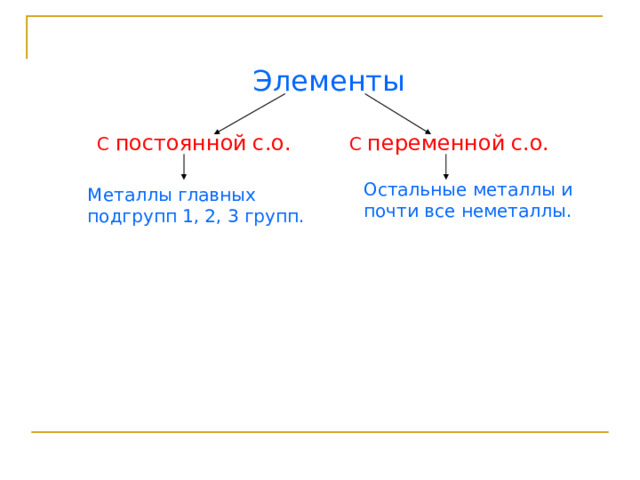
Элементы
С постоянной с.о.
С переменной с.о.
Остальные металлы и
почти все неметаллы.
Металлы главных
подгрупп 1, 2, 3 групп.

Правила составления формул
соединений:
1.Записываем знаки элементов рядом, причем на
первом месте пишется символ менее
электроотрицательного элемента.
2.Определяются с.о. каждого элемента
(с помощью ПСХЭ).
3.Значения с.о. записываются над символами
элементов.
4.Находим наименьшее общее кратное.
5.Рассчитываем индексы делением наименьшего
общего кратного на с.о.
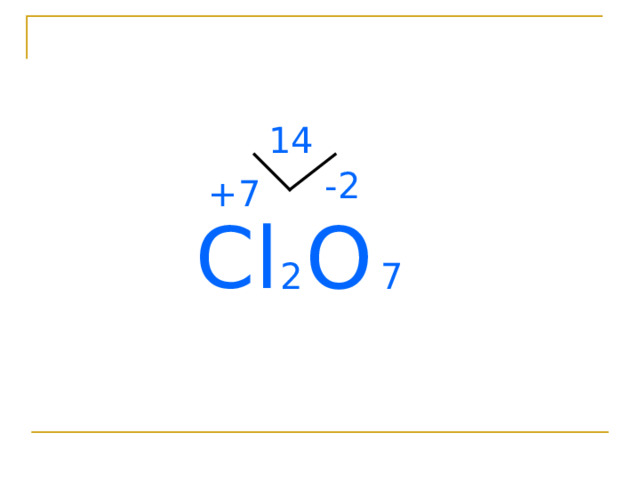
14
-2
+7
Cl
O
2
7

Номенклатура бинарных
соединений
1.На первом месте пишется латинское
название электроотрицательного элемента
с суффиксом – ид в именительном падеже.
2.На втором месте пишется название
металла или менее электроотрицательного
элемента в родительном падеже.

NaCl – хлор ид натрия
Al 2 S 3 – сульф ид алюминия
СаН 2 - гидр ид кальция

Если элемент проявляет перемен
ную с.о., то ее значение указывается
римской цифрой в скобках
+4 -1
PbCl 4 – хлорид свинца ( IV)
+7 -2
Cl 2 O 7 – оксид хлора ( VII)



























