
Муниципальное общеобразовательное учреждение «Болычевская основная общеобразовательная школа».
- «Строение электронных оболочек атомов.»
- Автор: Щенникова С.В-
- учител химии и биологии.

Цели урока: обобщение знаний о строении атома, изучение строения электронной оболочки атома
1. Обучающая:
Научить школьников записывать электронные конфигурации атомов элементов I-IV периодов.
2. Развивающие:
сформировать у учащихся личностную мотивацию, познавательный интерес к данной теме; развить интеллектуальные и творческие способности учащихся, диалектическое мышление; углубить знания о взаимосвязи строения атома и структурой ПСХЭ; отработать навыки работы с опорным конспектом и ПСХЭ.
3. Воспитательная:
развить познавательный интерес к устройству окружающего мира.

Цели урока
Обобщить и закрепить знания обучающихся об электронном строении атома, усовершенствовать умения рассчитывать число элементарных частиц .
ЗАДАЧИ УРОКА: ОБРАЗОВАТЕЛЬНЫЕ ЗАДАЧИ : АКТУАЛИЗИРОВАТЬ ЗНАНИЯ УЧАЩИХСЯ О СТРОЕНИИ АТОМА, ПОВТОРИТЬ СТРОЕНИЕ АТОМНОГО ЯДРА И ХАРАКТЕРИСТИКУ ЭЛЕМЕНТАРНЫХ ЧАСТИЦ,. РАЗВИВАЮЩИЕ ЗАДАЧИ : РАЗВИТИЕ У ОБУЧАЮЩИХСЯ УМЕНИЙ АНАЛИЗИРОВАТЬ И СРАВНИВАТЬ СТРОЕНИЕ АТОМОВ РАЗЛИЧНЫХ ЭЛЕМЕНТОВ, РАБОТАТЬ С ОБОРУДОВАНИЕМ В СООТВЕТСТВИИ С ТЕХНИКОЙ БЕЗОПАСНОСТИ. ВОСПИТАТЕЛЬНЫЕ ЗАДАЧИ : ФОРМИРОВАНИЕ ОСНОВНЫХ МИРОВОЗЗРЕНЧЕСКИХ ИДЕЙ: МАТЕРИАЛЬНОСТЬ МИРА, ПРИЧИННО-СЛЕДСТВЕННЫЕ СВЯЗИ ЯВЛЕНИЙ, ПОЗНАВАЕМОСТЬ МИРА. ЗНАНИЯ, УМЕНИЯ, НАВЫКИ И КАЧЕСТВА, КОТОРЫЕ АКТУАЛИЗИРУЮТ (ПРИОБРЕТУТ, ЗАКРЕПЯТ) УЧЕНИКИ В ХОДЕ УРОКА

Выберите правильный ответ
1 . Предложил название «электрон» 1) Стони 2) Томпсон 3) Беккерель 4) Резерфорд
2. Предложил планетарную модель атома 1) Стони 2) Томпсон 3)Беккерель 4) Резёрфорд
3. Число электронов в атоме натрия равно 1)23 2)12 3)34 4)11
4. Число нейтронов в атоме 39 К равно 1)39 2)58 3)26 4)20
5. Атомы какого химического элемента имеют в своем составе
5 протонов, 6 нейтронов, 5 электронов
а) углерода, б) натрия, в) бора, г) неона.
6.Число протонов в атоме кислорода равно:
1)8 2) 9 3)10 4)11
7. Атомы какого химического элемента имеют в своем составе
7 протонов, 7 нейтронов, 7 электронов а) углерода, б) натрия, в)азот, г) фтор.
8.Число нейтронов, протонов электронов в атоме 39 Ar равно
1)22 18 18 2)21 18 18 3)26 18 17 4)20 19 18

Правильные ответы
- Предложил название «электрон» 1) Стони 2) Томпсон 3) Беккерель 4) Резерфорд
2. Предложил планетарную модель атома 1) Стони 2) Томпсон 3)Беккерель 4) Резёрфорд
3. Число электронов в атоме натрия равно 1)23 2)12 3)34 4)11
4. Число нейтронов в атоме 39 К равно 1)39 2)58 3)26 4)20
5. Атомы какого химического элемента имеют в своем составе
5 протонов, 6 нейтронов, 5 электронов
а) углерода, б) натрия, в) бора , г) неона.
6.Число протонов в атоме кислорода равно:
1)8 2) 9 3)10 4)11
7. Атомы какого химического элемента имеют в своем составе
7 протонов, 7 нейтронов, 7 электронов а) углерода, б) натрия , в)азот , г) фтор.
8.Число нейтронов, протонов электронов в атоме 39 Ar равно
1)22 18 18 2)21 18 18 3)26 18 17 4)20 19 18

Атом водорода
Планетарная модель
атома
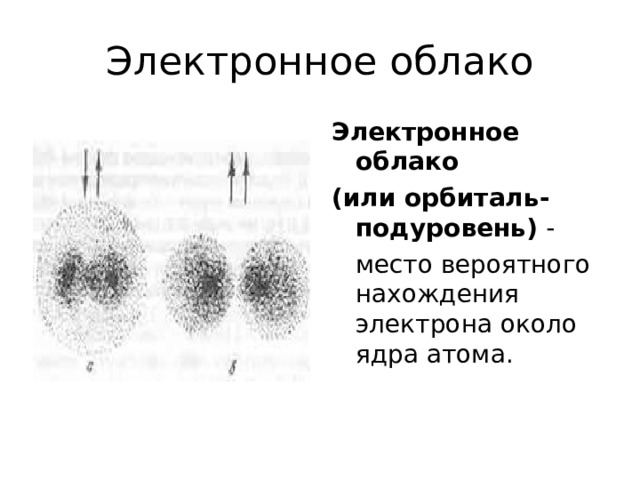
Электронное облако
Электронное облако
(или орбиталь-подуровень) -
место вероятного нахождения электрона около ядра атома.

Электронная оболочка -совокупность электронов.
Число электронов в оболочке атома
равно порядковому номеру элемента в таблице Д.И.Менделеева
Энергетический
уровень-
это совокупность
электронов с близкими значениями энергии
- Энергетический уровень- это совокупность электронов с близкими значениями энергии
Число энергетических уровней
определяется номером периода ХЭ в ПСХЭ

Строение атома
- Атом состоит из двух основных частей: __________ и ________________________ .
- В центре атома находится __________ , вокруг которого располагаются ________________ .
- Ядро состоит из _____________и _____________ .
- На электронных слоях располагаются _______________, их заряд - _________________ ,.
- Число протонов в атоме химического элемента равно____________________________________ .
- Число нейтронов можно вычислить по формуле___________________
_______________________________________________.
- Заряд ядра атома химического элемента равен _____________________
_____________________ .
- Общее число электронов в атоме химического элемента равно _______
_____________________ .
- Число заполняемых электронами энергетических уровней в атоме химического элемента равно ___________________________________ .
- Число электронов на внешнем энергетическом уровне равно ________
_____________ .


На рисунке отметьте точками, правильные ответы, соедините точки
- .
- 1. Опыление – это
- А. Перенос пыльцы с тычинок на рыльце пестика.. Б. Слияния спермия с центральной клеткой В. Прорастание пыльцевых зерен Г. Слияние половых клеток
- 2. Искусственное опыление – это перенос пыльцы с тычинок на рыльце пестика с помощью:
- А. Ветра Б. Человека В. Воды Г. Животных
- 3. Яркая окраска характерна для цветков, опыляемых:
- А. Ветром Б. Насекомыми В. Путем самоопыления Г. Искусственно
- 4. Самоопыление происходит у:
- А. Картофеля, гороха Б. Березы, орешника В. Вишни клевера Г. Ржи, кукурузы.
- Если на лице появилась улыбка, значит вы успешно справились с тестом, если улыбка немного исказилась, то у вас есть ошибки, над которыми нужно еще поработать.
- Урок окончен, спасибо.


Строение атома
- Атом состоит из двух основных частей: _____ положительно заряженного ядра и отрицательно заряженных
- электронов, образующих электронную оболочк _ .
- В центре атома находится ____ ядро ______ , вокруг которого располагаются _____ электроны ___________ .
- Ядро состоит из ___ протонов_и __нейтронов ___ .
- На электронных слоях располагаются _____ электроны, их заряд - ____минусовой_____________ ,.
- Число протонов в атоме химического элемента равно___ порядковому номеру элемента____ .
- Число нейтронов можно вычислить по формуле_______ N = A - Z ___
- Заряд ядра атома химического элемента равен _____ порядковому номеру элемента
Общее число электронов в атоме химического элемента равно _ порядковому номеру элемента
- Число заполняемых электронами энергетических уровней в атоме химического элемента равно ___ номеру периода
- Число электронов на внешнем энергетическом уровне равно ____ номеру группы

Число электронов на внешнем энергетическом уровне электронной оболочки атома равно номеру группы для химических элементов главных подгрупп.

Максимальное число электронов находящихся на Э.У определяем по формуле: N = 2 n 2 Где N - максимальное число электронов на уровне; n – номер энергетического уровня.
Энергетический уровень
Максимальное число электронов
1
2
2
3
8
4
18
32
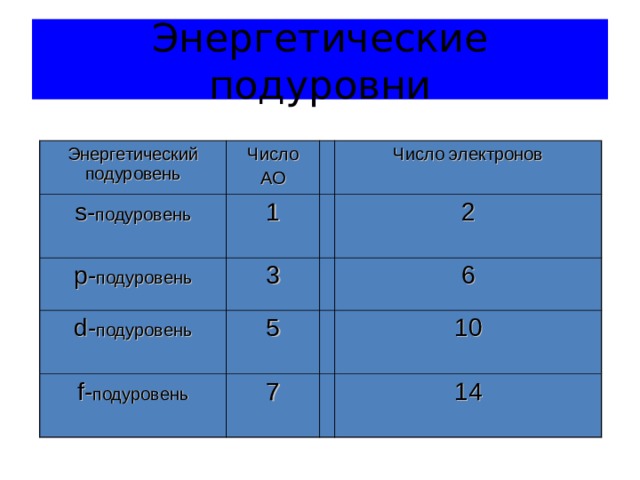
Энергетические подуровни
Энергетический подуровень
Число
АО
s - подуровень
1
p- подуровень
d- подуровень
3
Число электронов
2
5
f- подуровень
6
7
10
14

Подуровни энергии
- Согласно современной (квантовомеханической) модели атома энергетические уровни состоят из подуровней.
- Число подуровней, которые образуют конкретный уровень, равно его номеру. Подуровни обозначают буквами s, p, d, f.
Номер энергетического уровня
1
Подуровни энергии
2
s (один подуровень)
s, p (два подуровня )
3
4
s, p, d (три подуровня )
s, p, d, f (четыре подуровня
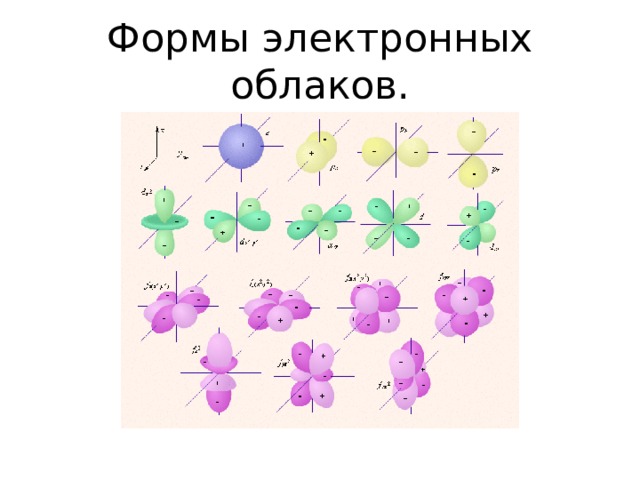
Формы электронных облаков.

Порядок заполнения АО

Электронные формулы Используя для обозначения уровня арабские цифры и обозначая орбитали буквами s и p , а число электронов данной орбитали арабской цифрой вверху справа над буквой, изображаем строение атомов более полными электронными формулами.
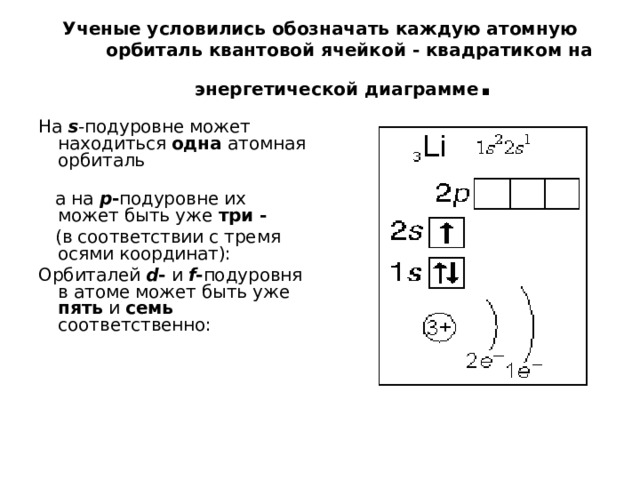
Ученые условились обозначать каждую атомную орбиталь квантовой ячейкой - квадратиком на энергетической диаграмме .
На s -подуровне может находиться одна атомная орбиталь
а на p - подуровне их может быть уже три -
(в соответствии с тремя осями координат):
Орбиталей d - и f - подуровня в атоме может быть уже пять и семь соответственно:
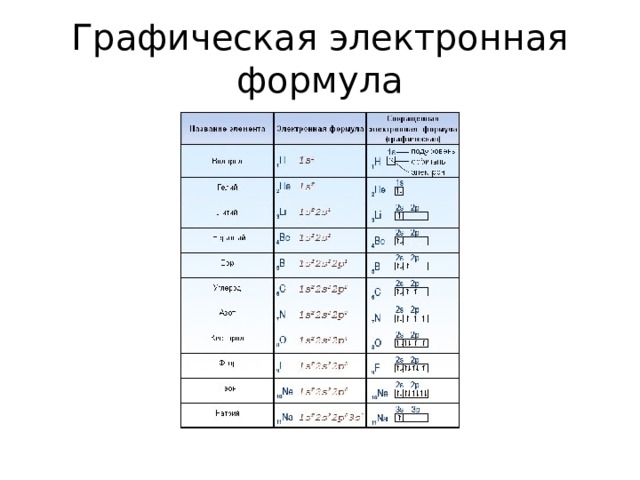
Графическая электронная формула

ТЕСТ . По данным о распределении валентных электронов найдите элемент:
- а ) 2s 1
- б ) 2s 2 2p 4
- в ) 3s 2 3p 6
- г ) 3d 10 4s 1
- д ) 4s 2 4p 3
- е ) 4s 2 4p 5
- ж ) 3s 2 3p 4










































