Просмотр содержимого документа
«Свойства этилового спирта»

МЕТАНОЛ И ЭТАНОЛ. ПОЛУЧЕНИЕ И ХИМИЧЕСКИЕ СВОЙСТВА ОДНОАТОМНЫХ СПИТРОВ.

Метанол (метиловый спирт)
Бесцветная жидкость
с температурой кипения
64,7 0 С, с характерным запахом.
Легче воды. Горит чуть
голубоватым пламенем.
Историческое название –
древесный спирт.
Метанол – прекрасный
растворитель, его используют для производства формальдегида,
некоторых лекарственных веществ.

Этанол ( этиловый спирт)
- Бесцветная жидкость с температурой кипения 68,73 0 С, с характерным запахом и жгучим вкусом.
- Легче воды. Смешивается с ней в любых соотношениях.
- Легко воспламеняется, горит слабо светящимся голубоватым пламенем.

Получение предельных одноатомных спиртов

Лабораторные
- Гидролиз галогеналканов
- Гидратация этиленовых углеводородов
Промышленные.
- Синтез метанола из синтез-газа
- Гидратация этилена
- Брожение
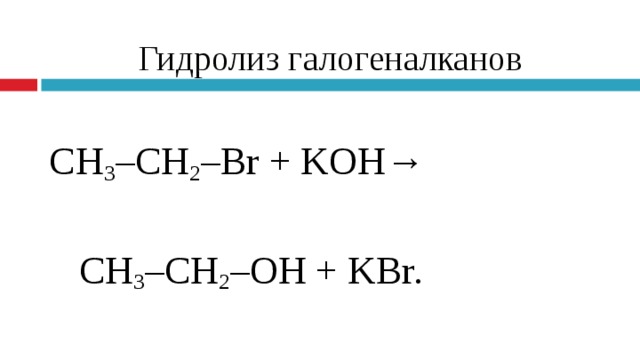
Гидролиз галогеналканов
CH 3 –CH 2 –Br + KOH→
CH 3 –CH 2 – ОН + KBr.
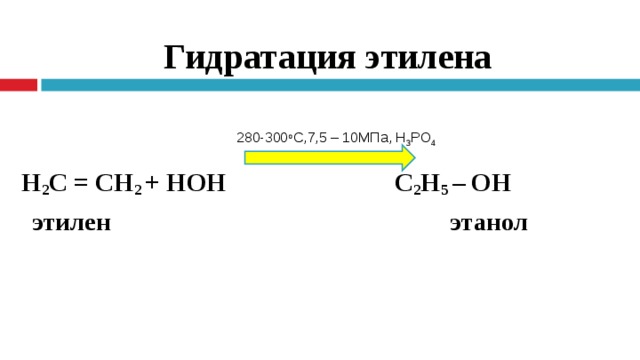
Гидратация этилена
Н 2 С = СН 2 + НОН С 2 Н 5 – ОН
этилен этанол
280-300 о С,7,5 – 10МПа, Н 3 PO 4
280-300 о С,7,5 – 10МПа, Н 3 PO 4
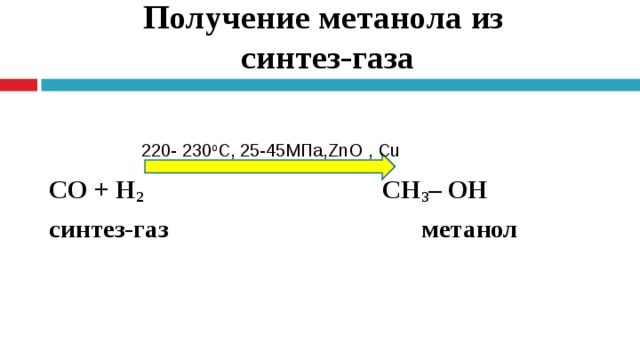
Получение метанола из синтез-газа
СО + Н 2 СН 3 – ОН
синтез-газ метанол
220- 230 о С, 25-45МПа, ZnO , Cu
220- 230 о С, 25-45МПа, ZnO , Cu
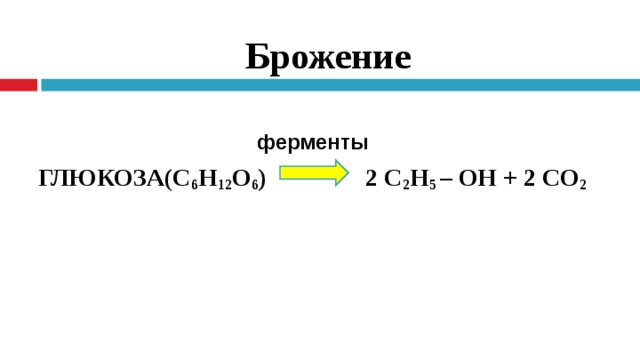
Брожение
ГЛЮКОЗА(С 6 Н 12 О 6 ) 2 С 2 Н 5 – ОН + 2 СО 2
ферменты
ферменты

Физические свойства спиртов
- С увеличением молекулярной массы плотность увеличивается, многоатомные спирты вязкие
- Одноатомные спирты имеют резкий запах, летучи.
- Первые представители С1 – С3 хорошо растворяются в воде .
- Т.о, спирты с большой молекулярной массой в воде будут растворяться хуже.
-

ХИМИЧЕСКИЕ СВОЙСТВА ПРЕДЕЛЬНЫХ ОДНОАТОМНЫХ СПИРТОВ

Реакции горения
- С 2 Н 5 ОН + 3О 2 = 2СО 2 + 3Н 2 О
- С 4 Н 9 ОН + 6 О 2 = 4СО 2 + 5 Н 2 О
- 2С 5 Н 11 ОН + 15 О 2 = 10 СО 2 +12 Н 2 О

Окисление спиртов (качественная реакция на одноатомные спирты)
3CH 3 -CH 2 -OH + K 2 Cr 2 O 7 + 4H 2 SO 4 → 3CH 3 COH + K 2 SO 4 + Cr 2 (SO 4 ) 3 + 7H 2 O
(запах зелёного яблока)
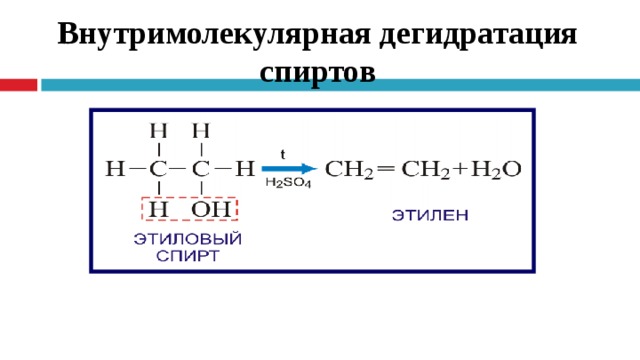
Внутримолекулярная дегидратация спиртов
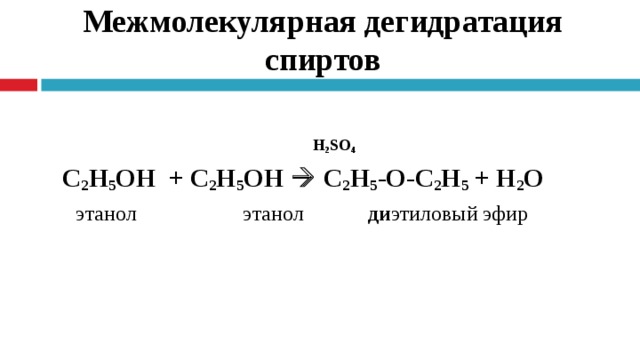
Межмолекулярная дегидратация спиртов
H 2 SO 4
C 2 H 5 OH + C 2 H 5 OH C 2 H 5 -О- C 2 H 5 + H 2 O
этанол этанол ди этиловый эфир
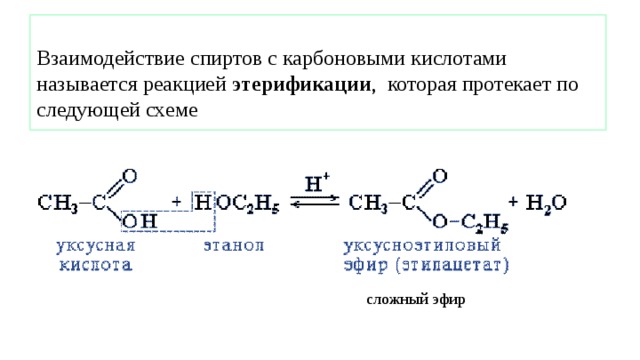
Взаимодействие спиртов с карбоновыми кислотами называется реакцией этерификации , которая протекает по следующей схеме
сложный эфир

Домашнее
задание
§ 17 стр.143-145, упр. № 9
Подготовить сообщение на тему: «Влияние этанола на организм человека"


































