«Простые вещества».
1 вариант
№1. Какова молярная масса водорода?
а) 2 г/моль; б) 2 кг/кмоль; в) 2 мг/ммоль.
№2. Формула для расчета числа структурных частиц вещества:
а)  ; б)
; б) 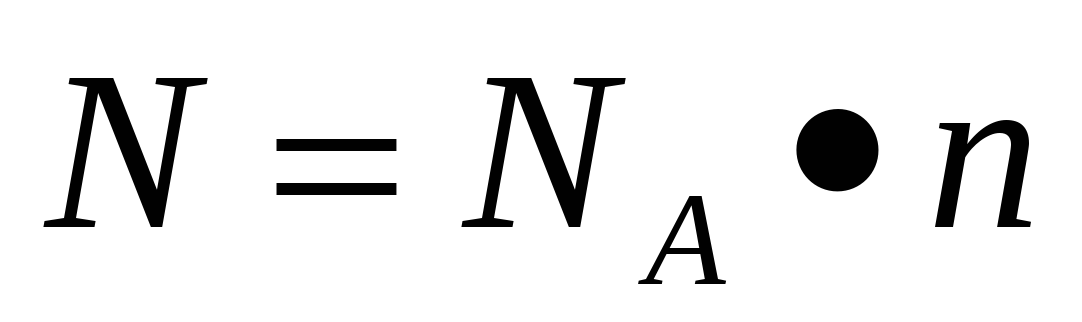 ; в)
; в) 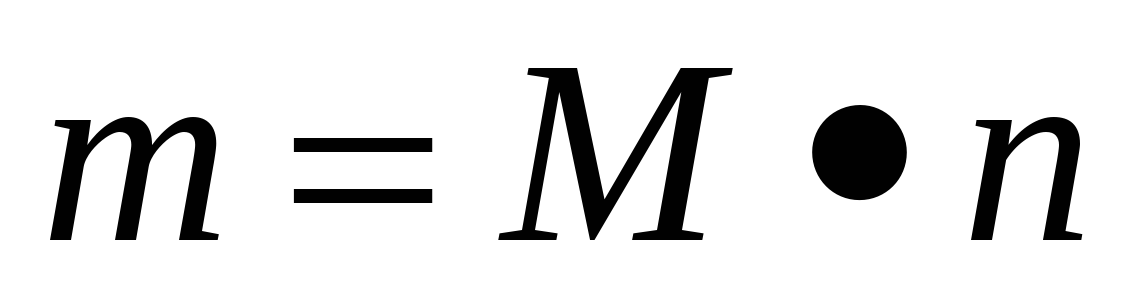
№3. Установите соответствие.
ВЕЛИЧИНЫ
Число структурных частиц вещества
Масса вещества
Количество вещества
Молярная масса
УСЛОВНЫЕ ОБОЗНАЧЕНИЯ ВЕЛИЧИН
а) n
б) N
в) Vm
г) M
д) V
е) NA
ж) m
№ 4. Какой объем займут при н. у. 16 г кислорода О2?
а) 11,2 л; б) 22,4 л; в) 6 л.
№5. Сколько молекул содержится в 180 мг воды?
«Простые вещества».
2 вариант
№1. Какова киломолярная масса водорода?
а) 2 г/моль; б) 2 кг/кмоль; в) 2 мг/ммоль.
№2. Формула для расчета массы вещества:
а) 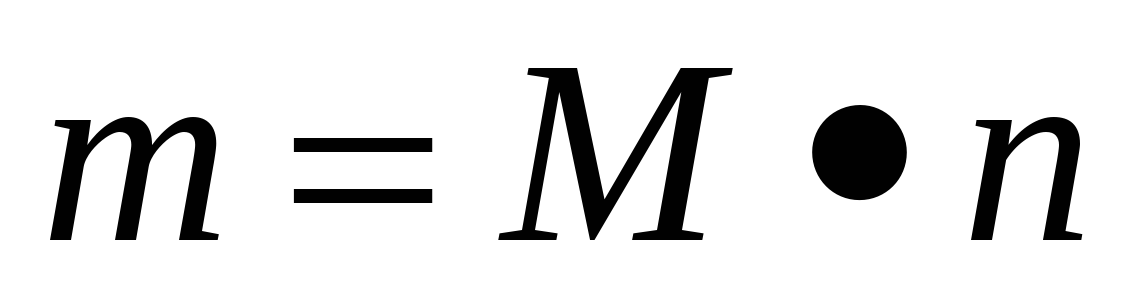 ; б)
; б) 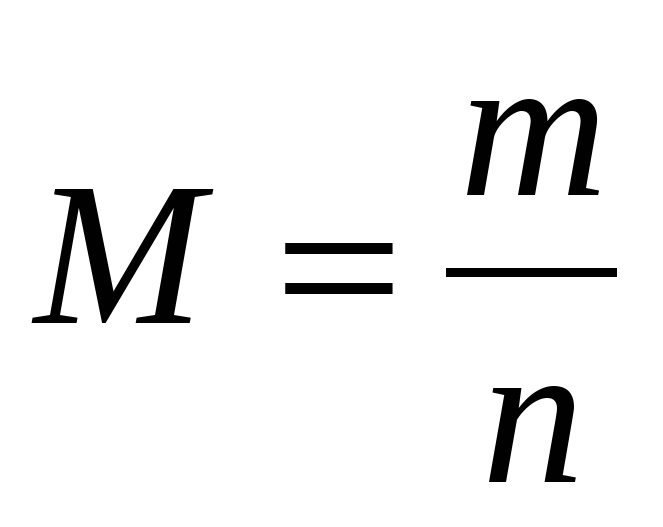 ; в)
; в) 
№3. Установите соответствие.
ВЕЛИЧИНЫ
Масса вещества
Количество вещества
Число структурных частиц вещества
Молярная масса
Постоянная Авогадро
РАЗМЕРНОСТЬ ВЕЛИЧИН
а) г/моль
б) моль
в) кг/кмоль
г) мг
д) кмоль
е) молекул/моль
ж) молекул
з) г
№4. Какой объем займут при н.у. 48 г озона О3?
а) 11,2 л; б) 22,4 л; в) 48 л.
№5. Найти массу 15 · 1023 молекул кислорода О2.
«Простые вещества».
3 вариант
№1. Какова миллимолярная масса водорода?
а) 2 г/моль; б) 2 кг/кмоль; в) 2 мг/ммоль.
№2. Формула для расчета количества вещества, если известна его масса:
а)  ; б)
; б)  ; в)
; в) 
№3. Установите соответствие между левой и правой частями уравнений.
NA = …
m = …
n = …
M = …
а) … = 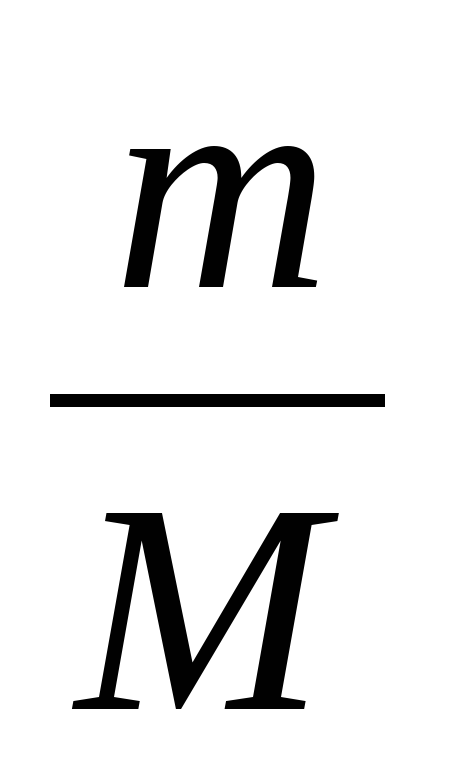
б) … = 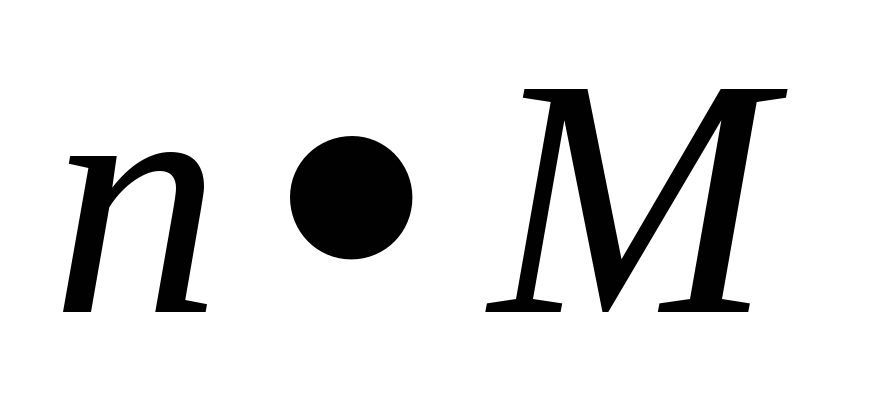
в) … = 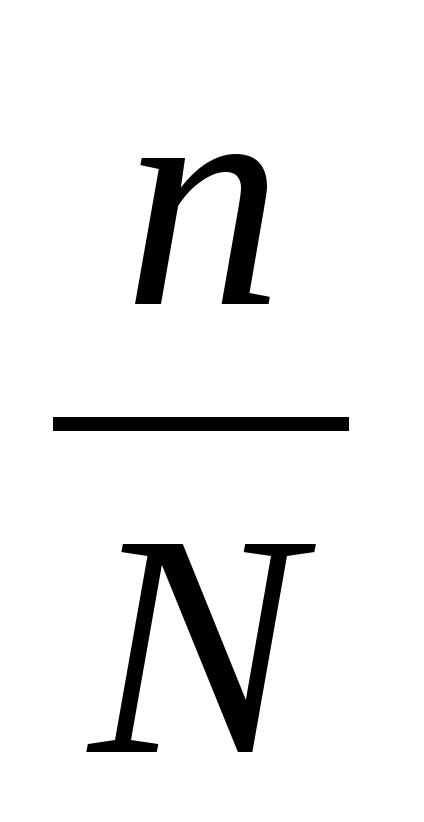
г) … = NA n
n
д) … = 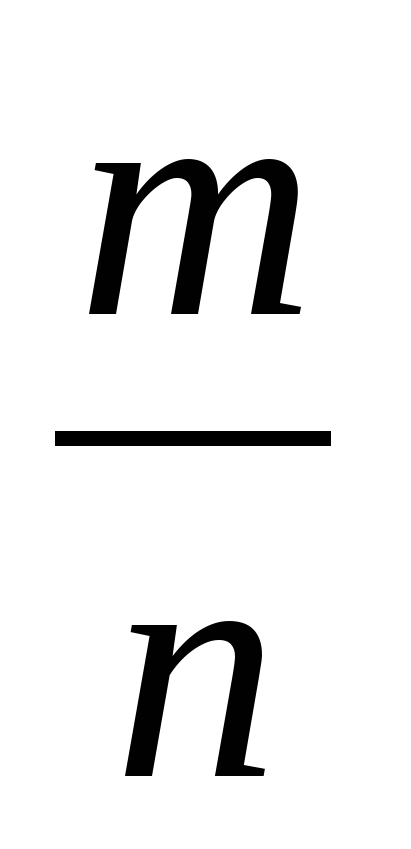
№4. Сколько молекул содержится в 180 г воды?
а) 6 · 1026 молекул; б) 6 · 1020 молекул; в) 6 · 1023 молекул.
№5. Какой объем занимают 14 г азота при н.у.?
«Простые вещества».
4 вариант
№1. Сколько молекул водорода содержится в 1моль водорода?
а) 6 · 1023 молекул; б) 6 · 1026 молекул; в) 6 · 1020 молекул.
№2. Формула для расчета количества вещества, если известно число структурных частиц:
а)  ; б)
; б)  ; в)
; в) 
№3. Установите соответствие.
ВЕЛИЧИНЫ
Масса вещества
Молярная масса
Постоянная Авогадро
Количество вещества
УСЛОВНЫЕ ОБОЗНАЧЕНИЯ ВЕЛИЧИН
а) n
б) NA
в) N
г) m
д) M
№4. Вычислите массу 3 · 1023 молекул озона О3.
а) 12 г; б) 2,4 г; в) 24 г.
№5. Какой объем займут при н. у. 16 г кислорода О2?
«Простые вещества».
5 вариант
№1. Сколько молекул водорода содержится в 1кмоль водорода?
а) 6 · 1023 молекул; б) 6 · 1026 молекул; в) 6 · 1020 молекул.
№2. Формула для расчета количества вещества, если известен его объем:
а)  ; б)
; б)  ; в)
; в) 
№3. Установите соответствие.
ВЕЛИЧИНЫ
Масса вещества
Молярная масса
Количество вещества
Постоянная Авогадро
РАЗМЕРНОСТЬ ВЕЛИЧИН
а) моль
б) г/моль
в) молекул
г) кмоль
д) кг/кмоль
е) г
ж) кг
з) молекул/моль
№4. Найти массу 15 · 1023 молекул кислорода О2.
а) 40 г; б) 80 г; в) 90 г.
№5. Сколько молекул содержится в 44 г углекислого газа СО2?
«Простые вещества».
6 вариант
№1. Сколько молекул водорода содержится в 1ммоль водорода?
а) 6 · 1023 молекул; б) 6 · 1026 молекул; в) 6 · 1020 молекул.
№2. Формула для расчета молярной массы вещества, если известна его масса:
а) 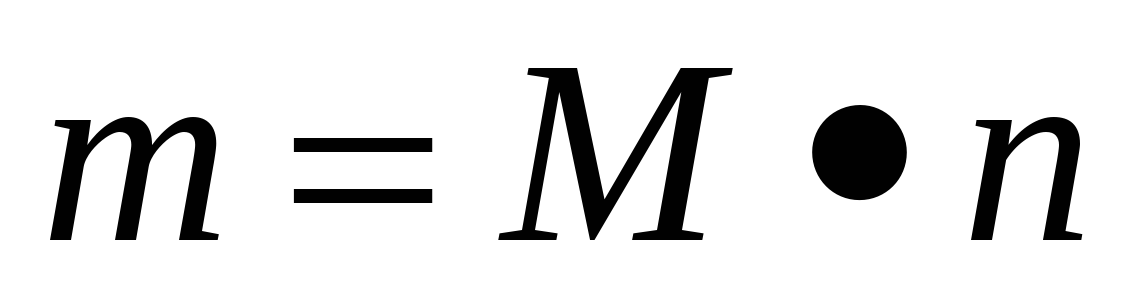 ; б)
; б) 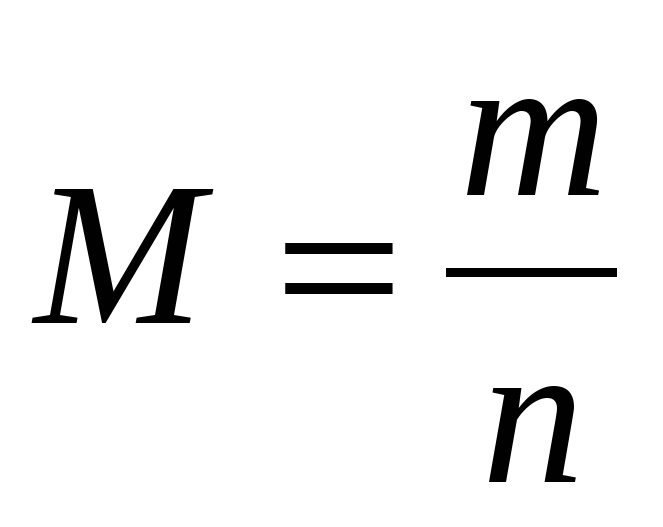 ; в)
; в) 
№3. Установите соответствие между левой и правой частями уравнений.
M = …
m = …
N = …
n = …
а) … = 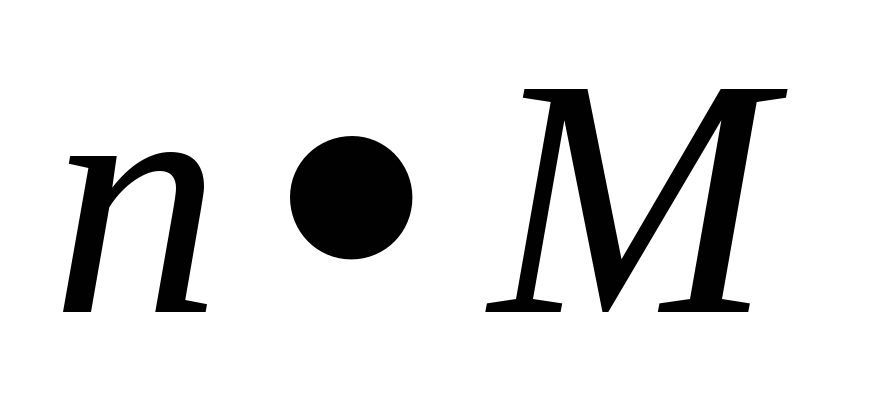
б) … = 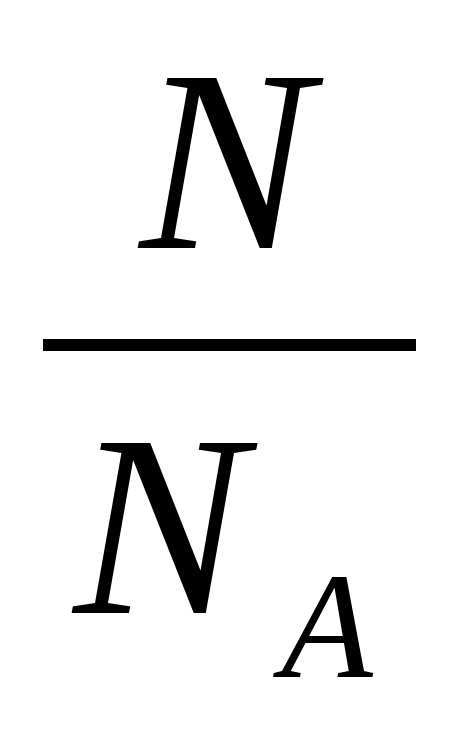
в) … = NA n
n
г) … =
д) … = 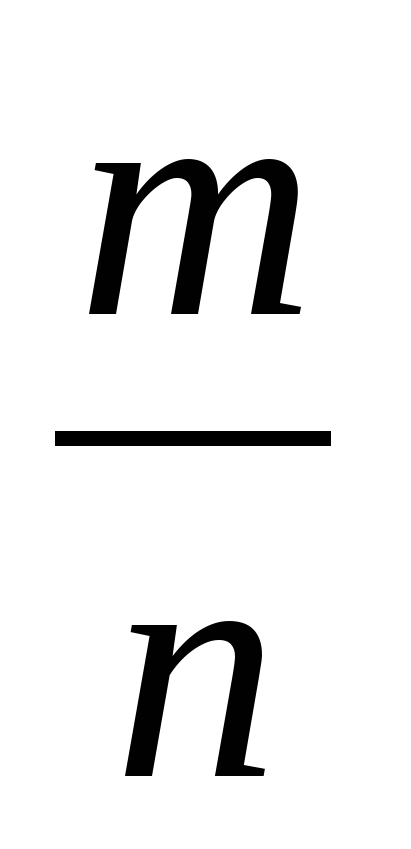
№4. Какое количество вещества составляет 490 г фосфорной кислоты Н3РО4?
а) 0,25 моль; б) 5 моль; в) 2,5 моль.
№5. Какой объем займут при н.у. 48 г озона О3?
«Простые вещества».
7 вариант
№1. Сколько будут весить 12 · 1020 молекул водорода?
а) 4мг; б) 4г; в) 4кг.
№2. Формула для расчета молярной массы вещества, если известно его количество вещества:
а) 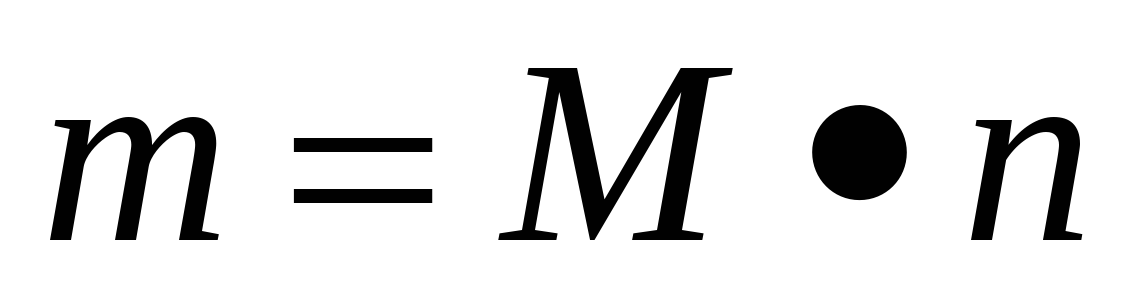 ; б)
; б) 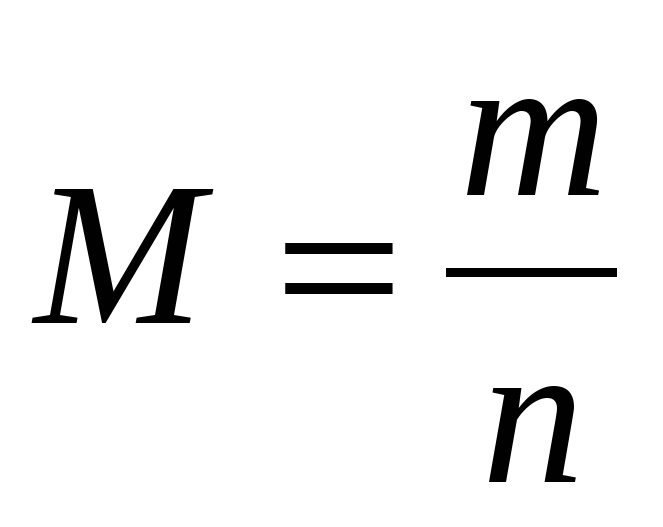 ; в)
; в) 
№3. Установите соответствие.
ВЕЛИЧИНЫ
Молярный объем газа
Количество вещества
Постоянная Авогадро
Объем газа
УСЛОВНЫЕ ОБОЗНАЧЕНИЯ ВЕЛИЧИН
а) M
б) N
в) V
г) NA
д) Vm
е) n
ж) m
№4. Какое количество вещества составляет 49 г серной кислоты Н2SО4?
а) 0,5 моль; б) 5 моль; в) 0,25 моль.
№5. Какова масса 33,6л углекислого газа СО2?
«Простые вещества».
8 вариант
№1. Сколько будут весить 12 · 1023 молекул водорода?
а) 4мг; б) 4г; в) 4кг.
№2. Формула для расчета объема вещества, если известно его количество вещества:
а) ; б)  ; в)
; в)
№3. Установите соответствие.
ВЕЛИЧИНЫ
Количество вещества
Молярный объем
Объем газа
РАЗМЕРНОСТЬ ВЕЛИЧИН
а) м3
б) м3/кмоль
в) кмоль
г) л/моль
д) моль
е) л
№4. Сколько молекул содержится в 342 г гидроксида бария Ва(ОН)2 ?
а) 6 · 1023 молекул; б) 12 · 1023 молекул;
в) 9 · 1023 молекул.
№5. Какую массу имеют 11,2 мл (н.у.) кислорода О2?
«Простые вещества».
9 вариант
№1. Сколько будут весить 12 · 1026 молекул водорода?
а) 4мг; б) 4г; в) 4кг.
№2. Формула для расчета числа структурных частиц вещества:
а)  ; б)
; б) 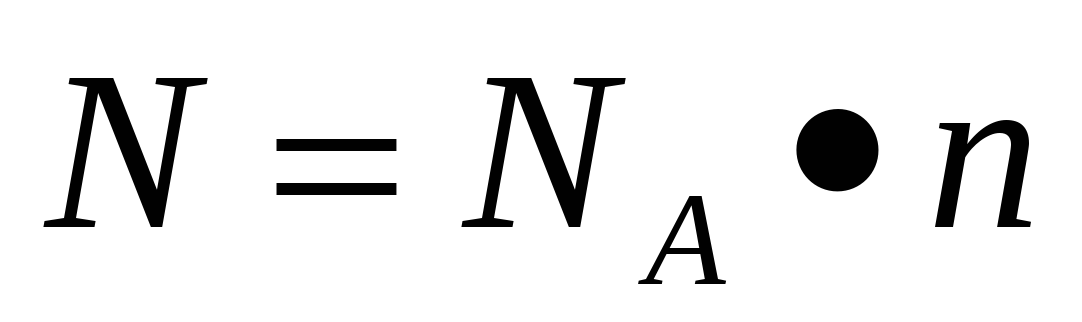 ; в)
; в) 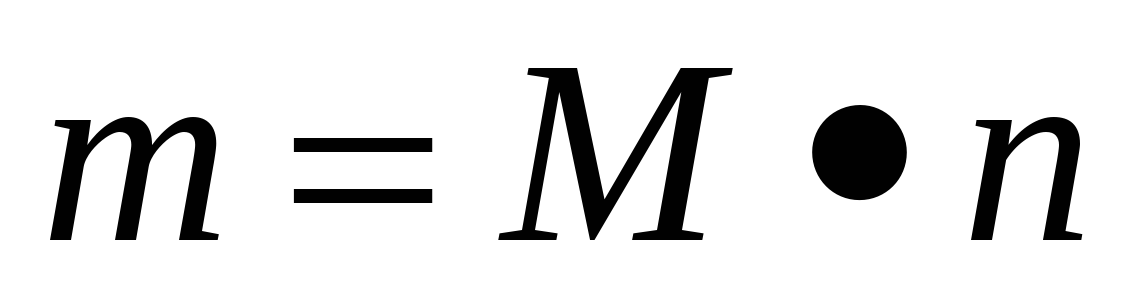
№3. Установите соответствие.
КОЛИЧЕСТВЕННЫЕ ХАРАКТЕРИСТИКИ ВЕЩЕСТВА
Масса вещества
Количество вещества
Объем
Число структурных частиц
ФОРМУЛЫ ДЛЯ РАСЧЕТА
а) 
б) 
в) 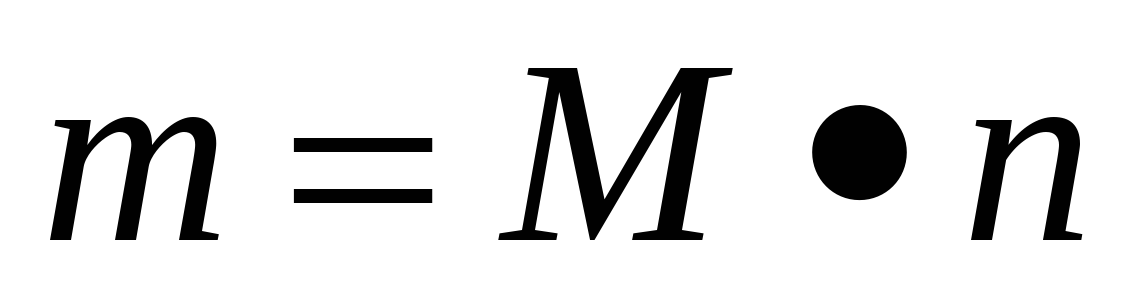
г) 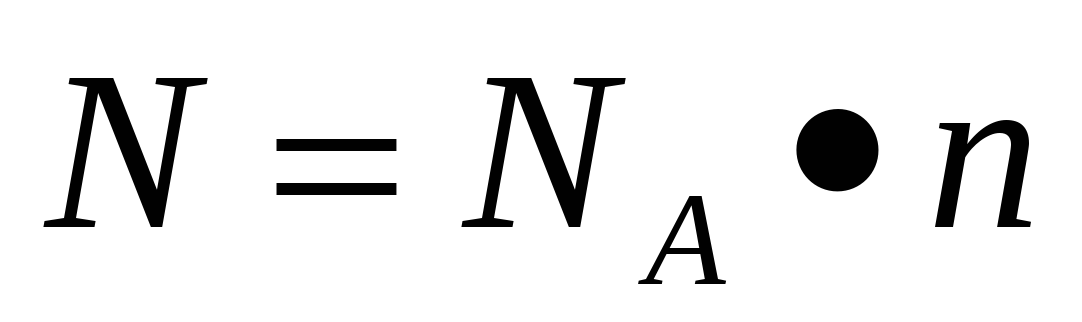
д)
е) 
№4. Какой объем занимают 14 г азота при н.у.?
а) 48 л; б) 22,4 л; в) 11,2 л.
№5. Сколько молекул содержится в 180 г воды?
«Простые вещества».
10 вариант
№1. Какой объем займут 12 · 1020 молекул водорода?
а) 44,8 мл; б) 44,8 л; в) 44,8 м3.
№2. Формула для расчета массы вещества:
а) 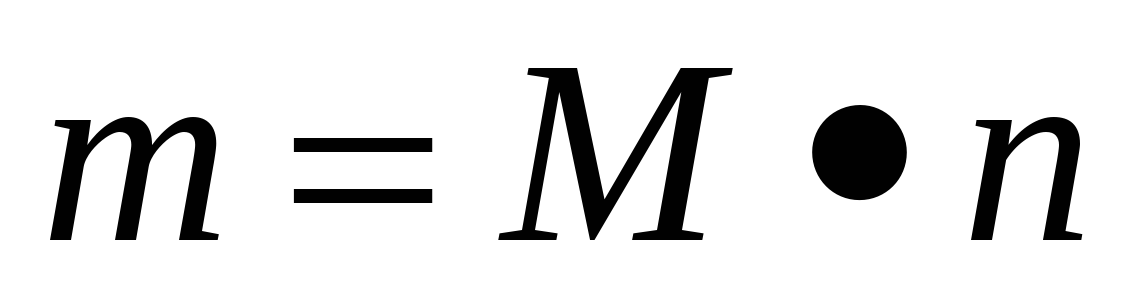 ; б)
; б) 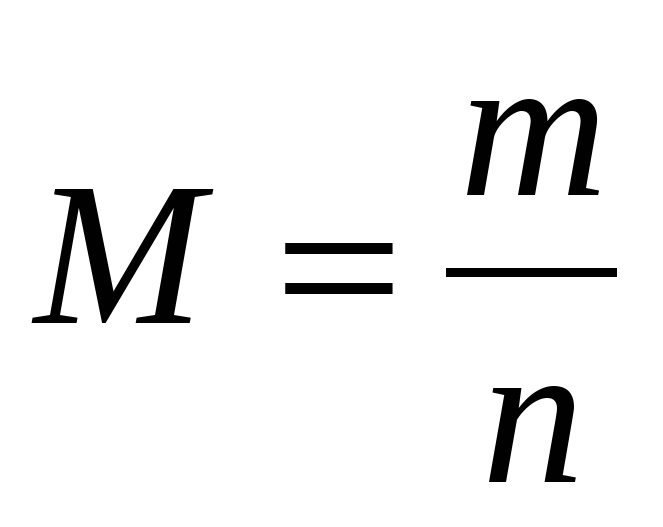 ; в)
; в) 
№3. Установите соответствие.
ВЕЛИЧИНЫ
Молярный объем
Объем газа
Объем кмоль газа
Постоянная Авогадро
Количество вещества
РАЗМЕРНОСТЬ ВЕЛИЧИН
а) м3
б) моль
в) м3/кмоль
г) л
д) л/моль
е) молекул/моль
ж) ммоль
з) мл
№4. Какой объем (н.у.) занимают 12 · 1023 молекул озона?
а) 48 л; б) 44,8 л; в) 11,2 л.
№5. Рассчитайте массу 0,25 моль карбоната кальция СаСО3.
«Простые вещества».
11 вариант
№1. Какой объем займут 12 · 1023 молекул водорода?
а) 44,8 мл; б) 44,8 л; в) 44,8 м3.
№2. Формула для расчета количества вещества, если известна его масса:
а)  ; б)
; б)  ; в)
; в) 
№3. Установите соответствие.
КОЛИЧЕСТВЕННЫЕ ХАРАКТЕРИСТИКИ ВЕЩЕСТВА
Объем
Количество вещества
Число структурных частиц
Масса вещества
ФОРМУЛЫ ДЛЯ РАСЧЕТА
а) 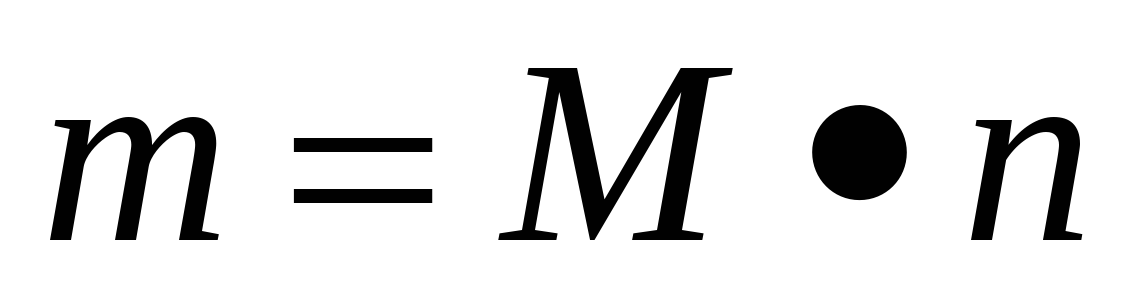
б) 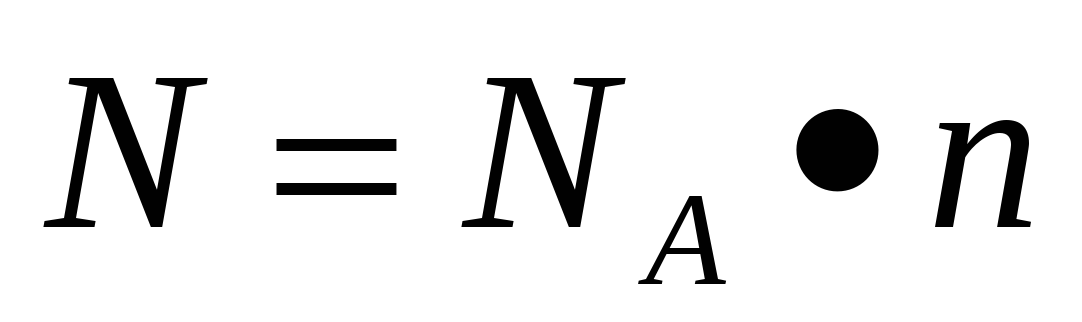
в)
г) 
д) 
е) 
№4. Какой объем (н. у.) занимают 3 · 1023 молекул водорода?
а) 22,4 л; б) 44,8 л; в) 11,2 л.
№5. Рассчитайте массу 0,25 моль железа.
«Простые вещества».
12 вариант
№1. Какой объем займут 12 · 1026 молекул водорода?
а) 44,8 мл; б) 44,8 л; в) 44,8 м3.
№2. Формула для расчета количества вещества, если известно число структурных частиц:
а)  ; б)
; б)  ; в)
; в) 
№3. Установите соответствие между левой и правой частями уравнений.
M = …
m = …
N = …
n = …
а) … = 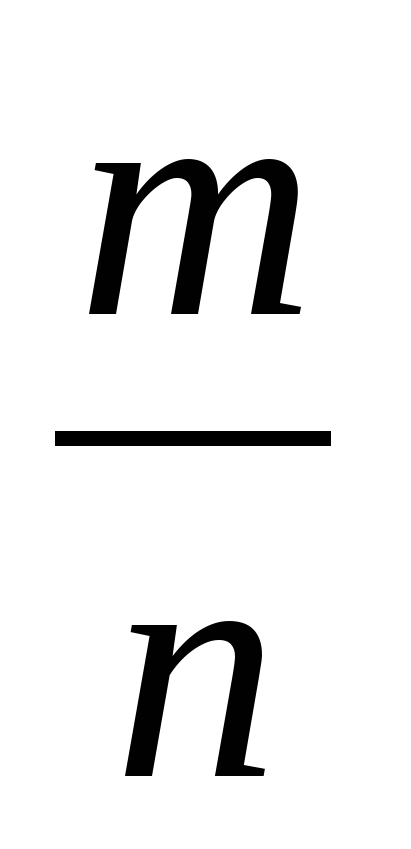
б) … = 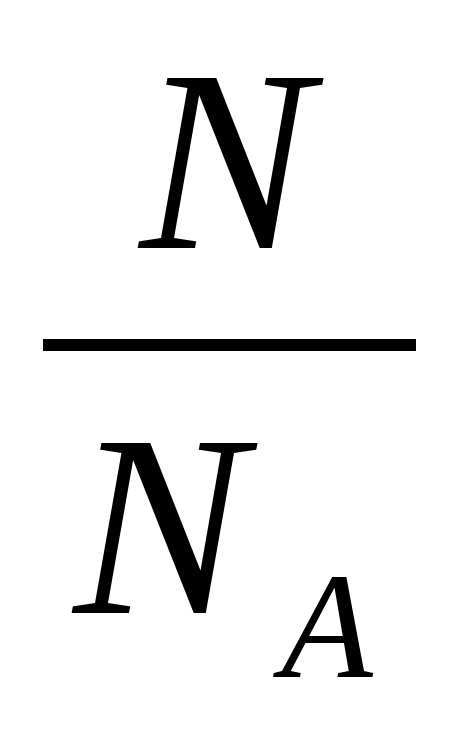
в) … = 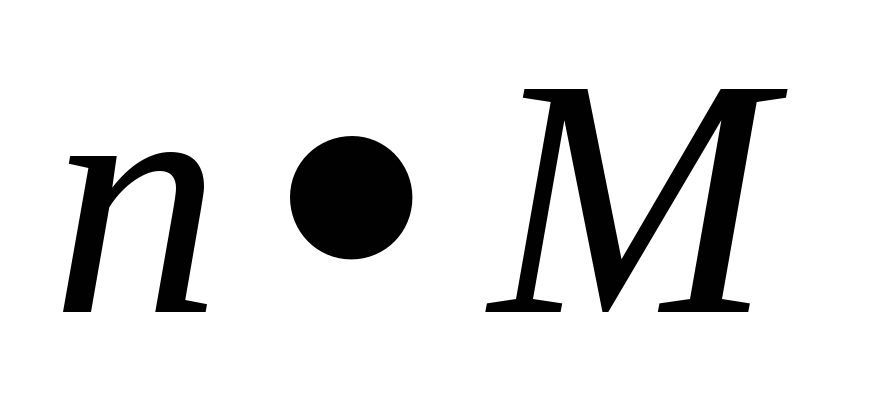
г) … =
д) … = NA n
n
№4. Какова масса 33,6л углекислого газа СО2?
а) 66 г; б) 33,6 г; в) 66,3 г.
№5. Какой объем (н.у.) занимают 12 · 1023 молекул озона О3?
«Простые вещества».
13 вариант
№1. Какова молярная масса кислорода?
а) 32 г/моль; б) 32 кг/кмоль; в) 32 мг/ммоль.
№2. Формула для расчета количества вещества, если известен его объем:
а)  ; б)
; б)  ; в)
; в) 
№3. Установите соответствие.
ВЕЛИЧИНЫ
Молярный объем газа (н.у.)
Количество вещества
Постоянная Авогадро
Молярная масса
УСЛОВНЫЕ ОБОЗНАЧЕНИЯ ВЕЛИЧИН
а) M
б) m
в) n
г) N
д) NA
е) V
ж) Vm
№4. Какой объем (н.у.) займут 18 · 1023 молекул сероводорода H2S?
а) 22,4 л; б) 66,7 л; в) 81,2 л.
№5. Какова масса 33,6л углекислого газа СО2?
«Простые вещества».
14 вариант
№1. Какова киломолярная масса кислорода?
а) 32 г/моль; б) 32 кг/кмоль; в) 32 мг/ммоль.
№2. Формула для расчета молярной массы вещества, если известна его масса:
а) 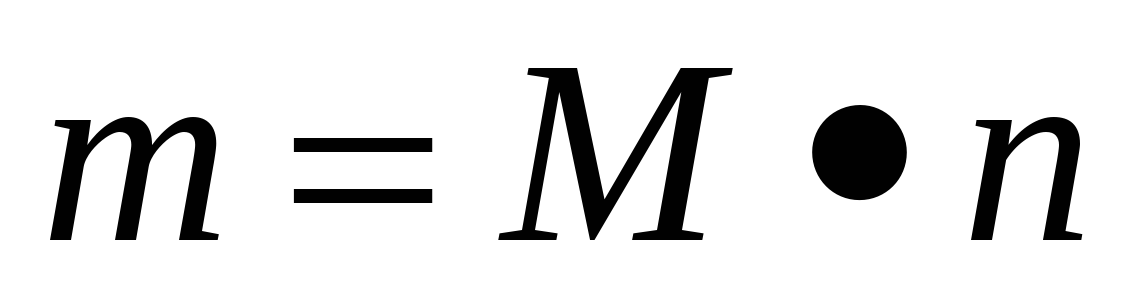 ; б)
; б) 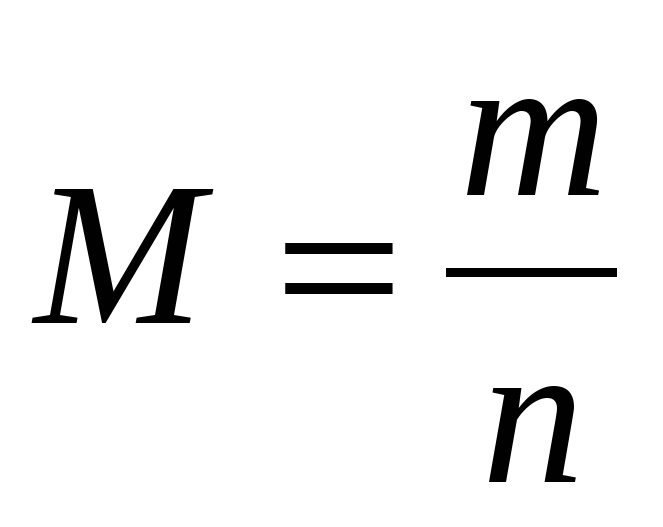 ; в)
; в) 
№3. Установите соответствие.
КОЛИЧЕСТВЕННЫЕ ХАРАКТЕРИСТИКИ ВЕЩЕСТВА
Объем
Количество вещества
Число структурных частиц
Масса вещества
ФОРМУЛЫ ДЛЯ РАСЧЕТА
а) 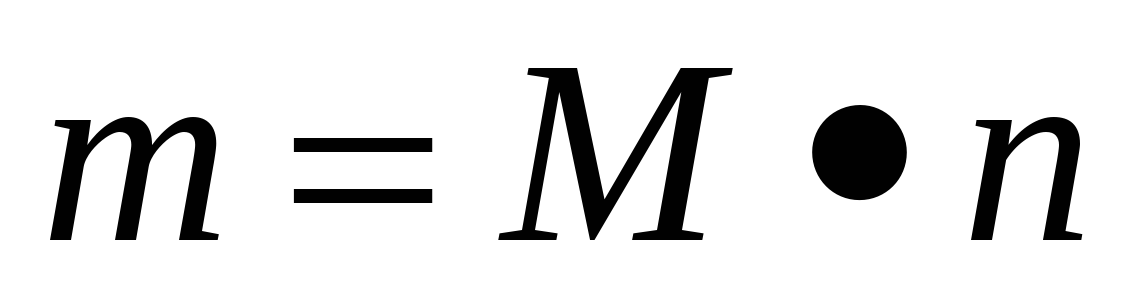
б) 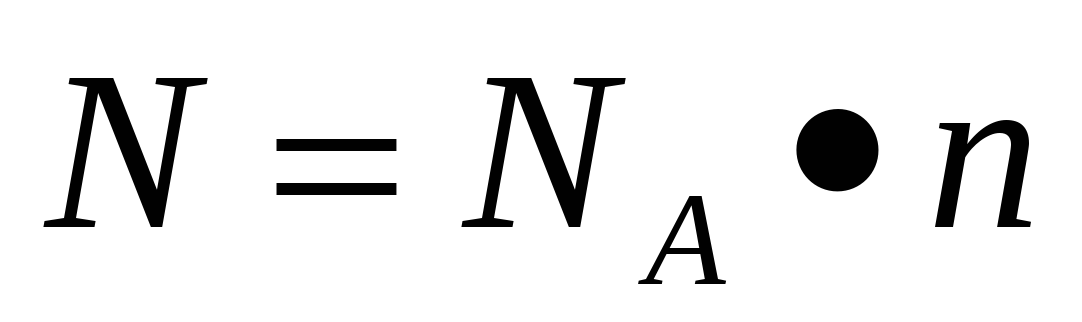
в)
г) 
д) 
е) 
№4. Какой объем займут 640 г кислорода О2 при н.у.?
а) 4,48 л; б) 44,8 л; в) 448 л.
№5. Сколько молекул будет содержать 1,5моль углекислого газа СО2?
«Простые вещества».
15 вариант
№1. Какова миллимолярная масса кислорода?
а) 32 г/моль; б) 32 кг/кмоль; в) 32 мг/ммоль.
№2. Формула для расчета объема вещества, если известно его количество вещества:
а) ; б)  ; в)
; в)
№3. Установите соответствие.
ВЕЛИЧИНЫ
Количество вещества
Молярный объем
Постоянная Авогадро
Объем газа
Объем кмоль газа
РАЗМЕРНОСТЬ ВЕЛИЧИН
а) м3
б) моль
в) м3/кмоль
г) л/моль
д) л
е) молекул/моль
ж) мл
з) ммоль
№4. Какой объем займут при н.у. 70 г оксида углерода (II) СО?
а) 56 л; б) 70 л; в) 44 л.
№5. Какое количество вещества составляет 49 г серной кислоты Н2SО4?
«Простые вещества».
16 вариант
№1. Какова молярная масса водорода?
а) 2 г/моль; б) 2 кг/кмоль; в) 2 мг/ммоль.
№2. Формула для расчета числа структурных частиц вещества:
а)  ; б)
; б) 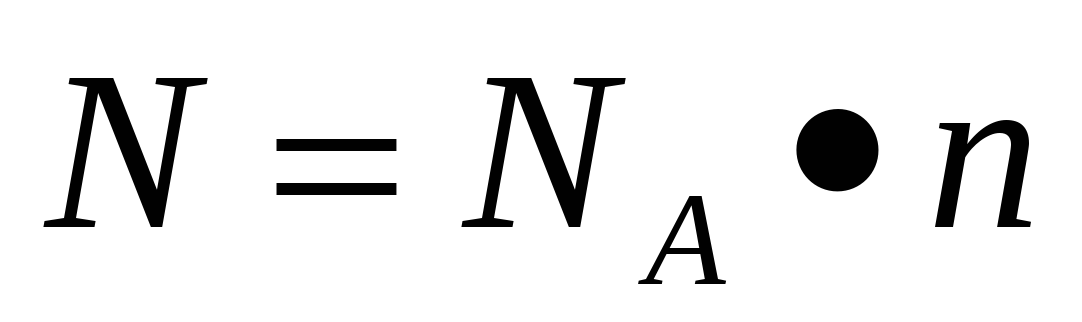 ; в)
; в) 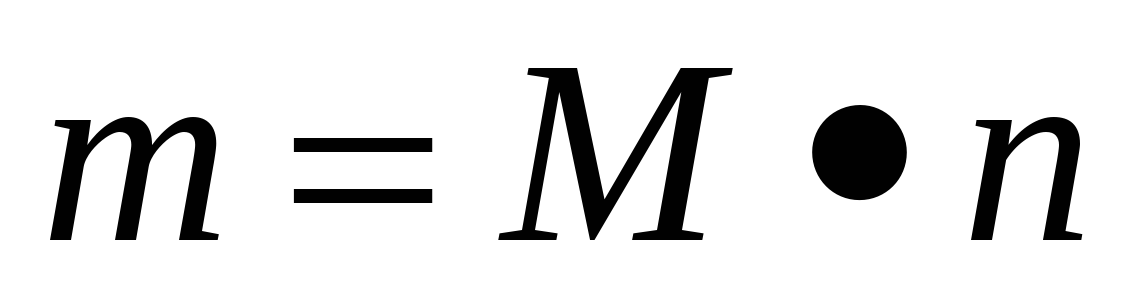
№3. Установите соответствие.
ВЕЛИЧИНЫ
Число структурных частиц вещества
Масса вещества
Количество вещества
Молярная масса
УСЛОВНЫЕ ОБОЗНАЧЕНИЯ ВЕЛИЧИН
а) n
б) N
в) Vm
г) M
д) V
е) NA
ж) m
№ 4. Какой объем займут при н. у. 16 г кислорода О2?
а) 11,2 л; б) 22,4 л; в) 6 л.
№5. Сколько молекул содержится в 180 мг воды?
«Простые вещества».
17 вариант
№1. Какова киломолярная масса водорода?
а) 2 г/моль; б) 2 кг/кмоль; в) 2 мг/ммоль.
№2. Формула для расчета массы вещества:
а) 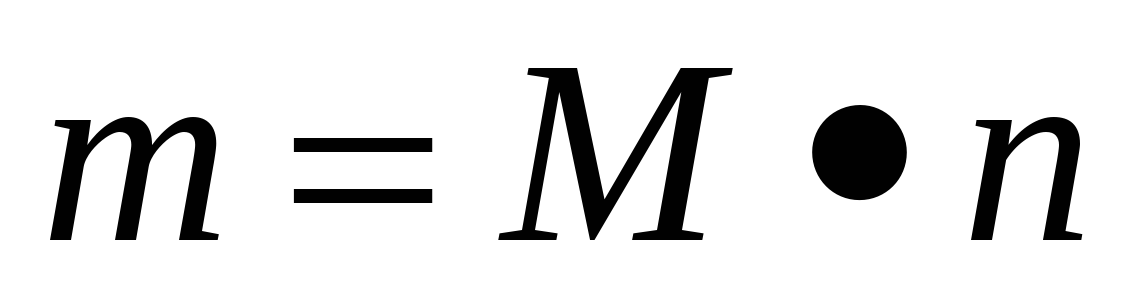 ; б)
; б) 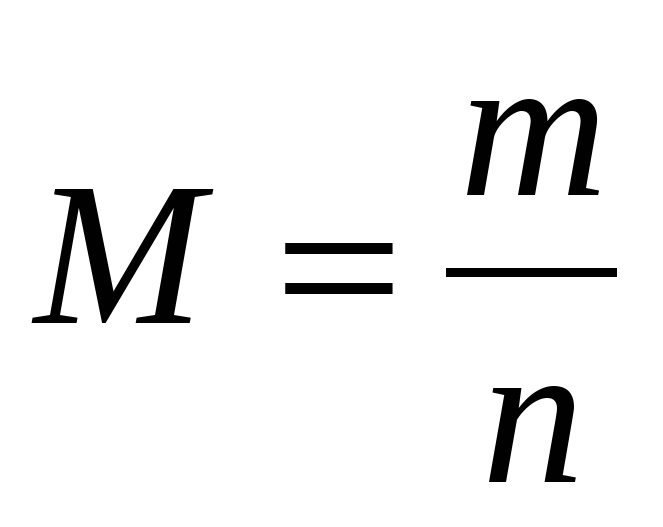 ; в)
; в) 
№3. Установите соответствие.
ВЕЛИЧИНЫ
Масса вещества
Количество вещества
Число структурных частиц вещества
Молярная масса
Постоянная Авогадро
РАЗМЕРНОСТЬ ВЕЛИЧИН
а) г/моль
б) моль
в) кг/кмоль
г) мг
д) кмоль
е) молекул/моль
ж) молекул
з) г
№4. Какой объем займут при н.у. 48 г озона О3?
а) 11,2 л; б) 22,4 л; в) 48 л.
№5. Найти массу 15 · 1023 молекул кислорода О2.
«Простые вещества».
18 вариант
№1. Какова миллимолярная масса водорода?
а) 2 г/моль; б) 2 кг/кмоль; в) 2 мг/ммоль.
№2. Формула для расчета количества вещества, если известна его масса:
а)  ; б)
; б)  ; в)
; в) 
№3. Установите соответствие между левой и правой частями уравнений.
NA = …
m = …
n = …
M = …
а) … = 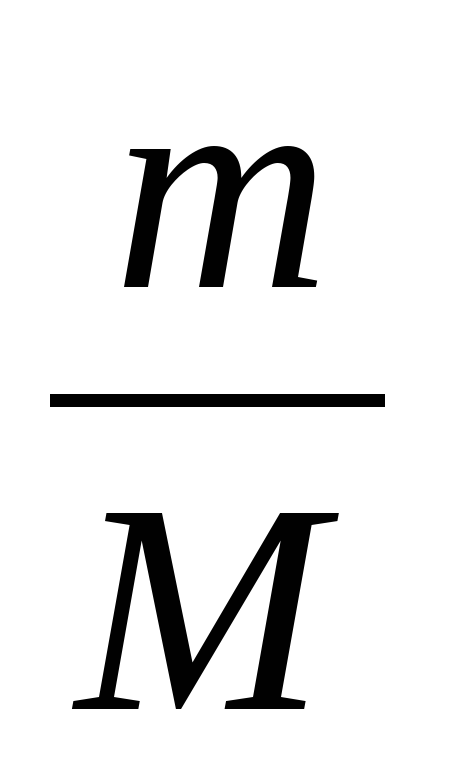
б) … = 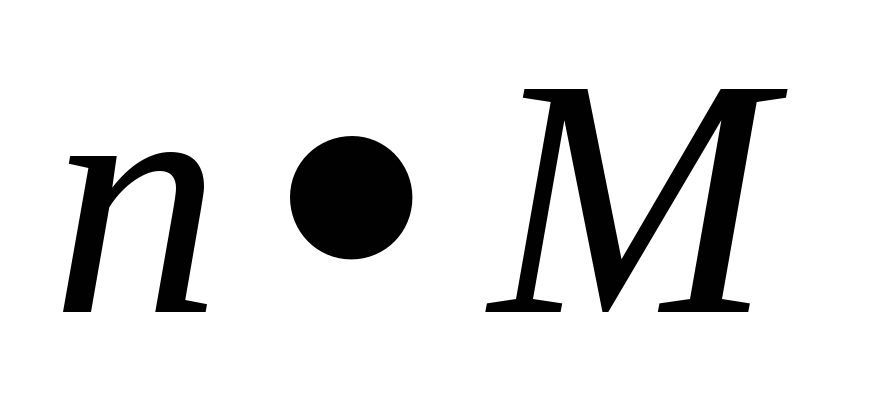
в) … = 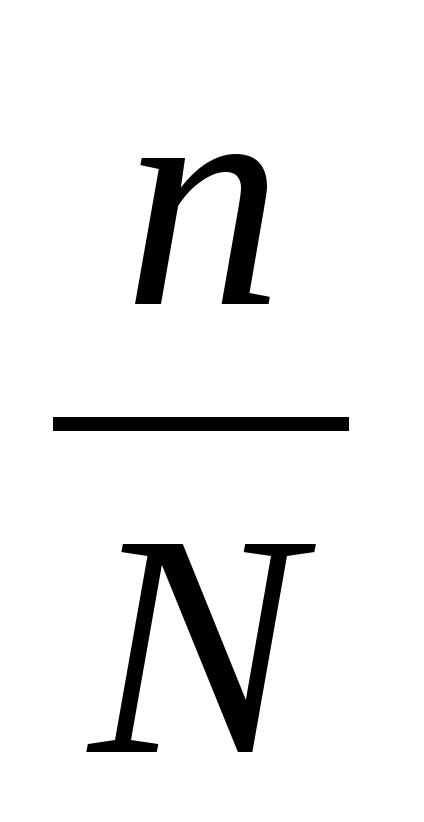
г) … = NA n
n
д) … = 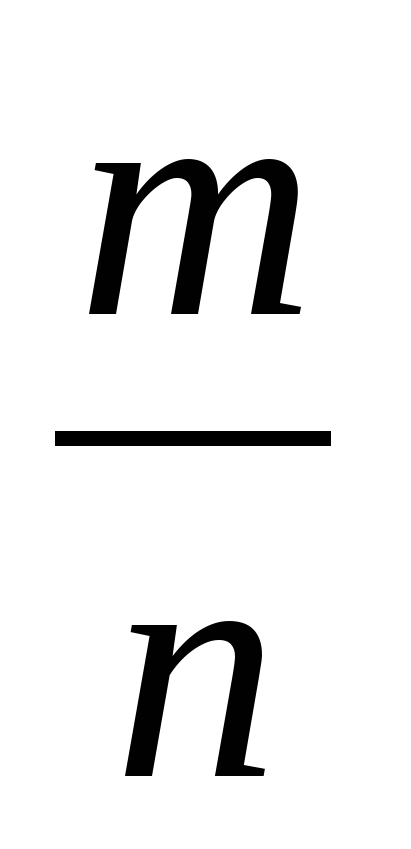
№4. Сколько молекул содержится в 180 г воды?
а) 6 · 1026 молекул; б) 6 · 1020 молекул; в) 6 · 1023 молекул.
№5. Какой объем занимают 14 г азота при н.у.?
«Простые вещества».
19 вариант
№1. Сколько молекул водорода содержится в 1моль водорода?
а) 6 · 1023 молекул; б) 6 · 1026 молекул; в) 6 · 1020 молекул.
№2. Формула для расчета количества вещества, если известно число структурных частиц:
а)  ; б)
; б)  ; в)
; в) 
№3. Установите соответствие.
ВЕЛИЧИНЫ
Масса вещества
Молярная масса
Постоянная Авогадро
Количество вещества
УСЛОВНЫЕ ОБОЗНАЧЕНИЯ ВЕЛИЧИН
а) n
б) NA
в) N
г) m
д) M
№4. Вычислите массу 3 · 1023 молекул озона О3.
а) 12 г; б) 2,4 г; в) 24 г.
№5. Какой объем займут при н. у. 16 г кислорода О2?
«Простые вещества».
20 вариант
№1. Сколько молекул водорода содержится в 1кмоль водорода?
а) 6 · 1023 молекул; б) 6 · 1026 молекул; в) 6 · 1020 молекул.
№2. Формула для расчета количества вещества, если известен его объем:
а)  ; б)
; б)  ; в)
; в) 
№3. Установите соответствие.
ВЕЛИЧИНЫ
Масса вещества
Молярная масса
Количество вещества
Постоянная Авогадро
РАЗМЕРНОСТЬ ВЕЛИЧИН
а) моль
б) г/моль
в) молекул
г) кмоль
д) кг/кмоль
е) г
ж) кг
з) молекул/моль
№4. Найти массу 15 · 1023 молекул кислорода О2.
а) 40 г; б) 80 г; в) 90 г.
№5. Сколько молекул содержится в 44 г углекислого газа СО2?
«Простые вещества».
21 вариант
№1. Сколько молекул водорода содержится в 1ммоль водорода?
а) 6 · 1023 молекул; б) 6 · 1026 молекул; в) 6 · 1020 молекул.
№2. Формула для расчета молярной массы вещества, если известна его масса:
а) 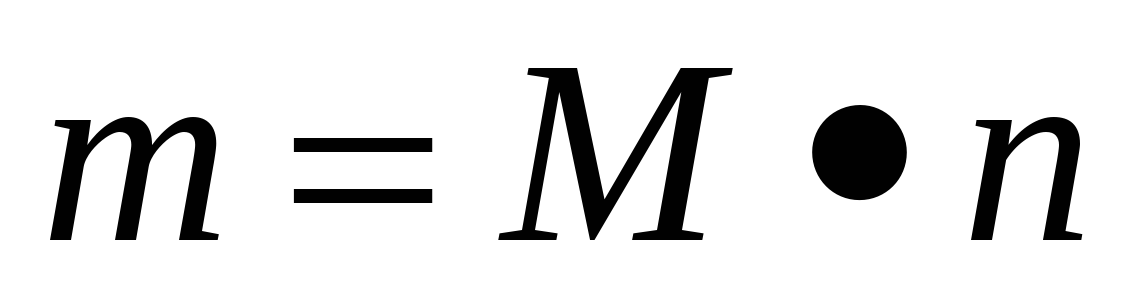 ; б)
; б) 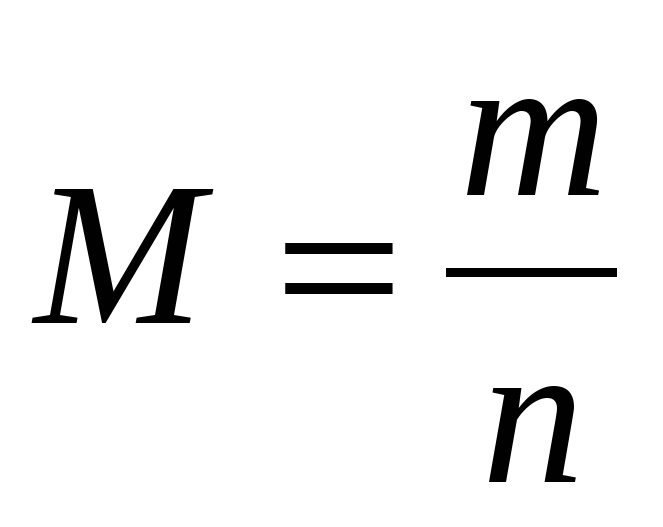 ; в)
; в) 
№3. Установите соответствие между левой и правой частями уравнений.
M = …
m = …
N = …
n = …
а) … = 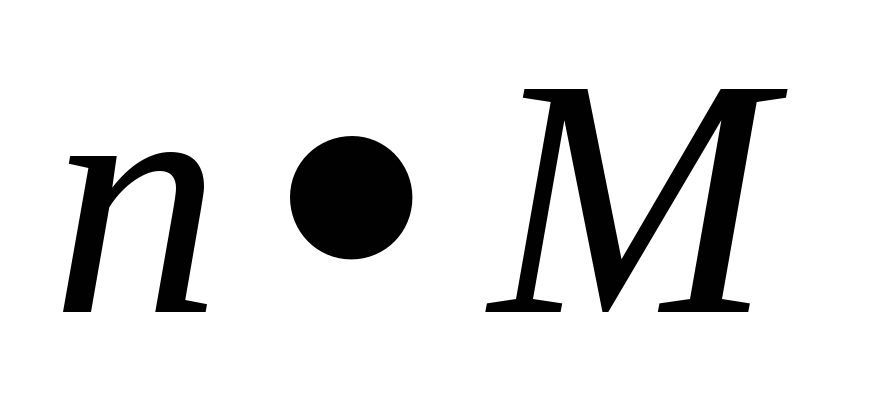
б) … = 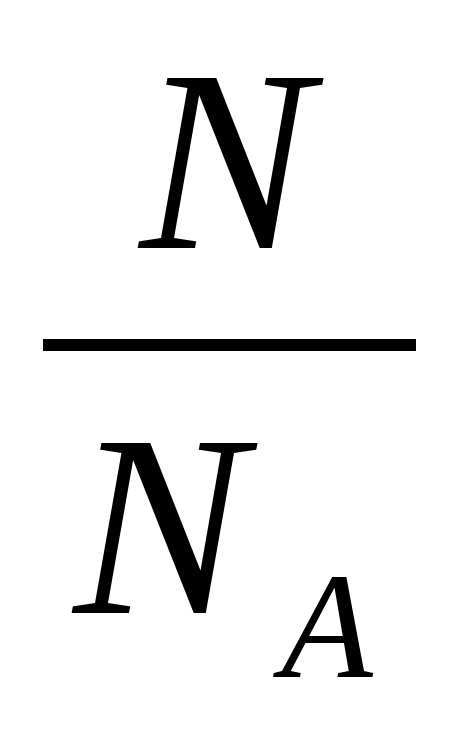
в) … = NA n
n
г) … =
д) … = 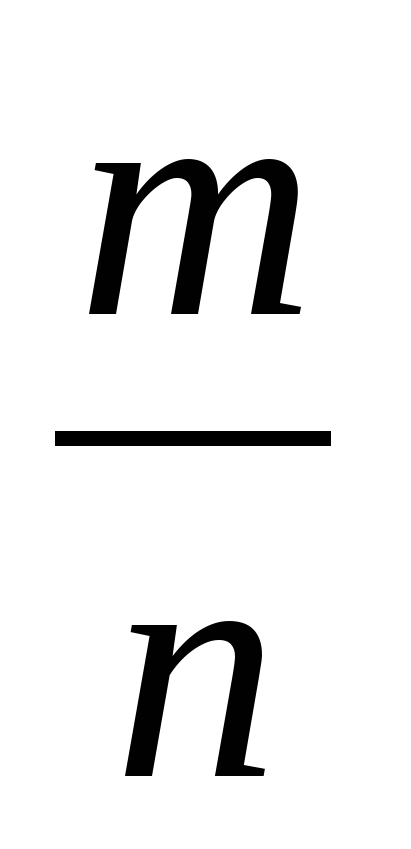
№4. Какое количество вещества составляет 490 г фосфорной кислоты Н3РО4?
а) 0,25 моль; б) 5 моль; в) 2,5 моль.
№5. Какой объем займут при н.у. 48 г озона О3?
«Простые вещества».
22 вариант
№1. Сколько будут весить 12 · 1020 молекул водорода?
а) 4мг; б) 4г; в) 4кг.
№2. Формула для расчета молярной массы вещества, если известно его количество вещества:
а) 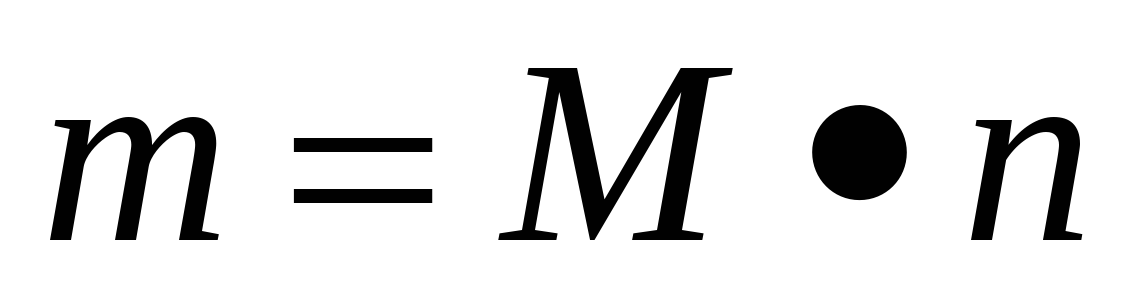 ; б)
; б) 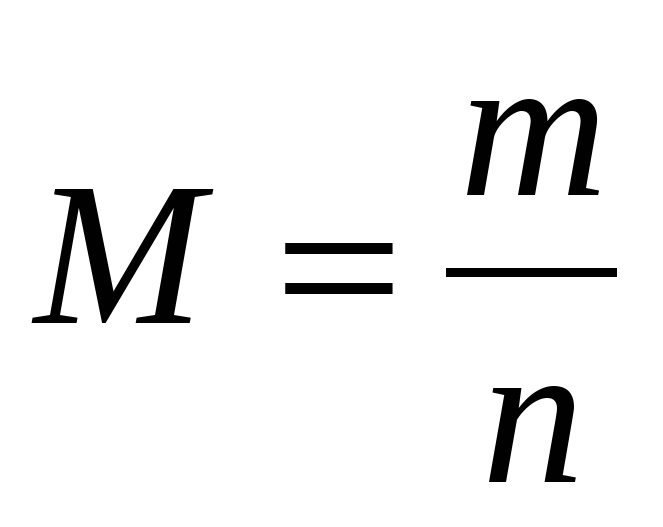 ; в)
; в) 
№3. Установите соответствие.
ВЕЛИЧИНЫ
Молярный объем газа
Количество вещества
Постоянная Авогадро
Объем газа
УСЛОВНЫЕ ОБОЗНАЧЕНИЯ ВЕЛИЧИН
а) M
б) N
в) V
г) NA
д) Vm
е) n
ж) m
№4. Какое количество вещества составляет 49 г серной кислоты Н2SО4?
а) 0,5 моль; б) 5 моль; в) 0,25 моль.
№5. Какова масса 33,6л углекислого газа СО2?
«Простые вещества».
23 вариант
№1. Сколько будут весить 12 · 1023 молекул водорода?
а) 4мг; б) 4г; в) 4кг.
№2. Формула для расчета объема вещества, если известно его количество вещества:
а) ; б)  ; в)
; в)
№3. Установите соответствие.
ВЕЛИЧИНЫ
Количество вещества
Молярный объем
Объем газа
РАЗМЕРНОСТЬ ВЕЛИЧИН
а) м3
б) м3/кмоль
в) кмоль
г) л/моль
д) моль
е) л
№4. Сколько молекул содержится в 342 г гидроксида бария Ва(ОН)2 ?
а) 6 · 1023 молекул; б) 12 · 1023 молекул;
в) 9 · 1023 молекул.
№5. Какую массу имеют 11,2 мл (н.у.) кислорода О2?
«Простые вещества».
24 вариант
№1. Сколько будут весить 12 · 1026 молекул водорода?
а) 4мг; б) 4г; в) 4кг.
№2. Формула для расчета числа структурных частиц вещества:
а)  ; б)
; б) 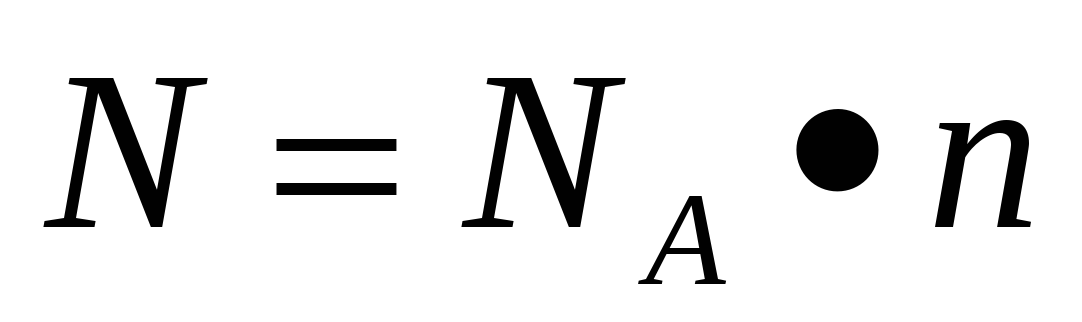 ; в)
; в) 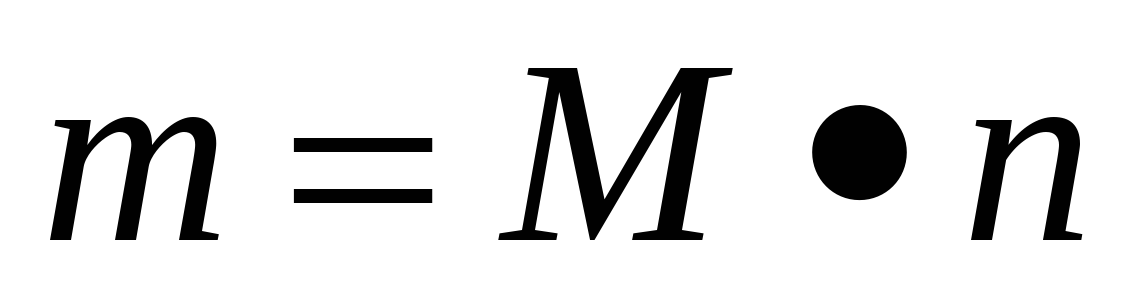
№3. Установите соответствие.
КОЛИЧЕСТВЕННЫЕ ХАРАКТЕРИСТИКИ ВЕЩЕСТВА
Масса вещества
Количество вещества
Объем
Число структурных частиц
ФОРМУЛЫ ДЛЯ РАСЧЕТА
а) 
б) 
в) 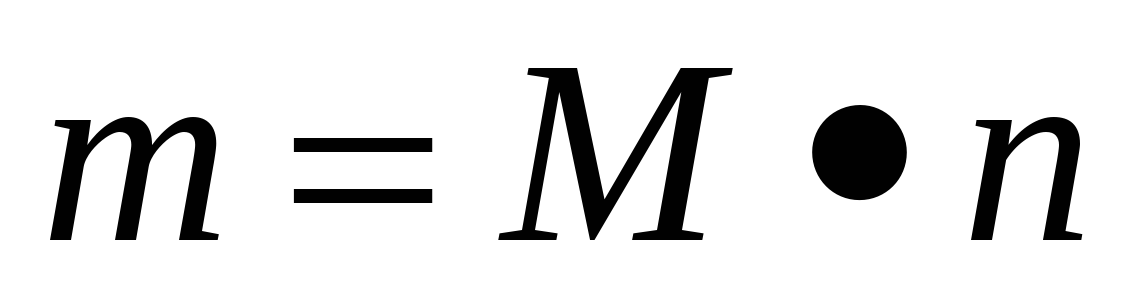
г) 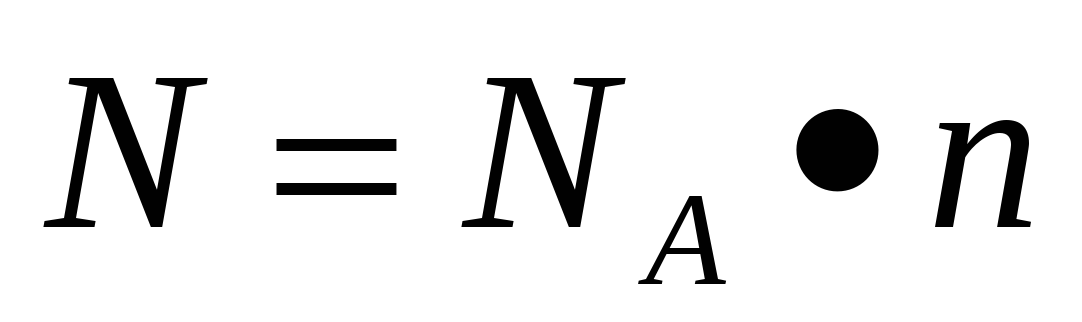
д)
е) 
№4. Какой объем занимают 14 г азота при н.у.?
а) 48 л; б) 22,4 л; в) 11,2 л.
№5. Сколько молекул содержится в 180 г воды?
«Простые вещества».
25 вариант
№1. Какой объем займут 12 · 1020 молекул водорода?
а) 44,8 мл; б) 44,8 л; в) 44,8 м3.
№2. Формула для расчета массы вещества:
а) 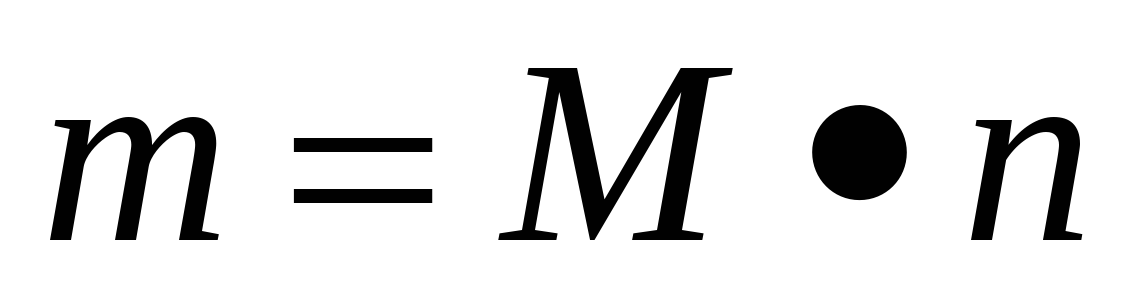 ; б)
; б) 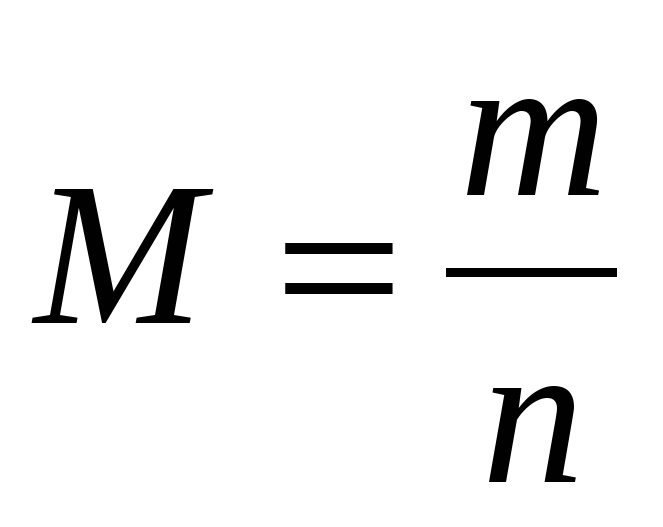 ; в)
; в) 
№3. Установите соответствие.
ВЕЛИЧИНЫ
Молярный объем
Объем газа
Объем кмоль газа
Постоянная Авогадро
Количество вещества
РАЗМЕРНОСТЬ ВЕЛИЧИН
а) м3
б) моль
в) м3/кмоль
г) л
д) л/моль
е) молекул/моль
ж) ммоль
з) мл
№4. Какой объем (н.у.) занимают 12 · 1023 молекул озона?
а) 48 л; б) 44,8 л; в) 11,2 л.
№5. Рассчитайте массу 0,25 моль карбоната кальция СаСО3.
«Простые вещества».
26 вариант
№1. Какой объем займут 12 · 1023 молекул водорода?
а) 44,8 мл; б) 44,8 л; в) 44,8 м3.
№2. Формула для расчета количества вещества, если известна его масса:
а)  ; б)
; б)  ; в)
; в) 
№3. Установите соответствие.
КОЛИЧЕСТВЕННЫЕ ХАРАКТЕРИСТИКИ ВЕЩЕСТВА
Объем
Количество вещества
Число структурных частиц
Масса вещества
ФОРМУЛЫ ДЛЯ РАСЧЕТА
а) 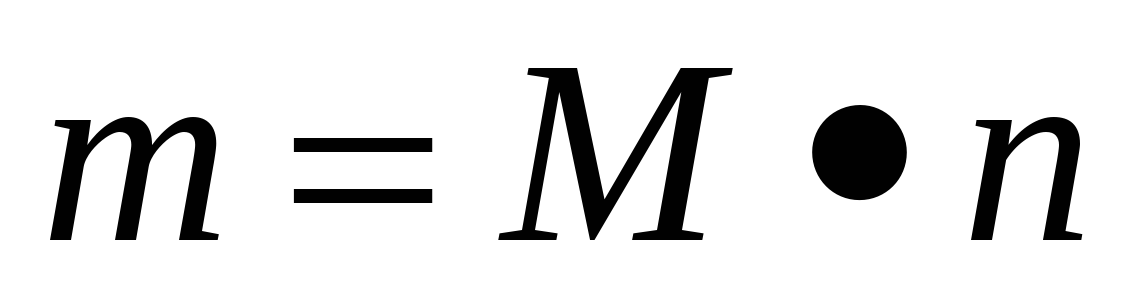
б) 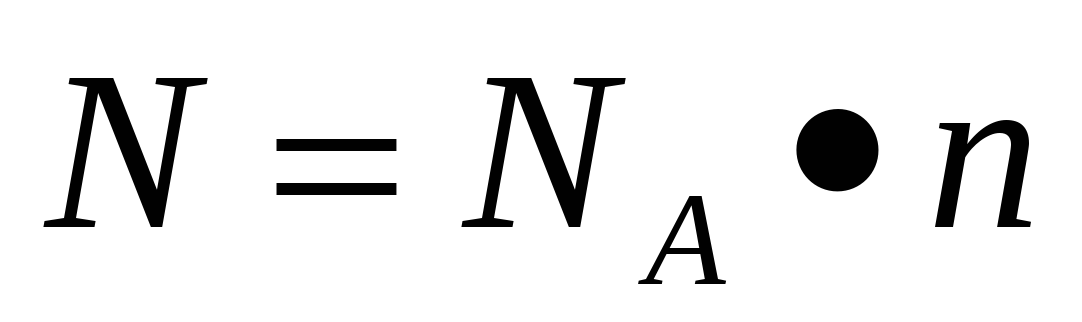
в)
г) 
д) 
е) 
№4. Какой объем (н. у.) занимают 3 · 1023 молекул водорода?
а) 22,4 л; б) 44,8 л; в) 11,2 л.
№5. Рассчитайте массу 0,25 моль железа.
«Простые вещества».
27 вариант
№1. Какой объем займут 12 · 1026 молекул водорода?
а) 44,8 мл; б) 44,8 л; в) 44,8 м3.
№2. Формула для расчета количества вещества, если известно число структурных частиц:
а)  ; б)
; б)  ; в)
; в) 
№3. Установите соответствие между левой и правой частями уравнений.
M = …
m = …
N = …
n = …
а) … = 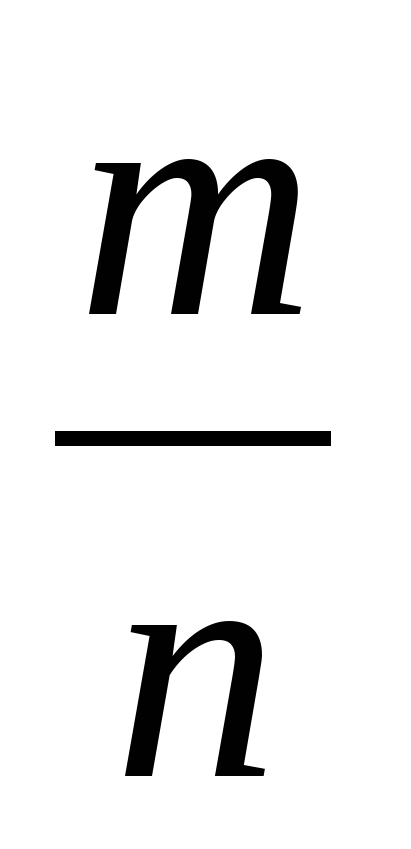
б) … = 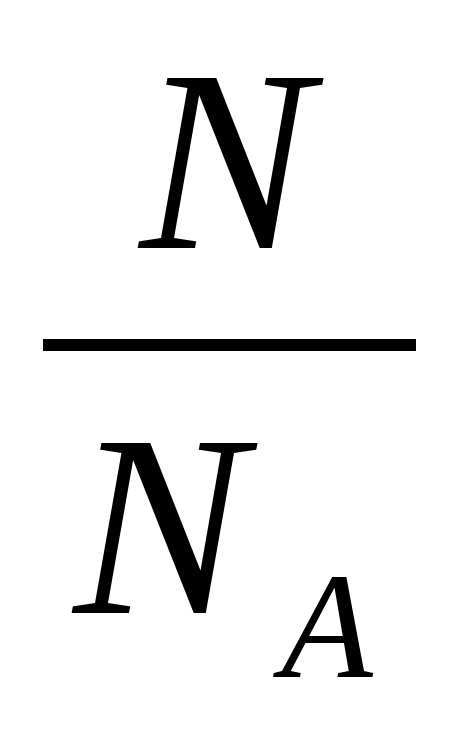
в) … = 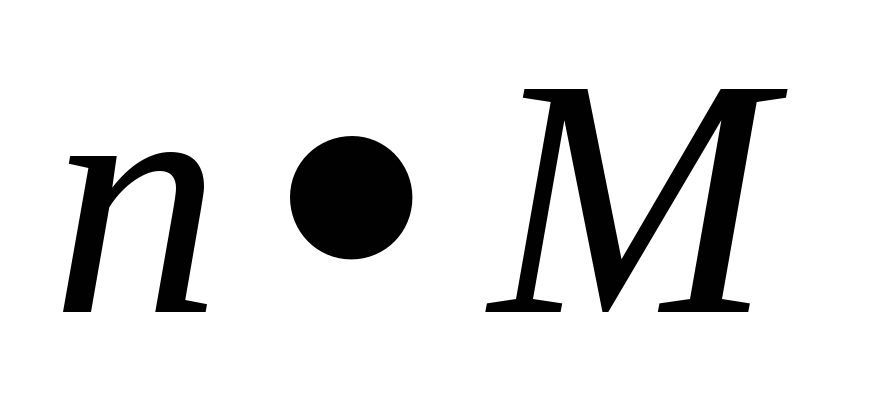
г) … =
д) … = NA n
n
№4. Какова масса 33,6л углекислого газа СО2?
а) 66 г; б) 33,6 г; в) 66,3 г.
№5. Какой объем (н.у.) занимают 12 · 1023 молекул озона О3?
«Простые вещества».
28 вариант
№1. Какова молярная масса кислорода?
а) 32 г/моль; б) 32 кг/кмоль; в) 32 мг/ммоль.
№2. Формула для расчета количества вещества, если известен его объем:
а)  ; б)
; б)  ; в)
; в) 
№3. Установите соответствие.
ВЕЛИЧИНЫ
Молярный объем газа (н.у.)
Количество вещества
Постоянная Авогадро
Молярная масса
УСЛОВНЫЕ ОБОЗНАЧЕНИЯ ВЕЛИЧИН
а) M
б) m
в) n
г) N
д) NA
е) V
ж) Vm
№4. Какой объем (н.у.) займут 18 · 1023 молекул сероводорода H2S?
а) 22,4 л; б) 66,7 л; в) 81,2 л.
№5. Какова масса 33,6л углекислого газа СО2?
«Простые вещества».
29 вариант
№1. Какова киломолярная масса кислорода?
а) 32 г/моль; б) 32 кг/кмоль; в) 32 мг/ммоль.
№2. Формула для расчета молярной массы вещества, если известна его масса:
а) 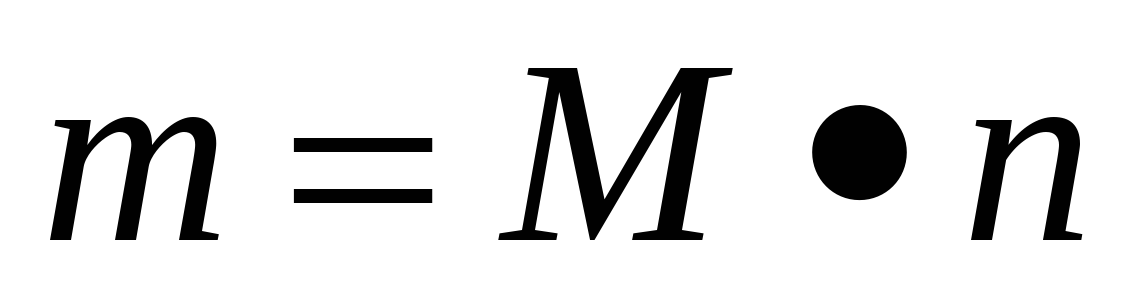 ; б)
; б) 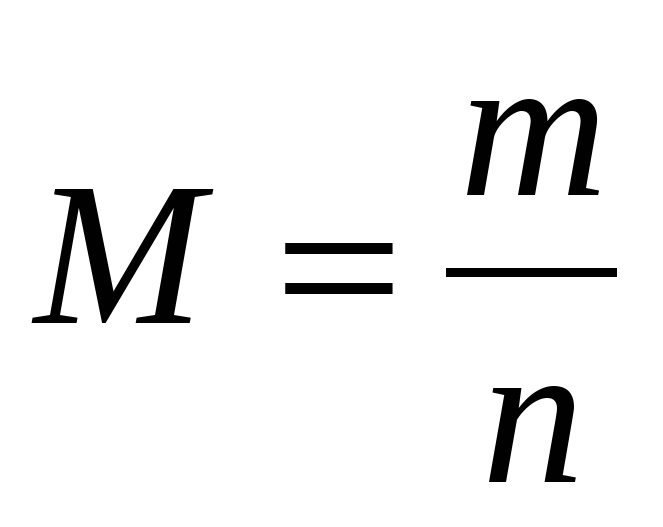 ; в)
; в) 
№3. Установите соответствие.
КОЛИЧЕСТВЕННЫЕ ХАРАКТЕРИСТИКИ ВЕЩЕСТВА
Объем
Количество вещества
Число структурных частиц
Масса вещества
ФОРМУЛЫ ДЛЯ РАСЧЕТА
а) 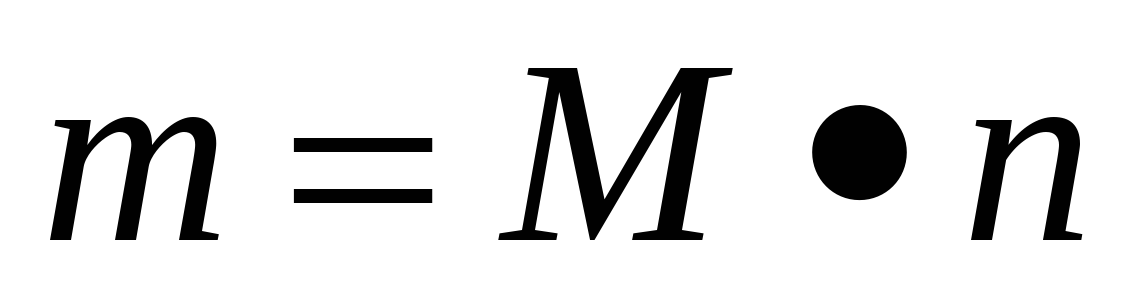
б) 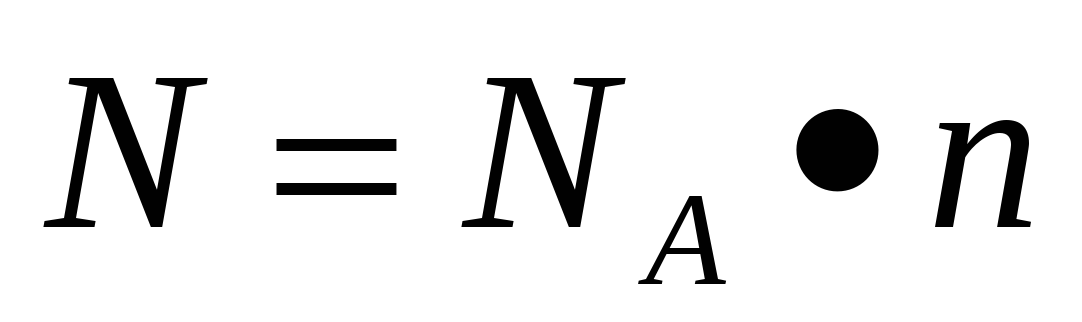
в)
г) 
д) 
е) 
№4. Какой объем займут 640 г кислорода О2 при н.у.?
а) 4,48 л; б) 44,8 л; в) 448 л.
№5. Сколько молекул будет содержать 1,5моль углекислого газа СО2?
«Простые вещества».
30 вариант
№1. Какова миллимолярная масса кислорода?
а) 32 г/моль; б) 32 кг/кмоль; в) 32 мг/ммоль.
№2. Формула для расчета объема вещества, если известно его количество вещества:
а) ; б)  ; в)
; в)
№3. Установите соответствие.
ВЕЛИЧИНЫ
Количество вещества
Молярный объем
Постоянная Авогадро
Объем газа
Объем кмоль газа
РАЗМЕРНОСТЬ ВЕЛИЧИН
а) м3
б) моль
в) м3/кмоль
г) л/моль
д) л
е) молекул/моль
ж) мл
з) ммоль
№4. Какой объем займут при н.у. 70 г оксида углерода (II) СО?
а) 56 л; б) 70 л; в) 44 л.
№5. Какое количество вещества составляет 49 г серной кислоты Н2SО4?

























