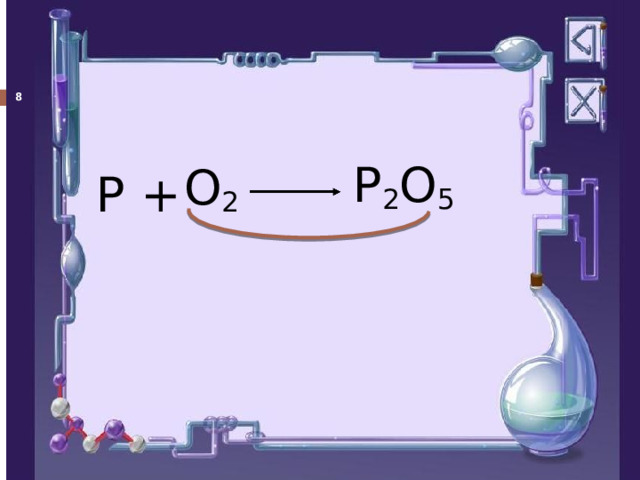Просмотр содержимого документа
«Уравнения химических реакций»

тема урока: «УРАВНЕНИЯ ХИМИЧЕСКИХ РЕАКЦИЙ»

Можно ли химические реакции изобразить на доске (в тетради)?
Если МОЖНО, то КАК???


Закон сохранения массы веществ:
Масса веществ, вступивших в реакцию равна массе веществ, получившихся в результате её.

При демонстрации презентации демонстрируется опыт «Горение фосфора в кислороде», или в презентацию вставить видео фрагмент «Горение фосфора в кислороде», данный видео фрагмент можно найти по ссылке http://school-collection.edu.ru/catalog/res/f83beda5-449d-d3dc-442c-a474a89eeca6/?
составления уравнения химической реакции
(на примере
взаимодействия фосфора и кислорода).

ЗАПОМНИТЬ : Формулы простых газообразных веществ состоят из двух атомов:
Н 2 , О 2 , N 2 , C l 2 , Br 2 и т.д.
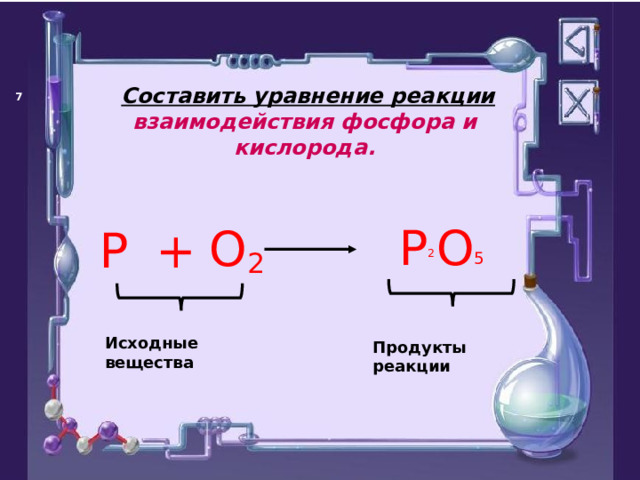
Составить уравнение реакции взаимодействия фосфора и кислорода.
P O
P
O 2
+
5
2
Исходные вещества
Продукты реакции
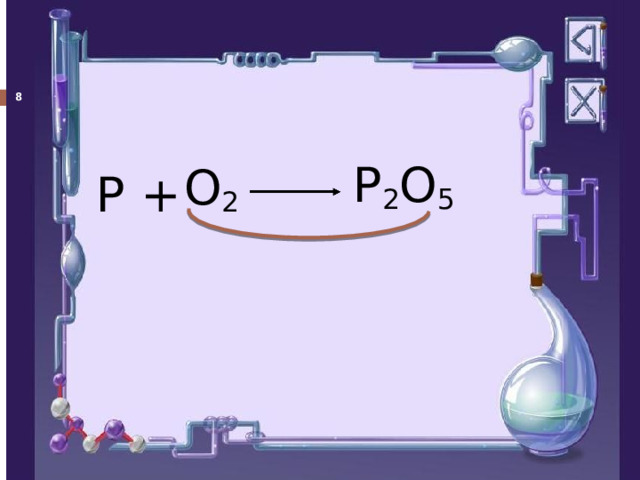
P 2 O 5
O 2
P
+
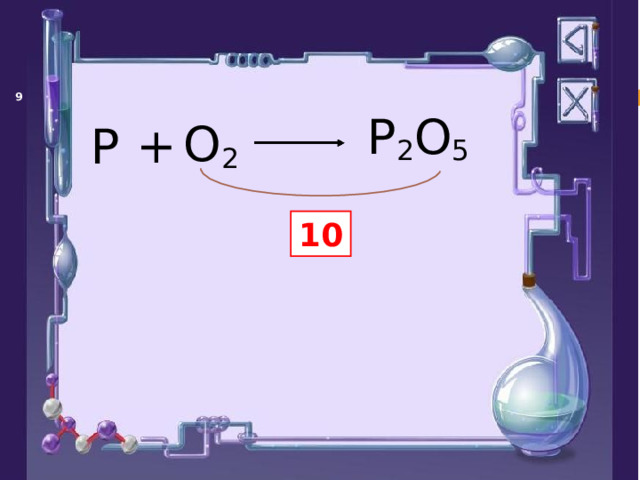
P 2 O 5
O 2
+
P
10
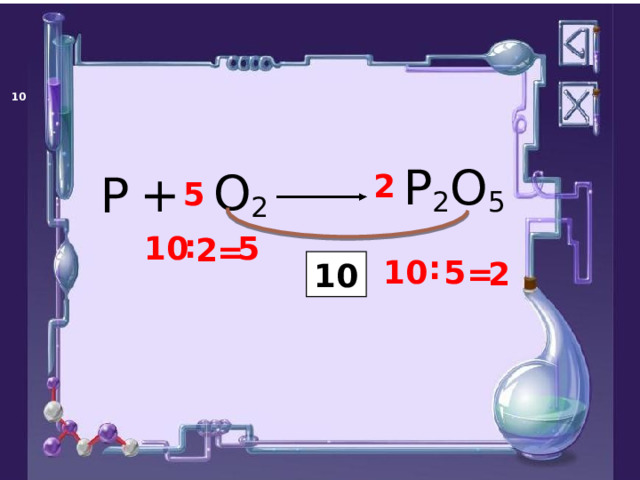
P 2 O 5
O 2
+
P
2
5
:
5
10
2
=
:
5
10
2
=
10
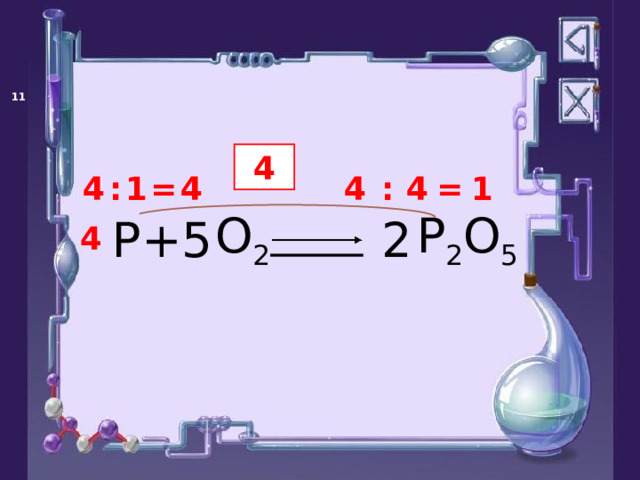
4
4
1
4
=
1
:
4
=
:
4
P
P 2 O 5
O 2
+
2
5
4

Уравнение реакции взаимодействия фосфора и кислорода.
P
O 2
P 2 O 5
+
2
5
4

Алгоритм

Составить уравнение реакции взаимодействия алюминия и кислорода.
3
2
2
Al
Al O
4
3
+
O 2
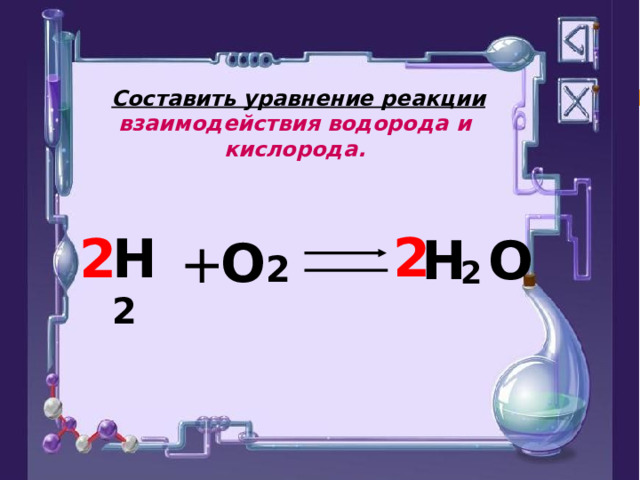
Составить уравнение реакции взаимодействия водорода и кислорода.
2
H O
2
H 2
2
O 2
+
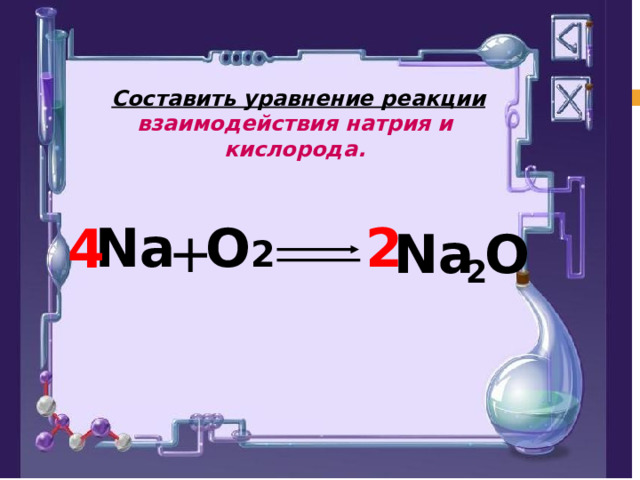
Составить уравнение реакции взаимодействия натрия и кислорода.
2
2
Na
O 2
Na O
4
+

ПРОВЕРКА
1 . Na 2 S
1. Сульфид натрия
2 . FeCl 3
2. Хлорид железа (III)
3 . CaCl 2
3. Хлорид кальция
4. Сульфид алюминия
5. Сульфид бария
6. Хлорид марганца (III)
7. Сульфид серебра (I)
8. Сульфид железа (III)
9. Хлорид цинка
10. Хлорид алюминия

Выполнить упр 3 стр 67 (самостоятельно)

Домашнее задание
прочитать § 20
Уметь составлять формулы бинарных соединений:
оксидов,
хлоридов;
сульфидов.