Конспект урока составила Цыплёнкова Ольга Валентиновна,
учитель химии МОУ СОШ №59, г. Ярославля
ЗАКОН СОХРАНЕНИЯ МАССЫ ВЕЩЕСТВ.
УРАВНЕНИЯ ХИМИЧЕСКИХ РЕАКЦИЙ.
Цель урока:
Сформировать понятие о химических уравнениях как об условной записи химической реакции с помощью химических формул. Начать формировать умение составлять уравнения химических реакций.
Задачи урока:
Образовательные
1. Опытным путём доказать и сформулировать закон сохранения массы веществ.
2. Дать понятие о химическом уравнении как об условной записи химической реакции с помощью химических формул.
3. Начать формирование навыков составления химических уравнений.
Тип урока: Комбинированный урок
Используемые учебники и учебные пособия:
-Габриелян О.С. Химия. 8 класс. М., Дрофа, 2008
Используемое оборудование:
компьютер, проектор, ИД, весы с разновесами, химические стаканы.
Используемые реактивы:
растворы сульфата меди (II) и щелочь
Используемые ЦОР:
Закон сохранения массы веществ (N 124972) (иллюстрация портрета М.В. Ломоносова, А. Лавуазье)
http://school-collection.edu.ru/catalog/res/617fb4b0-8cff-11db-b606-0800200c9a66/?from=d05469af-69bd-11db-bd13-0800200c9c08&interface=catalog&class=50&subject=31
Исходные вещества и продукты реакции (N 124975)
http://school-collection.edu.ru/catalog/res/617fb4b3-8cff-11db-b606-0800200c9a66/?from=d05469af-69bd-11db-bd13-0800200c9c08&interface=catalog&class=50&subject=31
Опыты, подтверждающие закон сохранения массы веществ (N 124973)
http://school-collection.edu.ru/catalog/res/617fb4b1-8cff-11db-b606-0800200c9a66/?from=d05469af-69bd-11db-bd13-0800200c9c08&interface=catalog&class=50&subject=31
Правила подбора коэффициентов в уравнениях химических реакций (N 124977)
http://school-collection.edu.ru/catalog/res/617fb4b5-8cff-11db-b606-0800200c9a66/?from=d05469af-69bd-11db-bd13-0800200c9c08&interface=catalog&class=50&subject=31
Составление химического уравнения (на примере взаимодействия водорода с кислородом) (N 124974) http://school-collection.edu.ru/catalog/res/617fb4b2-8cff-11db-b606-0800200c9a66/?from=d05469af-69bd-11db-bd13-0800200c9c08&interface=catalog&class=50&subject=31
Химические уравнения (N 124976)
http://school-collection.edu.ru/catalog/res/617fb4b4-8cff-11db-b606-0800200c9a66/?from=d05469af-69bd-11db-bd13-0800200c9c08&interface=catalog&class=50&subject=31
Закон сохранения массы (N 207293). (Закон сохранения массы веществ при химических реакциях с т.з. атомно-молекулярного учения) (видео-анимация)
http://school-collection.edu.ru/catalog/res/968c14a0-d78c-4199-a03c-a452575ed3b2/?from=c7fbc906-a8f3-4833-8f91-6d49e3ffabb0&interface=pupil&class=50&subject=31
ХОД УРОКА
Организационный этап.
Постановка цели. Сообщение темы и цели урока.
Сегодня на уроке мы приступаем к изучению новой темы «Изменения, происходящие с веществами».
Нам предстоит вспомнить, какие изменения могут происходить с веществами, по каким признакам они отличаются друг от друга.
Нам предстоит доказать и сформулировать один из важнейших законов природы, а также опираясь на этот закон продолжить изучение химического языка.
Повторение изученного материала
Вопросы для повторения:
1. Какие изменения (явления) могут происходить с веществами? (физические и химические)
2. Работа с ИД:
«Определите физические и химические явления, поместите выражения в соответствующие колонки таблицы»


3. По каким признакам можно отличаются физические явления от химических?
| При физических явления изменяется | При химических явлениях изменяется |
| - агрегатное состояние, - форма или размеры | - запах -цвет -выделяется или поглощается тепло и свет -образуется или исчезает осадок, -выделяется газ |
| -новые вещества не образуются | -новые вещества образуются |
Изучение нового материала
Главное отличие химических реакций от физических процессов – это образование новых веществ, свойства которых отличаются от свойств исходных.
Поэтому тема урока сегодня - «Химические реакции» (запись в тетради)
Закон сохранения массы веществ.
| Проблемный вопрос: | Решение проблемы |
| -Изменится ли масса реагирующих веществ по сравнению с массой продуктов реакции? -Можно ли проверить экспериментально, и каким образом? |
Для эксперимента необходимы весы и реагирующие вещества |
|
| Демонстрационный эксперимент (выполняет ученик под руководством учителя) - помещает на одной чаше весов два стаканчика с р-рами CuSO4 и KOH, на другой - гири для уравновешивания - смешивает растворы в один стаканчик, другой ставит рядом, - ребята отмечают, что равновесие весов не нарушилось, хотя реакция прошла, о чём свидетельствует выпадение синего осадка; |
| Какой вывод о проделанном эксперименте можно сделать? Меняется ли масса реагирующих веществ? | Формулируют закон сохранения массы: масса веществ, вступивших в реакцию, равна массе образовавшихся веществ |
В первые, этот закон (закон сохранения массы веществ) был теоретически сформулирован в 1748 году и экспериментально подтверждён в 1756 году русским ученым М.В. Ломоносовым.
Французский учёный Антуан Лавуазье в 1789 году окончательно убедил учёный мир в универсальности этого закона.
Как Ломоносов, так и Лавуазье пользовались в своих экспериментах очень точными весами. Они нагревали металлы (свинец, олово, и ртуть) в запаянных сосудах и взвешивали исходные вещества и продукты реакции.
(учащиеся записывают формулировку в тетрадь).
М.В. Ломоносов, 1748 год – «Закон сохранения массы веществ»
масса веществ, вступивших в реакцию, равна массе образовавшихся веществ

| Проблемный вопрос | Решение проблемы |
| Что происходит в ходе химической реакции?
| Использование ЦОР: Видео-анимация «Закон сохранения массы веществ с точки зрения атомно-молекулярного учения». 
|
Опираясь на закон сохранения массы веществ и атомно-молекулярное учение любой химический процесс можно представить на бумаге условной записью, используя формулы веществ и математические знаки, при этом надо учитывать, что число атомов вступивших в реакцию равно числу атомов образовавшихся. А значит, данную запись можно называть уравнением – уравнением химической реакции.
Химические уравнения.
| Проблемный вопрос | Решение проблемы |
| Как составить уравнение химической реакции? | Использование ЦОР: Составление химического уравнения (на примере взаимодействия водорода с кислородом) (флеш-анимация)  |
Записи в тетради
Химическое уравнение – это условная запись химической реакции посредством химических формул и математических знаков
Исходные вещества, принимающие участие в химических реакциях называются реагентами.
Новые вещества, образующиеся в результате химической реакции называются продуктами.
Примеры
2Н2+О2 = 2Н2О
4Р +5О2 = 2Р2О5
Тренировочные задания на составление уравнений химических реакций.
Используя правила составления уравнений, напишите уравнения следующих химических реакций
Задание 1. Работа с ИД


Алгоритм расстановки коэффициентов в уравнении химической реакции.
1. Подсчитать количество атомов каждого элемента в правой и левой части.
2. Определить, у какого элемента количество атомов меняется, найти Н.О.К.
3. Разделить Н.О.К. на индексы – получить коэффициенты. Поставить
коэффициенты перед формулами.
4. Пересчитать количество атомов, при необходимости действия повторить.
5. Начинать лучше с атомов О или любого другого неметалла (если только О не
находится в составе нескольких веществ).
Работа самостоятельная (или в парах) по карточкам, с последующей проверкой на ИД
Задание 4. Закончите уравнения реакций:
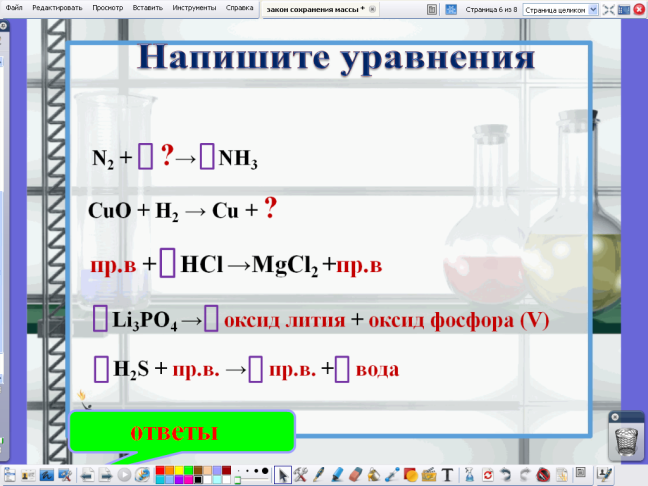

Закрепление
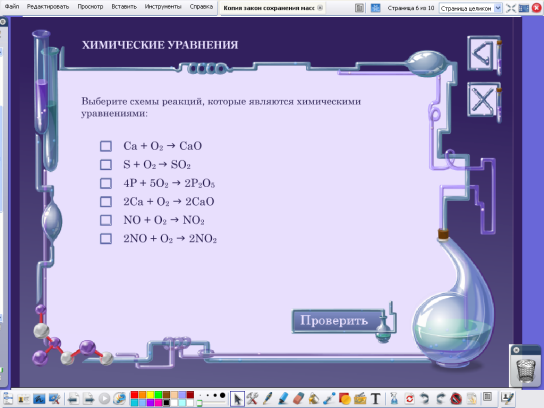
Задание 1.Использование ЦОР: Выберите схемы реакций которые являются химическими уравнениями
(флеш-анимация)
 1
1 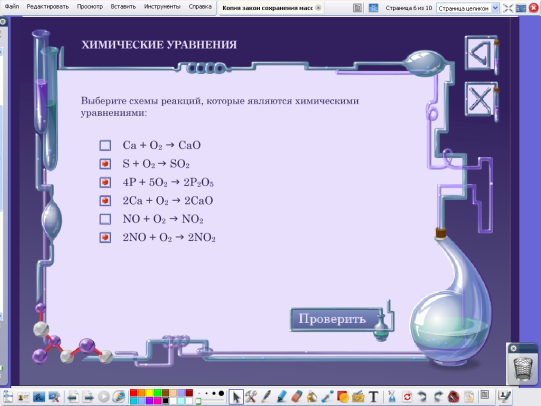 2
2
 3
3  4
4
Слайд исходный,
Слайд после выполнения задания учащимися,
Флеш-проверка,
Флеш-проверка,
Задание 2.Использование ЦОР: Расставьте коэффициенты в уравнениях реакций
(флеш-анимация)
 1.
1.  2.
2. 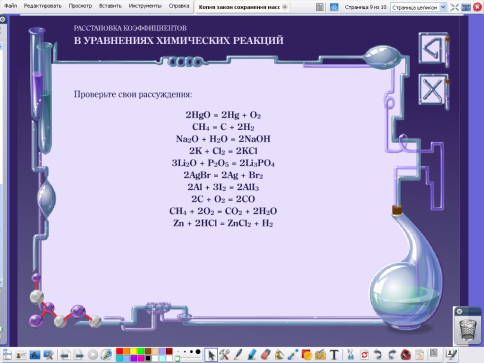 3
3
VI. Домашнее задание. § 27 (до типов реакций);
VII. Итог урока. Учащиеся формулируют выводы по уроку.
| Вариант 1 | Вариант 2 |
  N2+ ? → NH3 CuO + H2 → Сu + ?   Al(OH)3 → оксид алюминия + вода   пр.в. + HCl → MgCl2 + пр.в.   AgBr → Ag + Br2
|      ? + Cl2→ K Cl  Zn + H2O → ? + H2 Li3PO4 → оксид лития + оксид фосфора (V)    H2S + пр.в. → пр.в. + H2O C + O2 → CO
|
















 1
1  2
2  3
3  4
4  1.
1.  2.
2.  3
3










