| 1 | 2 | 3 | 5 | 6 | 7 |
| 1 | Организационный момент. | http://www.terikapress.ru/html/h010.html
| Демонстрация отрывка из книги | Внешняя и внутренняя (психологической ) готовность учащихся у к уроку. | 1мин |
| 2 | Проверка домашнего задания. | Презентация 1-4 слйды | Содержание этапа. Выяснить степень усвоения заданного на дом материала; определить типичные недостатки в знаниях и их причины; ликвидировать обнаруженные недочёты | Учащиеся на листочке записывают верные ответы, взаимопроверка. | 4 мин. |
| 3. | Постановка цели занятия перед учащимися.
| Презентация 5-8 слйды | Первичное введение материала с учетом закономерностей процесса познания при высокой мыслительной активности уч-ся. 31 января 1951 г. обрушился железнодорожный мост в Квебеке (Канада), введенный в эксплуатацию в 1947 г. в 1964 г. рухнуло одно из самых высотных сооружений в мире – 400-метровая антенная мачта в Гренландии.
У металлов есть и враг, который приводит к огромным безвозвратным потерям металлов, ежегодно полностью разрушается около 10% производимого железа. По данным Института физической химии РАН, каждая шестая домна в России работает впустую – весь выплавляемый металл превращается в ржавчину. | Воспринимают информацию презентации и отвечают на вопрос, используя материал учебника стр. 265, формулируют цель урока, которая фиксируется на доске | 4 мин |
| 4. | Организация усвоения способов деятельности путем воспроизведения информации и упражнений в ее применении (в том числе смена вариантов) по образцу. | http://slovari.yandex.ru/%D1%87%D1%82%D0%BE%20%D1%82%D0%B0%D0%BA%D0%BE%D0%B5%20%D0%BA%D0%BE%D1%80%D1%80%D0%BE%D0%B7%D0%B8%D1%8F/%D0%91%D0%A1%D0%AD/%D0%9A%D0%BE%D1%80%D1%80%D0%BE%D0%B7%D0%B8%D1%8F%20%D0%BC%D0%B5%D1%82%D0%B0%D0%BB%D0%BB%D0%BE%D0%B2/ | Учитель организует групповую работу учащихся | Учащиеся работая в группах, находят ответы на вопросы в учебнике «Химия 9» автор Кузнецова Н.Е. стр 260-263 или использование Интернет -ресурса
Коррозия включает физические и химические процессы? Слова «коррозия» и «ржавление» — это синонимы? Коррозия присуща только металлам? Какие факторы могут вызвать коррозию? Пояснить суть опыта http://files.school-collection.edu.ru/dlrstore/0ab9b4c5-4185-11db-b0de-0800200c9a66/x9_078.swf
| 10 мин |
| 5. | Творческое применение и добывание знаний, освоение способов деятельности путем решения проблемных задач, построенных на основе ранее усвоенных знаний и умений.
|
| Организация работы в группах. Перед вами 5 пронумерованных стаканов. В 1-ом стакане железный гвоздь находится в воде. Во 2-ом стакане железный гвоздь в растворе хлорида натрия. В 3-ем стакане к железному гвоздю прикрепили медную проволоку и они находятся в растворе хлорида натрия. В 4-м стакане железный гвоздь находится в контакте с цинком, и они помещены в раствор хлорида натрия. В 5-ом стакане железный гвоздь находится в растворах хлорида и гидроксида натрия. Давайте сравним полученные результаты и объясним результаты эксперимента (демонстрация приготовленного за несколько дней опыта по коррозии). Проблема: Почему в одних случаях коррозия усиливается, а в других замедляется? Объясните процессы, происходящие в каждом стакане | Учащиеся работают в 5 группах. В стакане №1 – железо прокорродировало слабо, в чистой воде коррозия идет медленно. Мы наблюдаем химическую коррозию. В стакане №2 – идет химическая коррозия, но здесь скорость коррозии выше, чем в 1-ом стакане, следовательно, хлорид натрия – увеличивает скорость коррозии. В стакане №3– мы наблюдаем электрохимическую коррозию (железо находится в контакте с медью). Скорость коррозии высока, т.к. раствор хлорида натрия – сильный электролит. 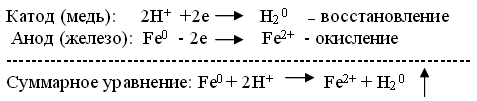 Суммарное уравнение: Fe0 + 2H+ →Fe2+ + H2 0 В стакане №4– также идет коррозия, но не железа, а цинка, т.к. железо менее активный металл является катодом, а цинк анодом: 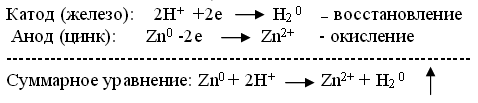 В стакане №5 – железо практически не подвергается коррозии, следовательно, гидроксид натрия – замедляет коррозию, гидроксид-ионы являются ингибиторами, т.е. замедляют коррозию. Вывод: Катионы водорода и растворенный в воде кислород – важнейшие окислители, вызывающие электрохимическую коррозию. Скорость коррозии тем больше, чем сильнее отличаются металлы по своей активности (т.е. чем дальше друг от друга они расположены в ряду напряжений металлов). В стакане №5 – железо практически не подвергается коррозии, следовательно, гидроксид натрия – замедляет коррозию, гидроксид-ионы являются ингибиторами, т.е. замедляют коррозию. Вывод: Катионы водорода и растворенный в воде кислород – важнейшие окислители, вызывающие электрохимическую коррозию. Скорость коррозии тем больше, чем сильнее отличаются металлы по своей активности (т.е. чем дальше друг от друга они расположены в ряду напряжений металлов).
| 7 мин |
| 6. | Обобщение изучаемого на уроке и введение его с систему ранее усвоенных знаний и умений. | http://files.school-collection.edu.ru/dlrstore/0ab9b4c6-4185-11db-b0de-0800200c9a66/x9_079.swf
http://files.school-collection.edu.ru/dlrstore/942bacf8-98d3-bde6-7e09-5df731f7faed/00119986215143138.htm
| Организует индивидуальную работу учащихся | Учащиеся работают за ПК индивидуально, отвечая на вопрос «4-5» «Объяснить сущность коррозийного процесса» «3» оформить отчет об интерактивном опыте И ответить на интерактивный тест | 10 мин |
| 7. | Контроль за результатами учебной деятельности, осуществляемой учителем и учащимися, оценка знаний. |
| Учитель дает оценку деятельности учащихся на уроке согласно задачам урока. |
| 1 мин |
| 8. | Домашнее задание к следующему уроку. | Презентация 9 слайд | Пояснение к домашнему заданию |
| 2 мин |
| 9. | Рефлексия, подведение итогов урока
|
| Ключ — это ваши знания, полученные на уроке. | 
Учащиеся оценивают свою деятельность на уроке. | 1 мин. |







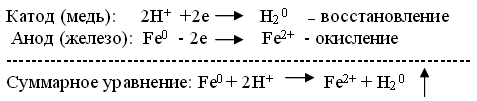
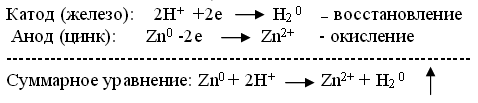 В стакане №5 – железо практически не подвергается коррозии, следовательно, гидроксид натрия – замедляет коррозию, гидроксид-ионы являются ингибиторами, т.е. замедляют коррозию. Вывод: Катионы водорода и растворенный в воде кислород – важнейшие окислители, вызывающие электрохимическую коррозию. Скорость коррозии тем больше, чем сильнее отличаются металлы по своей активности (т.е. чем дальше друг от друга они расположены в ряду напряжений металлов).
В стакане №5 – железо практически не подвергается коррозии, следовательно, гидроксид натрия – замедляет коррозию, гидроксид-ионы являются ингибиторами, т.е. замедляют коррозию. Вывод: Катионы водорода и растворенный в воде кислород – важнейшие окислители, вызывающие электрохимическую коррозию. Скорость коррозии тем больше, чем сильнее отличаются металлы по своей активности (т.е. чем дальше друг от друга они расположены в ряду напряжений металлов).



























