Сабақ жоспары / План урока
Пән / Предмет ХИМИЯ
Сынып/Класс ДЕВЯТЫЙ Сабақ / Урок № 54 Күні / Дата 06.04.2013 год
Тақырыбы / Тема: Ацетилен. Структурная формула. Получение ацетилена из метана и карбида кальция. Физические свойства. Горение ацетилена. Применение.
Сабақтың мақсаты / Цель урока: продолжить формирование знаний учащихся о непредельных углеводородах на примере ацетилена.
Білімділік / 0бразоватепъная:\ ознакомить с особенностями строения молекулы ацетилена, его свойствами, практическим значением.
Дамытушылық / Развивающая:_ умения сравнивать, анализировать, делать выводы; составлять таблицу сравнения углеводородов.
Тәрбиелік / Воспитательная: воспитывать ответственность, самостоятельность.
Көрнекілігі / Оборудование: доска, интерактивная доска, флипчарт, компьютер;
Пәнаралық байланыс Межпредметныe связи:
География.
Сабақ барысы / Ход урока:
1.Ұйымдастыру кезені
Организационный момент
Приветственное слово учителя. Организация учащихся.
2.Үй тапсырмасы тексеру
Проверка домашнего задания.
Задание 9 стр. 157.Вычислить объём и количество вещества этилена, полученного из 11,2 литров этана (у.н.)
Ответ: ν=0,5 моль, V=11,2 л.
3.Білімін тексеру
Проверка знаний:
Даны структурные формулы алканов:
А)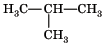 Б)
Б)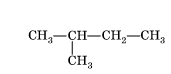 В)
В)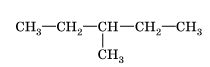
1.Дать данным алканам название.
А) 2-метилпропан Б) 2-метилбутан В) 3-метилпентан
2.Составить по данным формула структурные формулы алкенов, дать им названия.
А)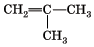 Б)
Б) 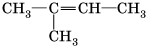 В)
В) 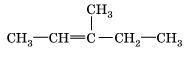
2-метилпропен-1 2-метилбутен-2 3-метилпентен-2
4.Жана тақырыптың мазмұны
Изложение нового материал:
УЧИТЕЛЬ:
Среди непредельных углеводородов есть углеводороды с общей формулой CnH2n-2, в молекуле которых есть одна тройная связь.
Составьте структурные формулы углеводородов с тройной связью ,в молекулах которых 2, 4 и 5 атомов углерода.
НС≡СН, НС≡С-СН2-СН3, НС≡С-СН2-СН2-СН3
Данные углеводороды относятся к непредельным углеводородам, которые называют алкинами.
Дайте названия углеводородам, формулы которых вы написали. Какие углеводороды получаться, если тройная связь будет находиться у второго атома углерода. Запишите их формулы и назовите их.
Н3С-С≡С-СН бутин-2, Н3С-С≡С-СН2-СН3 пентин-2.
Простейший представитель алкинов- ацетилен.
Ацетилен в промышленности получают путём нагревания метана
2СН4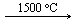 С2Н2↑+3Н2↑.
С2Н2↑+3Н2↑.
Также ацетилен можно получить при взаимодействии карбида кальция с водой:
СаС2+2Н2О→Са(ОН)2+ С2Н2↑
Где применяется ацетилен, полученный данным способом?
-При сварке и резке металлов кислородо-ацетиленовым сварочным аппаратом, так как при горение ацетилена выделяется большое количество теплоты.
Физические свойства.
Ацетилен- газ без цвета. Почти без запаха, горючий.
Химические свойства.
УЧИТЕЛЬ: зная строение молекулы ацетилена, предположите, какими химическими свойствами будет обладать ацетилен?
-Так как в молекуле ацетилена есть тройная связь, он имеет непредельный характер, а значит будет вступать в реакцию присоединения, горения, полимеризации.
-Записать уравнения реакций:
Присоединения одной молекулы водорода, двух молекул водорода.Какие вещества образовались в результате реакций?
С2Н2+Н2→С2Н4
С2Н2+2Н2→С2Н6
Запишите уравнение реакции горения ацетилена.
2С2Н2+5О2 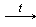 4СО2↑+2Н2О
4СО2↑+2Н2О
Сколько же энергии выделяется при сгорании ацетилена?
Решить задачу:
Составить термохимическое уравнение горения ацетилена, если при сжигании 5,6 литров ацетилена выделилось 325 кДж теплоты (у.н.)?

ДАНО: РЕШЕНИЕ:
V(С2Н2)=5,6 л 5,6л. 325кДж
Q=325 кДж 2С2Н2+5О2 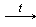 4СО2↑+2Н2О+ Q
4СО2↑+2Н2О+ Q
У.н. ν=2 моль
Н АЙТИ: 2∙22,4л х
АЙТИ: 2∙22,4л х
Q-? 5,6∙х=44,8∙325
х=2600 (кДж)
Ответ: 2С2Н2+5О2 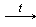 4СО2↑+2Н2О+2600кДж
4СО2↑+2Н2О+2600кДж
Применение ацетилена и его производных.
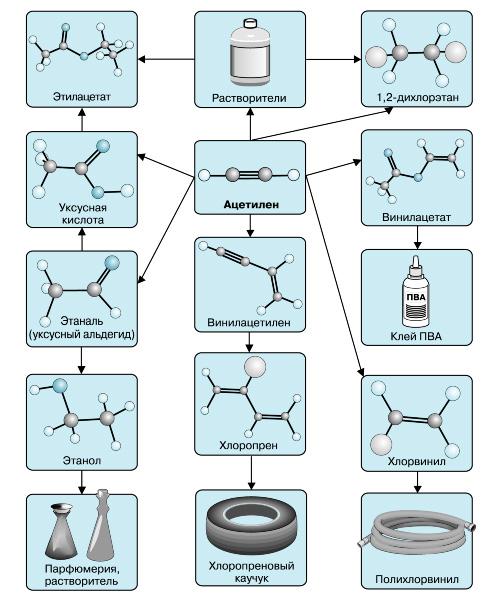
5.Өгілген тықырыпты бекіту
Первичное закрепление изученного материала:
Выполнить задание 6 стр. 159
СаС2→ С2Н2→ СО2→СаСО3
1. СаС2+2Н2О→Са(ОН)2+ С2Н2↑
2. 2С2Н2+5О2 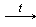 4СО2↑+2Н2О
4СО2↑+2Н2О
3. СО2+СаО→ СаСО3
Итог урока:
Закончить предложения:
1.Сегодня на уроке я узнал…
2.Я научился…
3.Теперь я знаю…
4.Сегодня урок мне…
|6. Үйге тапсырма беру
Задание на дом:
§ 49. Составить таблицу «Сравнение алакнов, алкенов, алкинов»





 В)
В)


 АЙТИ: 2∙22,4л х
АЙТИ: 2∙22,4л х










