СМК 08 ПД 01
Приложение 12
ГККП «Уральский политехнический колледж» УОАЗКО
(наименование организации образования)
План учебного занятия
(практического обучения)
| № | Группа | Дата | Заместитель директора по учебной работе |
|
|
|
|
|
|
|
|
|
|
| Предмет | физика |
| Группа | 25 |
| Учитель | Казмагамбетова Катима Гайисовна |
| Тема | Изопроцессы в газах. Газовые законы. |
| Тип урока | урок изучения и первичного закрепления новых знаний |
| Цели урока | формирование понятия изопроцессы формирование понятия газовые законы формирование умений выделять и описывать изопроцессы,доказывать их справедливость экспериментом; активизация познавательной деятельности учащихся. |
| Критерии оценивания | Учащиеся могут: - выводить газовые.законы - понимать, читать и строить графики изопроцессов |
| Языковые цели | макроскопиялық, қысым, көлем, температура, сызықтық тәуелділігі, кеңейту, қысу, қыздыру, салқындату, артады, кемиді, тура пропорционалды, кері пропорционалды макроскопический, давление, объем, температура, линейная зависимость, расширение, сжатие, нагревание, охлаждение, возрастает, убывает, прямо пропорционально, обратно пропорционально macroscopic, pressure, volume, temperature, linear dependence, expansion, compression, heating, cooling, increases, decreases, directly proportional, inversely proportional |
| Привитие ценностей | привитие любви к учебе через любознательность, творчество и критичность к изучаемому материалу, постоянное развитие ума |
| контроля учебной деятельности | по назначению: текущий; по содержанию: по теории; по уровню проверки: репродукция знаний, действия в новой ситуации; по продолжительности: кратковременный; по способу участия учеников: индивидуальный, групповой; - по виду ответа: устный, письменный. |
| Межпредметные связи | Математика (построение графиков: прямая, гипербола), химия (уравнение Менделеева-Клапейрона, законы Бойля-Мариотта, Гей-Люссака, Шарля), казахский, русский и английский языки (терминология), информатика (моделирование). |
| Навыки использования ИКТ | ПК с установленной ОС Windows и пакетом MicrosoftOffice; мультимедийный проектор; интерактивная доска или экран; презентация MicrosoftPowerPoint; Дидактический материал: карточки с заданиями. |
| Предварительные знания | Идеальный газ, молекулярно-кинетическая теория газов, уравнение состояния идеального газа (Менделеева-Клапейрона). |
| Этапы урока | Организационный момент 1мин Актуализация знаний 10 мин Изучение нового материала 20 мин Первичное закрепление 12 мин Подведение итогов урока. Информация о домашнем 2 мин задании |
Ход урока
Организационный момент.
Эмоциональный настрой на работу в рамках урока
Актуализация знаний
2.1. Фронтальный опрос. (Приложение 1)
Что является объектом изучения МКТ?
Какая физическая модель используется в МКТ газов, дайте характеристику этой модели?
Какие параметры в МКТ называются макроскопическими? Перечислите их.
. Какое уравнение устанавливает зависимость между макроскопическими параметрами?
В чѐм состоит смысл уравнения состояния идеального газа?
Какая форма уравнения состояния содержит больше информации: уравнение Клапейрона или уравнение Менделеева-Клапейрона?
Заполните пропуски в определениях. (Приложение 2) Самостоятельное выполнение задания.
Учащиеся получают карточку с определениями, в которых пропущены некоторые слова. В течение 3 минут требуется восстановить определения.
Идеальный газ – это ………… реального газа, в которой не учитывают ………. молекул и их взаимодействие ………………
Состояние идеального газа характеризуется ………………. параметрами состояния: давление,…………. и температура.
Уравнение, связывающее три макроскопических параметра …………….. называют
……………….
Приведите в соответствие вопросы и ответы. (Приложение 3)
Учащиеся получают карточку, где в левой части перечислены основные понятия, названия законов, а в правой – правильные ответы, расположенные беспорядочно. В течение 5 минут требуется записать правильный код ответа, например: 1-5; 2-6 и т.д.
| Вопросы | Ответы |
| 1 | Основное уравнение МКТ | 1 | 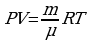 |
| 2 | Связь между давлением и средней кинетической энергией | 2 |  |
| 3 | Средняя кинетическая энергия теплового поступательного движения молекул | 3 |  |
| 4 | Уравнение состояния идеального газа | 4 |  |
| 5 | Зависимость давления газа от концентрации его молекул и температур | 5 |  |
| 6 | Уравнение Клапейрона | 6 |  |
Изучение нового материала
3.1. Ведение в тему урока
Учитель: Итак, мы отметили, что уравнение состояния идеального газа связывает между собой три макроскопических параметра: давление, объѐм и абсолютную температуру.
С помощью этого уравнения можно исследовать процессы, в которых масса газа и один из трех параметров – давление, объѐм или абсолютная температура – остаются неизменными.
Рассмотрим каждый из представленных процессов подробнее и установим для каждого из них связь между Т, р и V. Сегодня на уроке нам необходимо:
а) изучить процессы, в которых масса газа и один из трех параметров остаются неизменными;
б) выявить их особенности;
в) вывести формулы, описывающие эти процессы;
г) экспериментально подтвердить или опровергнуть эти законы, т.к. согласно А. Эйнштейну- «Истина – это то, что выдерживает проверку опытом»
И тема нашего сегодняшнего урока – «Изопроцессы в газах. Газовые законы»
Процессы, протекающие при неизменном значении одного из параметров называется изопроцессами.
Чтобы лучше запомнить названия изопроцессов, составим схему:

Количественные зависимости между двумя параметрами газа при фиксированном значении третьего называют газовыми законами.
Используя уравнение состояния идеального газа, можно вывести все три закона за 10 минут. Но в истории физики эти открытия были сделаны в обратном порядке: сначала экспериментально были получены газовые законы, и только потом они были обобщены в уравнение состояния. Этот путь занял почти 200 лет: первый газовый закон был получен в 1662 году Бойлем и Мариоттом, уравнение состояния – в 1834 году Клапейроном, а более общая форма уравнения – в 1874 году Д.И. Менделеевым.
3.2. Мотивация учебной деятельности. Демонстрация опытов
Проведѐм занимательный опыт, который приписывают французскому учѐному Рене Декарту.
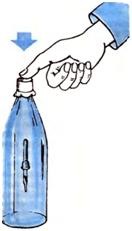 Демонстрация опыта “Картезианский водолаз”
Демонстрация опыта “Картезианский водолаз”
Оборудование: пластмассовая бутылка 1,5 л, заполненная водой с крышкой; медицинская пипетка, заполненная подкрашенной водой. Демонстрация: Бутылку наполнить водой, внутрь поместить пипетку. Iвариант: Закрыть плотно бутылку резиновой мембраной. Надавить на мембрану – пипетка погружается. Прекратить надавливание, пипетка всплывает.
II вариант: Закрыть плотно бутылку крышкой и взять в руки и сдавить еѐ – пипетка погружается, если убрать руки пипетка всплывает.
Создание проблемной ситуации:
Какие параметры газа меняются? (Р и V – изменяются)
Какой параметр остаѐтся постоянным? (Т - остаѐтся постоянной).
Итак: мы наблюдали процесс, протекающий при неизменном значении одного из параметров – температуры. Такой процесс называется изотермическим.
Демонстрация опыта “Шар в банке”
Оборудование: стеклянная банка на 2 л, воздушный шарик, горячая вода, пустой сосуд. Демонстрация: В пустую стеклянную банку налить горячей воды и подержать 1-2 мин, затем вылить ее в пустой сосуд. Банку накрыть надутым воздушным шариком и наблюдать, как шарик втягивается в банку. Создание проблемной ситуации:
Какие параметры газа меняются? (Т и V – изменяются)
Какой параметр остаѐтся постоянным? (Р - остаѐтся постоянной).
Итак: мы наблюдали процесс, протекающий при неизменном значении одного из параметров – давлении. Такой процесс называется изобарным.
Демонстрация опыта “Разрушение банки”
Оборудование: пластмассовая или металлическая банка с закручивающейся крышкой, очень горячая вода, сосуд с холодной водой.
Демонстрация: Налить горячую воду в банку подержать 2 мин. и вылить, быстро закрыв отверстие. Затем сразу облить ее холодной водой. Банку сплющит. Создание проблемной ситуации:
Какие параметры газа меняются? (Т и Р – изменяются)
Какой параметр остаѐтся постоянным? ( V остаѐтся постоянной).
Итак: мы наблюдали процесс, протекающий при неизменном значении одного из параметров – объѐма. Такой процесс называется изохорным.
3.3. Исследовательская работа
Чтобы объяснить эти опыты необходимо рассмотреть газовые законы.
Для групповой работы класс делится на три группы (три ряда). Работая с учебником, каждая группа изучает изопроцесс, по плану исследования:
Название процесса
Постоянный параметр
Определение
Формула закона, название закона
Формулировка закона
Графическое изображение процесса, название графика
Историческая справка
3.4. Презентация работы Рассмотрим три изопроцесса.
Каждая группа у доски представляет свой закон, заполняя таблицу и комментируя каждую позицию. Одна группа выступает, другие две группы записывают в тетрадь. (Приложение5)
| № п/п | Название процесса | Постоянный параметр | Определение | Формула закона | Формулировка | График |
| 1 | | | | | | |
| 2 | | | | | | |
| 3 | | | | | | |
I группа.
1) Изотермический процесс.
2) Т = const.
3) Процесс изменения состояния системы макроскопических тел (термодинамической системы) при постоянной температуре называют изотермическим («isos» - равный; «therme» - теплый). 4) pV = const при Т = const. Закон Бойля-Мариотта.
Для газа данной массы при постоянной температуре произведение давления газа на его объѐм постоянно.
Зависимость давления газа от объема при постоянной температуре графически изображают кривой, которую называют изотермой.

Историческая справка: этот закон экспериментально был открыт в 1662 г английским ученым Р.Бойлем и независимо от него несколько позже в 1676 г французским физиком Э. Мариоттом. Поэтому оно носит название закона Бойля – Мариотта.
Комментарий учителя: Этот изотермический процесс можно изобразить и в других координатных осях. Изобразим изотерму в координатах рТ и VТ.
 T
T 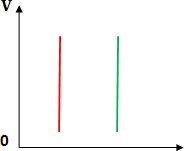 T
T
T2 T1 T2 T1
Закон Бойля-Мариотта начинает «работать на человека» (как, впрочем, и на любое млекопитающее) с момента его рождения, с первого самостоятельного вздоха.
При дыхании межреберные мышцы и диафрагма периодически изменяют объем грудной клетки. Когда грудная клетка расширяется, давление воздуха в легких падает ниже атмосферного, т.е. «срабатывает» изотермический закон (pV=const), и в следствие образовавшегося перепада давлений происходит вдох. Другими словами воздух идет из окружающей среды в легкие самотеком до тех пор, пока величины давления в легких и в окружающей среде не выровняются.
Выдох происходит аналогично: вследствие уменьшения объема легких давление воздуха в них становится больше, чем внешнее атмосферное, и за счет обратного перепада давлений он переходит наружу.
группа.
Изобарный процесс.
2) р = const.
Процесс изменения состояния термодинамической системы при постоянном давлении называют изобарным.
 = const при р = const. Закон Гей-Люссака.
= const при р = const. Закон Гей-Люссака.
Для газа данной массы при постоянном давлении отношение объѐма к абсолютной температуре постоянно.
Графическая зависимость объема от температуры изображается прямой линией – изобарой. При очень низких температурах закон Гей-Люссака не выполняется, поэтому сплошная линия на графике заменена пунктиром.
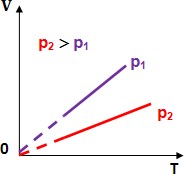
Историческая справка: этот закон был установлен экспериментально в 1802 г. французским физиком Ж. Гей-Люссаком и носит название закона Гей- Люссака.
Комментарий учителя: Изобразим изобару в координатах рТ и рV.

группа.
Изохорный процесс
V = const.
Процесс изменения состояния термодинамической системы при постоянном объѐме называют изохорным.
 = const при v = const. Закон Шарля.
= const при v = const. Закон Шарля.
Для газа данной массы отношение давления к абсолютной температуре постоянно, если объѐм не меняется.
Графическая зависимость давления от температуры изображается прямой линией – изохорой.

Историческая справка: этот газовый закон был установлен в 1787 г французским физиком Ж. Шарлем и носит название закона Шарля.
Комментарий учителя: Изобразим изохору в координатах VТ и рV.

Подведение итогов урока. Первичное закрепление.
4.1. Вспомним, что мы изучили на сегодняшнем уроке:
4.2. Решение задачи. Задача №2 стр 188.
В цилиндре под поршнем изобарический охлаждают газ объемом V1=10 л от температуры Т1=323 К до температуры Т2=273 К. Каков объем газа при температуре Т2?
4.3. Тестирование.
Информация о домашнем задании
(Д/З состоит из обязательного задания № 1 и двух дополнительных на выбор):
1. § 32 cтр 182-185.
*2. Экспериментальное задание:
Положите внутрь резинового шарика льдинку, а затем надуйте.
Ответе на вопросы:
Какие изменения произойдут с шариком через некоторое время?
Как изменяются при этом термодинамические параметры?
*3. Подготовить сообщение об ученых, чьи имена прозвучали на сегодняшнем уроке.
6. Рефлексия:
Было легко и интересно.
Было трудно, но интересно.
Было легко, но не интересно.
Приложение 1
Что является объектом изучения МКТ? (Идеальный газ.)
Какая физическая модель используется в МКТ газов, дайте характеристику этой модели? (Физическая модель - идеальный газ. Это газ, в котором размерами и взаимодействием между молекулами можно пренебречь.)
Какие параметры в МКТ называются макроскопическими? Перечислите их. (Величины, V, p, T, характеризующие состояние макроскопических тел без учета их молекулярного строения, называют макроскопическими параметрами)
Какое уравнение устанавливает зависимость между макроскопическими параметрами?
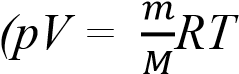 - уравнение Менделеева - Клапейрона).
- уравнение Менделеева - Клапейрона).
В чѐм состоит смысл уравнения состояния идеального газа? (Давление, объѐм и
температура меняются, но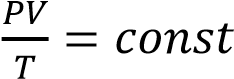 (не меняется значение дроби))
(не меняется значение дроби))
Какая форма уравнения состояния содержит больше информации: уравнение Клапейрона или уравнение Менделеева-Клапейрона?
(Содержит больше информации уравнение Менделеева-Клапейрона, потому что оно записывается для газа произвольной массы, а уравнение Клапейрона – для газа данной массы)
Приложение 2
Идеальный газ – это ………… реального газа, в которой не учитывают …………… молекул и их взаимодействие ……………….
Состояние идеального газа характеризуется ………………. параметрами состояния: давление, ……….. и абсолютная температура.
Уравнение, связывающее три макроскопических параметра …………. называют ………… .
Приложение 3 Приведите в соответствие вопросы и ответы
|
|
| Вопросы | Ответы | | 1 | Основное уравнение МКТ | 1 | 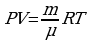 | | 2 | Связь между давлением и средней кинетической энергией | 2 |  | | 3 | Средняя кинетическая энергия теплового поступательного движения молекул | 3 |  | | 4 | Уравнение состояния идеального газа | 4 |  | | 5 | Зависимость давления газа от концентрации его молекул и температур. | 5 |  | | 6 | Уравнение Клапейрона | 6 |  |
|
| вопро сы | отве ты | | 1 | 5 | | 2 | 6 | | 3 | 2 | | 4 | 1 | | 5 | 3 | | 6 | 4 |
|
Приложение 5
| № п/п | Название процесса | Постоя нный параметр | Определение | Формула закона | Формулировка | График |
| 1 | Изотерми ческий | T = const | Процесс изменения состояния газа происходящ ий при постоянной температуре | pV = const Закон БойляМариотта | Для газа данной массы при постоянной температуре произведение давления газа на его объѐм постоянно |  Изотерма |
| 2 | Изобарный | P = const | Процесс изменения состояния газа при постоянном давлении |  = const = const Закон ГейЛюссака | Для газа данной массы при постоянном давлении отношение объѐма к абсолютной температуре постоянно |  Изобара |
| 3 | Изохорный | V =const | Процесс изменения состояния газа происходящ ий при постоянном объѐме |  = const. = const. Закон Шарля | Для газа данной массы отношение давления к абсолютной температуре постоянно, если объѐм не меняется |  Изохора |
Приложение 6
Бланк ответов
| Название задания |
|
|
|
|
|
|
|
|
| Фронтальный опрос |
|
|
|
|
|
|
|
|
| Заполните пропуски |
|
|
|
|
|
|
|
|
| Приведите в соответствие |
|
|
|
|
|
|
|
|
| Исследовательская работа |
|
|
|
|
|
|
|
|
| Решение задач |
|
|
|
|
|
|
|
|
| Тестирование |
|
|
|
|
|
|
|
|
Подводим итоги и выставляем оценки:
От 1 до 49 правильных ответов «2»
От 50 до 69- «3»
От 70 до 89 – «4»
От 90 до 100 – «5»






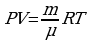






 Демонстрация опыта “Картезианский водолаз”
Демонстрация опыта “Картезианский водолаз” 
 T
T  T
T 














