| 3.Формирование мотивации | Рассказ, групповая работа, метод иллюстрации | Вызов уже имеющихся знаний по химическим веществам, активизация учащихся, мотивация для дальнейшей работы. Природные соединения кальция (мел, мрамор, известняк, гипс) и продукты их простейшей переработки (известь) были известны людям с древних времен. В 1808 г. английский химик Хэмфри Дэви подверг электролизу влажную гашеную известь (гидроксид кальция) с ртутным катодом и получил амальгаму кальция (сплав кальция с ртутью). Из этого сплава, отогнав ртуть Дэви получил чистый кальций.
Он же предложил название нового химического элемента, от латинского "сalx" обозначавшего название известняка, мела и других мягких камней. В ходе урока вы узнаете, почему кальций считают одним из важнейших элементов. Откройте, пожалуйста, методическое пособие № 1 и приступайте к выполнению работы в группах (по 4 человека). На работу отводится 3-4 минуты.
| Слушают учителя. Ученики «вспоминает», что им известно по изучаемому вопросу (делают предположения), систематизирует информацию до ее изучения | Прием «составление кластера» – составление списка известной информации по ключевым словам |
| 4.Актуализация опорных знаний | Беседа, групповая индивидуальная работа, метод иллюстрации | Составив «кластер», постараемся ответить на несколько вопросов, тем самым систематизируем наши знания по прошлой теме и подготовимся к изучению новой информации. В конце урока у вас будет возможность исправить ваш «кластер» или дополнить его. 1.Где в ПСХЭ находятся щелочноземельные металлы? Перечислите эти элементы. Правильно! 2.Почему элементам II группы, главной подгруппы дано такое название? Верно! 3. Кем в химических реакциях являются щелочноземельные металлы? Молодцы! 4.Какую валентность и степень окисления проявляют щелочноземельные металлы в соединениях? Верно, следующий вопрос будет посложнее! 5. Перечислите, с какими веществами взаимодействуют щелочноземельные металлы? Все правильно! | Слушают учителя и отвечают на вопросы, которые он задает 1.Все ЩМ находятся в 2 группе главной подгруппе Это бериллий(Be), магний (Mg), кальций (Ca), стронций (Sr),барий(Ba) и радий (Ra). 2. Происхождение этого названия связано с тем, что их гидроксиды являются щелочами, а оксиды по тугоплавкости сходны с оксидами алюминия и железа, носившими ранее общее название "земли" 3. Сильные восстановители 4.Валентность II, степень окисления +2. 5.Реагируют с водой при комнатной температуре (кроме Be) с выделением водорода. Обладают большим сродством к кислороду (восстановители). С водородом образуют солеобразные гидриды ЭH2. Оксиды имеют общую формулу ЭО. Тенденция к образованию пероксидов выражена слабее, чем для щелочных металлов.
| Использование ПС, учебник |
| 5.Усвоение новых знаний и умений | Беседа, самостоятельная, групповая работа учащихся, метод иллюстрации | Запишите в тетради дату нашего занятия и тему урока. Сегодняшняя работа будет идти по алгоритму (написано на доске): а) положение металла в ПСХЭ Д.И. Менделеева, строение его атома; б) физические и химические свойства металла – простого вещества, его получение; в) соединения: оксиды, гидроксиды, соли; г) применение металла и его соединений; д) биологическая роль металла. А) Найдите кальций в периодической системе химических элементов и дополните или заполните окошко методического пособия №1 «Положение в ПСХЭ». 1.Дайте характеристику элемента (Ca2+) по ПСХЭ Напишите электронное и электронно-графическое строение атома кальция. 2. Укажите, валентность и степень окисления, которые проявляет кальций в химических соединениях Б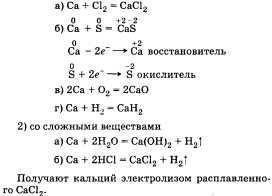 ) По физическим свойствам: кальций - металл серебристо-белого цвета, относительно легкий (плотность р = 1,54), температура плавления 854 °С, окисляется на воздухе. ) По физическим свойствам: кальций - металл серебристо-белого цвета, относительно легкий (плотность р = 1,54), температура плавления 854 °С, окисляется на воздухе. Получение: в промышленности Ca можно получить с помощью электролиза расплавленного хлорида кальция CaCl2. CaCl2 = Ca + Cl2 Переходя к характеристикам химических свойств кальция, следует отметить, что его высокая активность объясняется легкостью отдачи двух электронов, расположенных на внешнем электронном слое.
Таким образом, в химических реакциях кальций - восстановитель. Это можно подтвердить уравнениями реакций кальция, как с простыми, так и со сложными веществами:
Показываю опыт взаимодействия кальция с водой, комментируя происходящее.
В) Продолжим. Следующая станция «Соединения кальция». Кальций принадлежит к числу самых распространённых в природе элементов. В земной коре его содержится приблизительно 3% (масс.). Из-за своей химической активности в чистом виде кальций в природе не встречается, встречается только в виде соединений (солей). Оксид кальция (СаO) – негашеная или жженая известь – белое огнестойкое вещество, образованное кристаллами. Учитель сообщает о техническом названии СаО, о реакции «гашение извести» (стр. 99-100 в учебнике). Называется жженой известью из-за способа его получения – обжигание карбоната кальция. Обжиг производят в высоких шахтных печах. В печь закладывают слоями известняк и топливо, а затем разжигают снизу. При накаливании происходит разложение карбоната кальция с образованием оксида кальция: 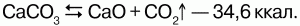
Получение: 1) при взаимодействии простых веществ: 2Ca + O2 = 2CaO; 2) при термическом разложении гидроксида и солей: 2Ca(NO3)2 = 2CaO + 4NO2 + O2. Химические свойства: 1) взаимодействует с водой: СаO + H2O = Са(OH)2; 2) реагирует с оксидами неметаллов: СаO + SO2 = CaSO3; 3) растворяется в кислотах, образуя соли: CaO + 2HCl = CaCl2 +H2O. Гидроксид кальция Ca(OH)2 (гашеная известь) является гидроксидом с типично основными свойствами и относится к щелочам. В лаборатории мы называем его известковой водой. На она воздухе мутнеет в результате поглощения углекислого газа, образуя карбонат кальция. Получение: 1) образуется при растворении кальция и оксида кальция вводе: CaO + H2O = Са(OH)2; 2) при взаимодействии солей кальция со щелочами: Ca(NO3)2 + 2NaOH = Ca(OH)2 + 2NaNO3. Химические свойства: 1) при нагревании до 580 °C разлагается: Са(OH)2 = СаO + H2O; 2) реагирует с кислотами: Ca(OH)2 + 2HCl = CaCl2 + 2H2O. При изучении химии в дальнейшем мы будем встречаться с соединениями кальция. В параграфе 15 описываются соли кальция, дома вы более подробно с ними познакомитесь. Г) Обратите внимание на слайд. Следующая станция «Применение Ca и его соединений». (Ca) Применение: благодаря большой химической активности кальций применяют для восстановления некоторых тугоплавких металлов (титан, цирконий, т.д.) из оксидов. Кальций также используют на производстве для отчистки стали и чугуна от кислорода, серы и фосфора, для получения некоторых прочных сплавов. Оксид кальция (CaO) - негашеная известь Применение: При взаимодействии с водой выделяется большое количество теплоты, и оксид кальция превращается в гидроксид кальция - гашеная извеcть. Гидроксид кальция (Ca(OH)2) - гашеная известь Применение: Гидроксид кальция применяется в виде гашеной извести, известкового молока, и известковой воды. Гашеная известь: Белый рыхлый порошок немного растворенный в воде. Тестообразную смесь гашеной извести с цементом, водой и песком используют в строительстве. Смесь постепенно твердеет. Известковое молоко: Суспензия, похожая на молоко. Она образуется при смешивании избытка гашеной извести с водой. Известковое молоко применяется для получения хлорной извести, производстве сахара, для побелки стволов деревьев. Известковая вода: Прозрачный раствор гидроксида кальция. Известковую воду получают фильтрованием известкового молока. При прохождении через нее оксида углерода мутнеет СаС2– применяют для получения ацетилена и восстановления металлов, некоторые соли (CaCl2, глюконат кальция) – используются как лекарственные средства. Д) Следующая наша остановка станция «Биологическая роль кальция» Давайте попытаемся вспомнить, какова биологическая роль кальция, в состав чего входит этот элемент в нашем организме. Среди главных функций, выполняемых кальцием, необходимо перечислить следующие жизненно важные процессы: -образование костной ткани (организм постоянно избавляется от старых клеток, а на их месте появляются новые – все это происходит благодаря наличию кальция в структуре костной ткани); -помогает мышцам расслабляться (особенно это важно для сердца, которое никогда не перестает работать и потому наличие фазы его отдыха является чрезвычайно важным фактором нормального функционирования всего организма); -расслабление мышц, прикрепленных к скелету человека (именно с этой целью кальций рекомендуется принимать для того, чтобы снять судороги); -регулирование свертываемости крови (при нехватке кальция рана долго не может закрыться, что приводит к потери большого количества крови и к возможному заражению открытой раны.
| А)1. Один ученик отвечает у доски. В ПСХЭ Д. И. Менделеева кальций Са расположен в 4-м периоде II группы главной подгруппы.
(По желанию учащийся может привести состав, графическую схему и электронную формулу кальция)
2. Работа учащихся в методических пособиях №1, с последующим заслушиванием ответов. Кальций Са -металл. В своих соединениях проявляет валентность равную двум, т. е. образовывает две связи, за счет двух 4s электронов. Основная степень окисления +2 Формулы высшего оксида и гидроксида СаО и Са(ОН)2. Оба соединения проявляют основные
свойства. Б) Внимательно слушают учителя, задают вопросы. Заполняют или дополняют методическое пособия №1 (недостающие данные сообщает учитель)
В) Учащиеся вспоминают о соединениях металлов. Записывают формулу CaO и определяют его характер, вспоминают свойства основных оксидов. Задают вопросы Учащиеся записывают формулу Ca(OH)2 и определяют его характер, вспоминают свойства гидроксидов, задают вопросы по данной теме.
Г) Внимательно слушают учителя, просмотр слайдов, задают вопросы.
Д) Слушают учителя, высказывают свои предположения на задаваемые вопросы. На слайдах учащиеся рассматривают продукты, содержащие кальций: сыр, творог, мясо, рыба, зелень, чеснок.
| Записи на доске, учебник, презентация |







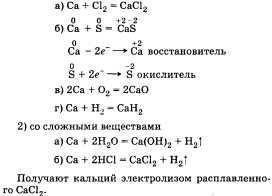 ) По физическим свойствам: кальций - металл серебристо-белого цвета, относительно легкий (плотность р = 1,54), температура плавления 854 °С, окисляется на воздухе.
) По физическим свойствам: кальций - металл серебристо-белого цвета, относительно легкий (плотность р = 1,54), температура плавления 854 °С, окисляется на воздухе.









