Урок химии "Классификация химических реакций". 8-й класс
Цель урока: систематизировать уже имеющиеся знания учащихся о химических реакциях с помощью классификации химических реакций по числу и составу исходных и полученных веществ.
Задачи:
Образовательная - систематизировать, обобщить и углубить знания учащихся о химических реакциях и их классификации, развить навыки самостоятельной работы, умения записывать уравнения реакций и расставлять коэффициенты, указывать типы реакций, делать выводы и обобщения.
Развивающая - развить речевые навыки, способности к анализу; развитие познавательных способностей, мышления, внимания, умения использовать изученный материал для познания нового.
Воспитательная - воспитание самостоятельности, сотрудничества, нравственных качеств – коллективизма, способности к взаимовыручке.
Тип урока: урок обобщения, систематизации и закрепления с элементами получения новых знаний
Оборудование: спиртовка, цинк, соляная кислота, штатив, пробирки, лучинка, вата, хлорид бария, сульфат натрия, серная кислота, вода, бихромат аммония, презентация.
Методы:
Словесный (рассказ, беседа, объяснение);
Наглядный (проектор);
Практический (выполнение опытов).
Приемы: лабораторная работа; демонстрационный опыт; самостоятельная работа; ребус, загадка как фрагмент дидактической игры.
Форма работы: групповая, фронтальная, индивидуальная.
Ход урока
1. Организационный момент. (1 мин) (Мотивация к уроку)
Без химии ты глух и нем
И шагу не шагнешь порою,
Не вырастишь хороший хлеб
И дом хороший не построишь.
Химию любить и не лениться –
Значит, понятно будет все:
Почему коптит порою примус,
На морозе сушится белье.
Жизнь вокруг себя узнаешь,
Разрешишь любой серьезный спор,
Без огня в дороге яйца сваришь
И без спичек разведешь костер
2. Этап актуализации знаний. Повторение изученного материала
| Деятельность учителя | Деятельность ученика |
| Сегодня мы продолжим разговор о химических реакциях. Для этого повторим некоторые сведения о веществах и химических превращениях. Возьмите каточки, разложенные на столах, подпишите фамилию и ответьте на вопросы, предложенные на слайде. Время работы – 5м.  | Учащиеся работают самостоятельно по заданиям на индивидуальной карточке и на слайде презентации (Приложение 1). Слайд№2
|
Задание на карточке учащегося (Приложение 1):
| I вариант | II вариант |
| Напишите определение: |
| Химическое явление – … | Уравнение химической реакции – … |
| Выберите из предложенных веществ, определите валентность химических Элементов: |
| простые | сложные |
| N2; CO2; H2O; HCl; O3; Сu; Fe2O3; H2 |
| Деятельность учителя | Деятельность ученика |
| Отложите карточки и посмотрите на следующий слайд. С помощью общепринятых правил разгадывания ребуса и загадки, отгадайте слово (1 минута). | Учащиеся отгадывают ребус и загадку. |
| Проверим задание. У кого получилось слово целиком? 
-Отгадай загадку и узнай о чем пойдет речь на сегодняшнем уроке 
| Классификация. (Можно проверить слово по частям, соответствующим картинкам: класс (убрать букву «с»), сифон (убрать буквы «о», «н»), акация (первую букву «а» заменить на букву «и»). (Слайд№3,4) |
|

| Учащиеся записывают тему урока со слайда (Слайд№5) |
На слайде появляется разгаданное слово и дополняющие слова, формулирующие тему урока:
Этап усвоения новых знаний
| Деятельность учителя | Деятельность ученика |
| На предыдущих уроках мы знакомились с химическими явлениями или химическими реакциями, с условной записью уравнений химических реакций на основании закона сохранения массы веществ. Сегодня мы попытаемся дать первую классификацию химическим процессам на основе имеющихся знаний. | 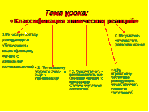
|
| Лабораторный опыт горение магния |
| Сколько веществ вступило в химическую реакцию? | Два. |
| А образовалось? | Одно. |
| Давайте представим схему реакции. Запишите уравнение химической реакции в тетради. Проверим 2Mg + O2 = 2MgO | Учащиеся составляют уравнение реакции горения магния в тетради и проверяют на доске 2Mg + O2 = 2MgO |
|
|
| Итак, в химическую реакцию вступило, соединилось два вещества, а образовалось одно вещество. Как вы думаете, к какому типу относится данная реакция? | Соединения. |
| Правильно. Запишите, пожалуйста, определение данного типа реакции со стр. 36 в учебнике. Повторим еще раз. | Один из учащихся дает определение реакции соединения.
Химические реакции, в которые вступают два вещества и более, а получается одно более сложное вещество, называются реакциями соединения. |
| II. Давайте рассмотрим следующий тип химических реакций. Для этого необходимо провести лабораторный опыт. |
|
| Запишите название лабораторного опыта в тетради. | Учащиеся записывают название опыта и приступают к его выполнению. |
| Лабораторный опыт «Разложение бихромата аммония (NH4)2Cr2O7». |
| Положите бихромат аммония в фарфоровую чашку, сделайте углубление, капните 1-2 капли спирта и осторожно подожгите. Опишите его физические свойства. По каким признакам вы можете определить, что прошла химическая реакция? (NH4)2Cr2O7 = Сr2O3 + N2 + 4H2O | Ученик 1. Вещество твердое, оранжевого цвета. В процессе реакции изменило цвет с оранжевого на темно-зеленой цвет. Ученик 2. На стенках чашки появились капли воды. |
| Ответьте на вопросы. Сколько веществ первоначально вступило в реакцию? | Одно. |
| Сколько веществ образовалось? | Мы заметили два вещества: зеленый порошок и вода и газ |
| Посмотрите, как записывается уравнение данной химической реакции на слайде и объясните, почему вы не увидели еще одно вещество? (Приложение 1) | Третьим получившимся веществом в этой реакции является газ. Он не имеет цвета и запаха. |
|
|
| III. С помощью следующего лабораторного опыта рассмотрим еще один тип химических реакций. Работать будем капельным методом. Одно из веществ, участвующих в реакции, – кислота. Работают с кислотами аккуратно и осторожно. Запишите название опыта. | Учащиеся записывают название опыта в тетрадь. |
| Лабораторный опыт «Взаимодействие цинка с соляной кислотой». |
| Возьмите планшет для проведения реакций капельным методом. В одной из ячеек планшета находится гранула цинка. Рассмотрите металл. Добавьте в ячейку небольшое количество соляной кислоты. Какие признаки химической реакции вы наблюдаете? | Учащиеся выполняют опыт под руководством учителя. Описывают наблюдения. Ученик. Наблюдается выделение газа. Это признак химической реакции. |
| Правильно. Давайте запишем уравнение химической реакции в тетрадь, проверим его. (Приложение 1) Рассмотрим с точки зрения состава веществ, какие вещества вступили в реакцию, а заодно еще раз проверите задание 2 на своей карточке. | Zn + 2HCl = ZnCl2 + H2 Ученик 1. Цинк состоит из атомов одного вида, следовательно, цинк – простое вещество. Ученик 2. Молекула соляной кислоты состоит из атомов разного вида, следовательно, соляная кислота – сложное вещество. |
|
|
| Т.е. в данную реакцию вступили простое вещество и сложное вещество. А получились? | Получились два вещества. Одно простое – водород. Одно сложное. |
| Это сложное вещество называется хлорид цинка. Подпишите название вещества под его формулой. Найдите определение данного типа реакций в учебнике на стр. 36, запишите его в тетрадь. Проверим. | Учащиеся подписывают названия веществ, проверяя себя по слайду.
Записывают определение в тетрадь, один из учащихся повторяет. Ученик. Реакции, в которых атомы простого вещества замещают атомы в сложном веществе, называются реакциями замещения. |
| IV. Четвертый тип реакций – это реакции обмена. Более подробно мы познакомимся с ними позже, а сейчас посмотрим опыт, определим признаки реакции и запишем в тетрадь уравнение химической реакции и определение. Демонстрационный опыт: «Взаимодействие серной кислоты и хлорида бария». | Учащиеся записывают в тетрадь название опыта «Взаимодействие серной кислоты и хлорида бария». |
|
|
| В химическом стакане находится раствор вещества серной кислоты . Опишите его видимые свойства. | Ученик. Бесцветное, жидкое вещество |
| Добавим в стакан раствор другого вещества – хлорида бария. По каким признакам можно судить, что прошла химическая реакция? | Изменился цвет. Стал белый и непрозрачный. |
| Говорят, выпал осадок, образовалось нерастворимое вещество. Давайте вместе запишем уравнение реакции. H2SO4 + BaCl2 = 2HCl + BaSO4↓ Обратите внимание, если вещество не растворяется в воде, то при написании уравнения химической реакции рядом с формулой вещества ставится стрелка вниз. Подпишем названия под формулами веществ: серная кислота , хлорид бария, соляная кислота, сульфат бария | Учащиеся записывают уравнение реакции в тетрадь H2SO4 + BaCl2 = 2HCl + BaSO4↓, подписывают названия веществ. |
| Обратимся к составу веществ. В данную реакцию вступили два сложных вещества и образовались два сложных вещества. В процессе реакции они поменялись, обменялись составными частями, поэтому данный тип реакций называется реакциями обмена. Запишем определение в тетрадь. Реакции, в ходе которых сложные вещества обмениваются составными частями, называются реакциями обмена. | Учащиеся записывают определение реакции обмена. Реакции, в ходе которых сложные вещества обмениваются составными частями, называются реакциями обмена. |
Физкульминутка: Показать действием-движением реакции разложения, соединения, обмена, замещения
Этап закрепления полученных знаний
| Деятельность учителя | Деятельность ученика |
| Итак, проверим, что усвоилось, и повторим пройденное. Возьмите свои карточки и выполните оставшиеся задания, опираясь на запись | Учащиеся работают самостоятельно по карточкам, полученным в начале урока. |
| I вариант | II вариант |
| Выберите схемы уравнений химических реакций, соответствующие реакциям. Расставьте коэффициенты: Fe(OH)3 → Fe2O3 + H2O; Li + O2 → Li2O; CuSO4 + Fe → FeSO4 + Cu Li2O + H2O → LiOH; HCl + MgO → MgCl2 + H2O; HNO3 → NO2 + H2O + O2 |
| Соединения | Разложения |
| Обмена | Замещения |
Этап рефлексии
| Деятельность учителя | Деятельность ученика |
| 
| Учащиеся оценивают урок, свою деятельность на уроке, комфортность на предложенной схеме. Сдают листочки с работой. |
Учитель. Запишите домашнее задание 16, упр. 5-7, стр. 47-48. Сдайте листочки с работой. Урок окончен. Классификация химических реакций( схема в тетради),
«5» -написать 4 примера хим-ских реакции с коэффициентами,
«4»- написать 3 примера хим-ских реакции с коэффициентами
«3»- написать 2 примера хим-ских реакции с коэффициентами
Самооценка + оценка учителя = средняя оценка ставится в журнал.
Приложение №1
Карточка 1: САМОСТОЯТЕЛЬНАЯ РАБОТА УЧЕНИКА_______________________
| ФИО |
| I вариант | II вариант |
| Химическое явление –
| 1. Уравнение химической реакции –
|
| 2. Выберите из предложенных веществ N2; CO2; H2O; HCl; O3; Сu; Fe2O3; H2 |
| Простые вещества | Сложные вещества |
|
|
|
| 3. КЛАССИФИКАЦИЯ |
| 4. Реакции соединения:
| 4. Реакции разложения:
|
| 5. Реакции обмена:
| 5. Реакции замещения:
|
1_______,2_________,3________4__________
МКОУ «Ортолыкская средняя общеобразовательная школа им.М.И.Лапшина»
УРОК ПО ХИМИИ
в 8 классе
по теме:
"Классификация химических реакций"

Разработчик: учитель химии
Джуманова Е.Ж.,
Стаж работы: 15лет,1 КК
с.Ортолык,2016г
Представление
на урок химии учителя
МКОУ «Ортолыкская средняя общеобразовательная школа им.М.И.Лапшина» Джумановой Е.Ж.
Предметная область: химия
Тема урока: "Классификация химических реакций".
Класс: 8-й
Цель урока: систематизировать уже имеющиеся знания учащихся о химических реакциях с помощью классификации химических реакций по числу и составу исходных и полученных веществ.
Форма организации учащихся: индивидуальная , коллективная
Тип урока: урок обобщения, систематизации и закрепления с элементами получения новых знаний
Оформление урока: 1) компьютер, проектор, экран, необходимые реактивы к уроку
Урок с элементом системно-деятельностного подхода. Основным этапом урока является знакомство с классификацией химических реакций по количеству вступивших и получившихся веществ и по их составу. Изучение проводится на основе повторения и закрепления ранее изученного материала о простых и сложных веществах, химических реакциях, химических формулах. Рассматриваются реакции соединения, замещения, разложения, обмена с использованием лабораторных и демонстрационных опытов.
Урок насыщен фактическим материалом, предлагаемым автором данной программы и поурочного планирования. Частичная визуализация объектов через использование ИКТ позволяет сделать работу на уроке более осмысленной. Такие уроки требуют переключения деятельности учащихся с целью усвоения материала, поддержания интереса к предмету, сохранения комфортной психологической обстановки. Ребус, загадка представленные в ходе урока, рефлексия занимают немного времени и способствуют продуктивной деятельности учащихся. При подготовке к данному уроку учитель продумал этапы проведения лабораторных и демонстрационных опытов, информацию, представленную на слайдах при использовании ИКТ.
Директор __________Б.К.Абулова
Заявка
Участника регионального этапа Международной Ярмарки социально-педагогических инноваций - 2016
| № | Содержание заявки | Информация участника |
| 1. | Тема проекта - продукта | Разработка урока «Классификация химических реакции» |
| 2. | Содержательное направление деятельности (в соответствии с Положением о Ярмарке) | Инновационные решения в сфере образования
|
| 3. | ФИО | Джуманова Еркежан Жунусовна
|
| 4. | Организация | МКОУ «Ортолыкская СОШ им.М.И.Лапшина» |
| 5. | Должность, наличие квалификационной категории | Учитель химии, 1КК |
| 6. | Стаж работы | 15 лет |
| 7. | Адрес (служебный) | С.Ортолык, ул.Эки-Тыт,10 |
| 8. | Рабочий телефон/факс | 83884228349 |
| 9. | Мобильный телефон | 89833254022 |
| 10 | Электронный адрес | [email protected] |
| 13. | Наличие продукта интеллектуальной собственности для продажи (обмена) на Ярмарке | имеется |































