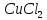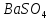Урок по теме: «Соли. Состав. Номенклатура. Классификация».
8класс
Цель: сформировать систему знаний о солях, выяснить их практическое применение.
Задачи урока:
образовательные: повторить основные понятия: оксид, основание, кислота; закрепить умение различать данные классы веществ; познакомить с понятием солей, как продуктах взаимодействия оксидов, оснований и кислот между собой; рассмотреть состав и название солей; продолжить развивать практические навыки и умения составлять формулы веществ; познакомить учащихся с физическими свойствами и классификацией солей;
развивающие: развивать умение использовать химическую терминологию, развивать мыслительные операции (анализ, синтез, установление причинно-следственных связей, проведение аналогий, обобщение);
воспитательные: воспитывать интерес к предмету, формировать навыки поведения в коллективном и индивидуальном учебном труде, осуществить экологическое воспитание учащихся на примере влияния нитратов на организм человека и живых организмов, значении поваренной соли для человека и промышленности, воспитание бережного отношения к школьному оборудованию.
Планируемые результаты обучения:
1. Предметные
обучающиеся должны знать состав и классификацию солей; составлять формулы средних солей и давать названия средним, кислым и основным солям;
составлять уравнения реакций получения и химических свойств различных групп солей;
2. Метапредметные
обучающиеся должны уметь ставить учебную задачу на основе сотнесения того, что уже известно и усвоено и того, что ещё неизвестно; вносить необходимые дополнения и коррективы в план и способ действия исходя из оценки этого результата самим обучающимся, учителем;
ставить оценку результатам своей работы; определять цели, функции участников для работы в группе, способы взаимодействия;
сотрудничать с обучающимися класса в поиске и сборе информации; уметь выражать свои мысли в соответствии с задачами; владеть монологической и диалогической формами речи в соответствии с грамматическими и синтаксическими нормами родного языка;
уметь работать с различными источниками информации, преобразовывать ее из одной формы в другую, выделять главное в тексте, структурировать учебный материал, готовить отчет об исследованиях и презентации.
3. Личностные
знать о значении солей для живого мира, их влиянии на экологическую обстановку,
обучающиеся должны самостоятельно организовывать учебное взаимодействие в группе (определять общие цели, распределять роли, договариваться друг с другом;
овладеть умением оценивать вред различных веществ на организм человека.
Методы: рассказ, беседа, частично- поисковый, объяснительно- иллюстративный, демонстрация таблиц, самостоятельная работа учащихся со справочными материалами, учебником, лабораторные опыты с элементами проблемного обучения.
Межпредметные связи: биология, география.
Средства обучения: таблица «Растворимость кислот, солей, оснований», ПСХЭ Д.И.Менделеева, таблицы, мультимедиапроектор с экраном, компьютер, презентация к уроку, учебник Химия – 8 класс (автор Рудзитис Г.Е., Фельдман Ф.Г.), Электронное приложение к учебнику Химия – 8 класс (автор Рудзитис Г.Е., Фельдман Ф.Г.) .
Оборудование и реактивы: образцы хлорида натрия, карбоната кальция, фосфата кальция.
Тип урока: комбинированный.
Ход урока
І. Оргмомент.
Учитель проверяет готовность класса к занятию. Акцентирует внимание на то, что нельзя трогать руками реактивы, стоящие на столах без разрешения учителя.
ІІ. Проверка домашнего задания:
у доски работают учащиеся с домашними упражнениями:
первый ученик -упражнение №2 (ІІ столбик) с.135
второй ученик - химические свойства оксида калия
третий ученик - химические свойства оксида серы (VI).
с места: повторить номенклатуру кислотных остатков. Повторить правила: – закончить фразу…
реакция нейтрализации – это …
кислоты – это …
оксиды – это …
классификация оксидов …
ІІІ. Актуализация знаний.
А теперь задание для всего класса:
Из предложенных на доске формул СаО, Са(ОН)2, Н2SO4, NaCl, СаCO3 , Са3(PO4)2 определить:
а) к какому классу неорганических соединений относится каждое вещество;
б) дать определение этих классов.
Формулы последних веществ вызывает затруднение. Чтобы определить принадлежность этого вещества к какому-либо классу, определяем его состав. И чтобы узнать, как называется этот класс веществ, прочтем некоторые интересные факты:
1.Это вещество входит в состав крови человека.
2.Легионеры Древнего Рима получали часть жалованья этим веществом.
3.За 5 плиток этого вещества в Эфиопии можно было купить раба.
4.Оно содержится в Мировом океане.
5.Из него в Боливии строят отели.
6.Наши предки встречали гостей в знак дружбы хлебом и … солью!
Как называется класс веществ, который мы будем изучать?
Этот класс веществ называется соли.
Эпиграф: Соль – всему голова, без соли и жито – трава.
Эта русская пословица свидетельствуют о большом значении солей в нашей жизни. Мы сегодня выясним, какие вещества называются солями, познакомимся с классификацией этих веществ, их применением.
ІV. Изучение новой темы.
Запишите тему урока «Соли. Состав. Номенклатура. Классификация» (слайд №1)
Нашей задачей будет познакомиться с составом солей, и научиться составлять названия солей (слайд №2)
-А теперь давайте вернемся к нашим оставшимся формулам: NaCl, CaCO3, Са3(РО4)2. Перепишите формулы веществ в столбик.
Рассказ учителя: NaCI - все мы знаем, что это хорошо растворимая в воде соль, известна под названием поваренная соль. Без этой соли невозможна жизнь растений, животных и человека. Садясь за стол, никто и не думает о том, что из-за данного кристаллического белого порошка, люди когда-то могли сражаться друг с другом, кочевать из стран в страны, продавать в рабство.
Вспомните, были ли в России какие-нибудь войны, либо бунты из-за соли? (Соляной бунт. 1648 г.) Боярин Б. И. Морозов обложил налогом часть продуктов, в том числе и соль.
Значение соли отражено в многочисленных пословицах, поговорках, обычаях. Хлеб и соль стали символом гостеприимства и радушия русской нации.
Пословицы и поговорки:
1.Без соли стол кривой (Говорится тогда, когда к столу не подана соль).
2.Недосол на столе, а пересол на спине. (Недосоленное кушанье можно досолить, а за пересоленное только наказать. За обедом прежде всего гневались на повара).
3. Друга узнать - вместе пуд соли съесть.
В названиях многих городов и поселков разных стран присутствует слово соль: Солт-Лейк-Сити (США, штат Юта). «Солт» в переводе с английского значит «соль». В названиях русских городов так же встречается слово «соль»: Соль-Илецк (Город расположен в 70 км. от Оренбурга), Соликамск (Пермский край) Усолье (Пермский край) Усолье-Сибирское, (Иркутская область), Соледар (Донецкая область). Во всех этих городах происходит добыча соли.
В России, в Астраханской области, есть озеро в котором концентрация соли такая, что удерживает человека на поверхности воды. Название этого озера Баскунчак. Солёность озера — около 300 г/л. В воде обитают только бактерии, которые выносят соль.
Мы с вами говорили о поваренной соли. Но не все соли солены! Давайте познакомимся с другими солями.
CaCO3 входит в состав мрамора, мела, известняка. Это соль, из которой морские животные (моллюски, простейшие) строят покровы своего тела. Скапливаясь после гибели на дне морей, эти раковины за сотни миллионов лет образовали мощные пласты известняков. Эта соль - строительный материал наружного скелета моллюсков, кораллов, ракушек, скорлупы яиц.
Замечательный строительный камень — мрамор – состоит только из СаСО3. Есть белый, но чаще всего различные примеси окрашивают его в различные цвета. Чистый белый мрамор встречается редко и в основном идет на работу скульпторам. В строительстве цветной мрамор используют как облицовочный материал (Московское метро) или даже в качестве основного строительного материала дворцов.
Следующее вещество, относящееся к классу соли это: Са3(РО4)2— это основа минералов фосфоритов и апатитов. Из них производят необходимые в сельском хозяйстве фосфорные удобрения, без которых, в свою очередь, было бы невозможно получение высоких урожаев: фосфорная мука, суперфосфаты, аммофос.
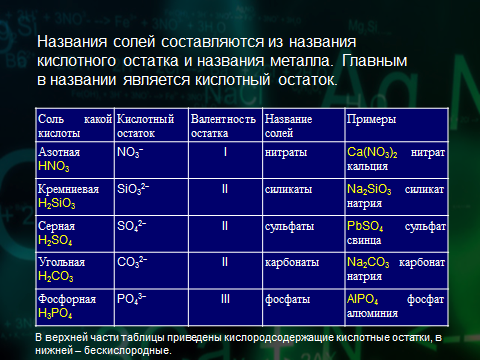
А теперь давайте научимся называть соли. Вернемся в нашим трем солям и дадим им названия:(первую соль называет учитель и записывает): NaCl - хлорид натрия, СaCO3 -карбонат кальция, Са3(РО4)2 - фосфат кальция. У данных металлов валентность постоянная, поэтому в скобках мы ее не указываем (слайд №3, 4)
Задание 1. Попробуйте сами дать названия следующим солям: KNO3 - нитрат калия, СuSO4 – сульфат меди (II)
Задание 2. Составьте формулы следующих солей: сульфат алюминия

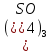 , нитрат меди (II) Cu(NO3)2, сульфат натрия Na2SO4.
, нитрат меди (II) Cu(NO3)2, сульфат натрия Na2SO4.
Алгоритм составления формул солей:
Напишем химический знак алюминия и обозначение кислотного остатка серной кислоты, поставим валентность.
Найдем наименьшее общее кратное, выражающее валентность алюминия и валентность кислотного остатка. Наименьшее общее кратное этих чисел – 6
Найдем число атомов алюминия и число кислотных остатков.
Классификация солей
СОЛИ
средние кислые основные ( слайд №5, 6)
Na2CO3, CuSO4 NaHСO3, NaHSO4 CuOHCl, AlOHCl2
а) соли средние (нормальные): Na2CO3, CuSO4 – это продукт полного замещения всех атомов водородав кислоте на атомы металла.
б) соли кислые: NaHСO3, NaHSO4 - результат неполного замещения атомов водорода в кислоте на атом металла. Такие соли получаются при избытке кислоты. В названии таких солей на первое место ставится слово «гидро», далее называется кислотный остаток и самым последним – металл: гидрокарбонат натрия.
в) соли основные: CuOHCl, AlOHCl2 – это соли, в составе которых имеются гидроксогруппы. Такие соли получаются при избытке основания. В названии этих солей на первое место ставится слово «гидроксо», далее называется кислотный остаток и металл: гидроксохлорид меди (II).
Применение солей
Выступление эксперта – химика (слайд №8)
«Собираясь пить чай, клади в него щепотку соли. От неё быстрее усвоится пища, исчезнут болезни желудка».
Из бурятской народной медицины.
Соль – хлорид натрия встречается в природе в виде минерала называемого галитом, от греческого «галос», означающего соль и море. Гомер называл хлорид натрия «божественной солью». Соль дороже золота, поскольку без золота жить можно, а без соли нельзя. В далекие времена соль была драгоценностью. На столах солей, императоров, королей и шахов стояли солонки из золота и заведовал ими особо доверенный человек – солоничий.
Воинам платили жалование солью, а чиновники получали солевой паек.
Торговля солью являлась государственной монополией. По русскому обычаю, когда подносят хлеб-соль, то тем самым желают им здоровья. В католической церкви при крещении в ротик младенца кладут кристаллик соли. У всех народов разных времен рассыпать соль значило накликать беду, потерять здоровье. (Демонстрация фотографий электронного приложения «Фотоизображения хлоридов»)
Выступление эксперта – диетолога
Различные растения обладают разной способностью к накоплению нитратов: из овощей несомненные лидеры – зеленые культуры (салат, укроп, петрушка и т.д.), за ними идет свекла, дальше с существенным отставанием – капуста и морковь. У картофеля менее развита склонность к такому накопительству.
Распределяются нитраты в разных овощах неравномерно, концентрируясь в определенных зонах, например, капуста накапливает нитраты в кочерыжке м верхних листьях; огурцы и патиссоны – в кожуре; кабачки, свекла, морковь – в нижней части плода.; картофель – в середине.
Как избавиться от нитратов в продуктах?
Специалисты рекомендуют:
- удалять из овощей «нитратные зоны».
- отваривать овощи, т.к. нитраты хорошо растворяются. В отвар уйдет большая часть вредных соединений.
- рекомендуем овощи солить, мариновать, квасить, так как при таких заготовках в рассол уходит до 60% нитратов.
Вода с повышенным содержанием нитратов представляет потенциальную опасность для здоровья человека и животных. Она имеет горько-соленый вкус и непригодна для питья. Внесение избыточного количества азотных удобрений приводит к накоплению нитратов в растениях. Увеличение содержания нитратов в овощных культурах, зеленом корме значительно снижает их биологическую ценность, вкусовые качества.
V. Закрепление материала (работа в парах)
Задание. Составить формулы солей и дать названия.
| Формула | Название |
| 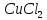
| - |
| - | нитрат серебра |
| 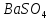
| - |
| - | сульфид цинка |
VI. Итог. Оценивание
Учитель:
– Какие моменты урока наиболее запомнились?
– Какой ответ на основной вопрос урока мы можем дать?
– Как оцените свою работу? Выставление оценок.
VII. Домашнее задание
§ 46
Составить формулы веществ, найти и выписать области применения:
калийная селитра (нитрат калия)
поваренная соль (хлорид натрия)
ляпис (нитрат серебра)
норвежская селитра (нитрат кальция)
Задача
Мы каждый день употребляем в пищу соль - хлорид натрия.
- Где она еще применяется?
Она применяется для обработки кожевенного и мехового сырья.
Ученые подсчитали, что человек в день употребляет 12-15г соли. Сколько соли съели вы за свою жизнь!
Сделаем следующий расчет потребления соли, взяв за основу
15г - в сутки.
За месяц 15г х 30 = 450г
За год 450г х 12 = 5400г
Теперь рассчитайте, сколько вы съели соли за свою жизнь. Для этого количество соли, которое вы употребили за год, умножьте на свой возраст.
- Сколько получилось?
VIII. Рефлексия. «Сигнальные карточки»
Зеленая – «Мне было интересно»
Синяя – «Я усвоил новую информацию»
Желтая – «Мне было сложно»
Красная – «Я ничего не понял»
Приложение







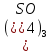 , нитрат меди (II) Cu(NO3)2, сульфат натрия Na2SO4.
, нитрат меди (II) Cu(NO3)2, сульфат натрия Na2SO4.