СДЕЛАЙТЕ СВОИ УРОКИ ЕЩЁ ЭФФЕКТИВНЕЕ, А ЖИЗНЬ СВОБОДНЕЕ
Благодаря готовым учебным материалам для работы в классе и дистанционно
Скидки до 50 % на комплекты
только до
Готовые ключевые этапы урока всегда будут у вас под рукой
Организационный момент
Проверка знаний
Объяснение материала
Закрепление изученного
Итоги урока

Была в сети 17.05.2023 15:01
Зубенко Вера Алексеевна
учитель химии
61 год
Местоположение
Россия, Севастополь
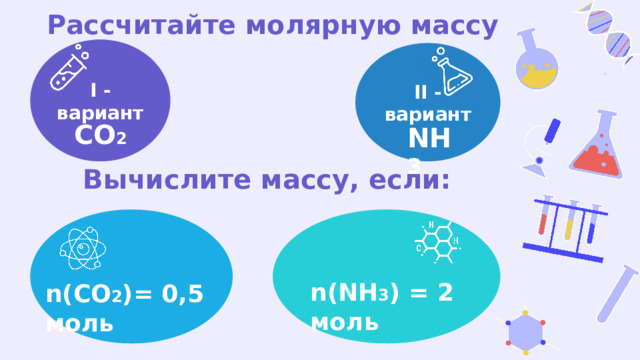
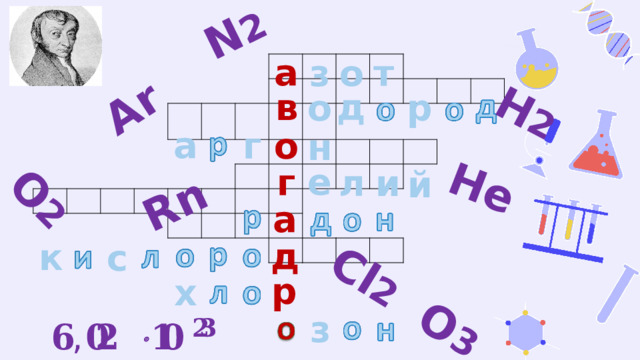
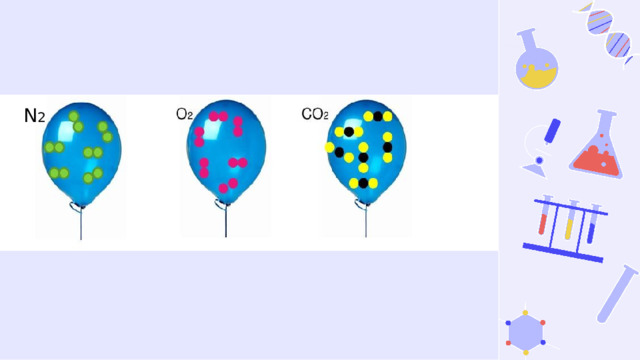
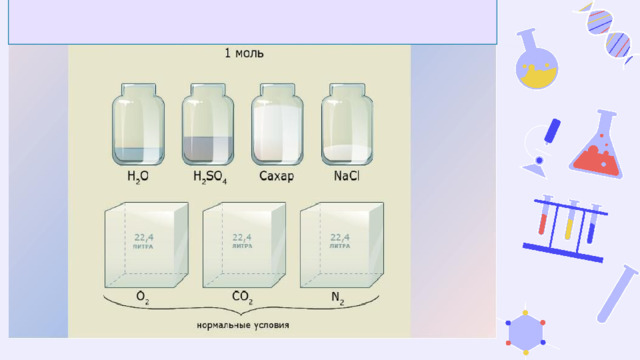
Урок в 8 классе "Закон Авогадро. Молярный объем газов"
Категория:
Химия
17.05.2023 14:46