ВАРИАНТ 1
Определите, в главных подгруппах каких групп периодической системы находятся химические элементы, электронные схемы атомов которых приведены в первом столбце таблицы. Буквы, соответствующие правильным ответам, дадут название элемента.
| Электронные схемы | Группы |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 2е 4е | Щ | Ж | Э | К | А | Б | У |
| 2е 8е 2е | В | А | К | М | Н | О | П |
| 2е 1е | Л | С | Ы | Ф | Ю | А | Я |
| 2е 8е 5е | Р | Б | Т | В | Ь | Е | Г |
| 2е 8е 1е | Ц | Д | Ж | И | К | З | М |
| 2е 8е 7е | Л | О | В | Н | У | П | И |
| 2е 8е 3е | Р | Т | Й | Х | Ц | Ч | Ф |
ВАРИАНТ 2
Определите, в главных подгруппах каких групп периодической системы находятся химические элементы, электронные схемы атомов которых приведены в первом столбце таблицы. Буквы, соответствующие правильным ответам, дадут название элемента.
| Электронные схемы | Группы |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 2е 4е 2е | Щ | Ф | Э | К | А | Б | У |
| 2е 8е 1е | О | А | К | М | Н | О | П |
| 2е 1е 5е | Л | С | Ы | Ф | С | А | Я |
| 2е 8е 3е | Р | Б | Ф | В | Ь | Е | Г |
| 2е 8е 4е | Ц | Д | Ж | О | К | З | М |
| 2е 8е 7е | Л | О | В | Н | У | П | Р |
Урок химии в 9 классе.
Тема - Открытие Менделеевым периодического закона
Открытию периодического закона предшествовало накопление знаний о веществах и свойствах. По мере открытия новых химических элементов, изучения состава и свойств их соединений появлялись первые попытки классифицировать элементы по каким-либо признакам. В общей сложности до Д.И. Менделеева было предпринято более 50 попыток классификации химических элементов. Ни одна из попыток не привела к созданию системы, отражающей взаимосвязь элементов, выявляющей природу их сходства и различия, имеющей предсказательный характер.
При переходе от лития к фтору происходит закономерное ослабление металлических свойств и усиление неметаллических.
При переходе от фтора к следующему по значению атомной массы элементу натрию происходит скачок в изменении свойств (Nа повторяет свойства Li)
За Na следует Mg, который сходен с Ве - они проявляют металлические свойства. А1, следующий за Mg, напоминает В. Как близкие родственники, похожи Si и С; Р и N; S и О; С1 и F.
При переходе к следующему за С1 элементу К опять происходит скачок в изменении и химических свойств.
На основании своих наблюдений 1 марта 1869 г. Д.И. Менделеев сформулировал периодический закон, который в начальной своей формулировке звучал так: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементо
Д. И. Менделеев опубликовал свою первую схему периодической таблицы в 1869 году в статье «Соотношение свойств с атомным весом элементов» (в журнале Русского химического общества); ещё ранее (февраль 1869 г.) научное извещение об открытии было им разослано ведущим химикам мира. Днём открытия периодического закона считается 1 марта (17 февраля по старому стилю) 1869 года, в который Д. И. Менделеев закончил работу над «Опытом системы элементов, основанной на их атомном весе и химическом сходстве». И только в декабре выходит работа немецкого химика Мейера, который изменил своё решение в пользу мысли Д. И. Менделеева и в зарубежной литературе считается либо «одним из первооткрывателей», либо «независимо от Менделеева опубликовавшим этот периодический закон».
По легенде, мысль о системе химических элементов пришла к Менделееву во сне, однако известно, что однажды на вопрос, как он открыл периодическую систему, учёный ответил:
«Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово».
В начале XX века с открытием строения атома было установлено, что периодичность изменения свойств элементов определяется не атомным весом, а зарядом ядра, равным атомному номеру и числу электронов, распределение которых по электронным оболочкам атома элемента определяет его химические свойства.
Дальнейшее развитие периодической системы связано с заполнением пустых клеток таблицы, в которые помещались всё новые и новые элементы: благородные газы, природные и искусственно полученные радиоактивные элементы. В 2010 году, с синтезом 117 элемента, седьмой период периодической системы был завершён, проблема нижней границы таблицы Менделеева остаётся одной из важнейших в современной теоретической химии.
Днём открытия периодического закона считается 1 марта (17 февраля по старому стилю) 1869 года, в который Д. И. Менделеев закончил работу над «Опытом системы элементов, основанной на их атомном весе и химическом сходстве».
1. Заполните таблицу
Таблица
| Поряд-
ковый номер | Символ
химического элемента | Русское название | Произ-
ношение | Номер периода | Номер ряда | Группа | Под-
группа |
| 7 | N | Азот | Эн | 2-й | 2-й | V | Главная |
| 1 | | | | | | | |
| | Мg | | | | | | |
| | | Кислород | | | | | |
| | | | Силициум | | | | |
| 29 | | | | | | | |
| | He | | | | | | |
| | С | | | | | | |
| 16 | | | | | | | |
| | | | Эс | | | | |
| | | Цинк | | | | | |
| | Hg | | | | | | |
| | Ba | | | | | | |
| 14 | | | | | | | |
| | | Фосфор | | | | | |
| | | | Хлор | | | | |
| | Cu | | | | | | |
| | | Серебро | | | | | |
| | | | Калий | | | | |
| | | Кальций | | | | | |
| | | | Феррум | | | | |
| 23 | | | | | | | |
2 Из таблицы 5 выпишите знаки (символы) элементов металлов и неметаллов.
3 Запишите знаки элементов:
2-го периода ……………………………………………………………………………………….. ,
Iа подгруппы ………………………………………………………………………………………. ,
Iв подгруппы ………………………………………………………………………………………. .
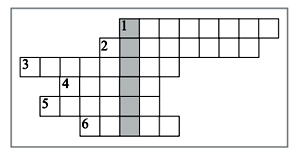
4. Кроссворд «Названия химических элементов». Впишите в кроссворд названия химических элементов и разгадайте зашифрованное ключевое слово.
По горизонтали: 1. Химический элемент с порядковым номером 46. 2. Элемент, расположенный во II группе главной подгруппы, во 2-м периоде. 3. Элемент, простое вещество которого необходимо для дыхания. 4. Металл, расположенный во 2-м периоде. 5. Элемент, произношение которого «пэ». 6. Элемент VIII группы главной подгруппы.