
Жидкие вещества и роль воды в химических реакциях.
Выполнила: Власенко А.В.

Чем отличаются жидкости от газов и биологическая роль воды.
Жидкости текучи, т.е. не имеют своей формы, потому что молекулы находятся рядом, поэтому, при попытке изменить объем жидкости начинается деформация самих молекул, поэтому жидкости молосжимаемы.
Биологическая роль воды велика, ведь, как известно, животные, растения, человек состоят из нее на 70-80%. Все реакции обмена веществ в организме, гидролиза, протекают с участием воды. Без воды было бы невозможно существование биосферы, да и жизни на Земле.
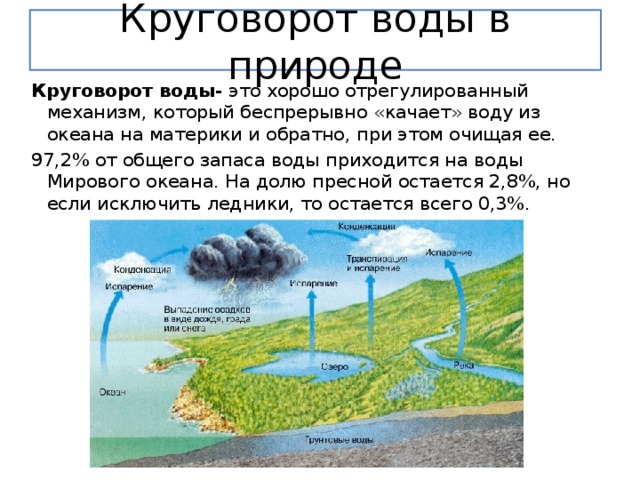
Круговорот воды в природе
Круговорот воды- это хорошо отрегулированный механизм, который беспрерывно «качает» воду из океана на материки и обратно, при этом очищая ее.
97,2% от общего запаса воды приходится на воды Мирового океана. На долю пресной остается 2,8%, но если исключить ледники, то остается всего 0,3%.

Что значит выражение «жесткая вода»?
Жесткой называют воду, содержащую ионы кальция, магния, железа. В жесткой воде мыло не мылится, при стирке белья повышается расход моющих средств, а волосы при мытье секутся, появляется накипь в чайнике и т.д. Этому способствует также особая группа солей, которые называют кислыми.
Кислыми называют соли, которые являются продуктами неполного замещения атомов водорода в молекуле кислоты на металл.
Жесткость воды называют временной и постоянной . В первом случае, она устраняется кипячением, а во втором, ее никак не устранить.

Минеральная вода.
Минеральная вода — вода, содержащая в своем составе растворённые соли, микроэле-менты, а также некоторые биологически активные компоненты. Наиболее богат минеральными источниками одноименный район Кавказских Минеральных вод. Она полезна, потому что дистиллированная, искусственная вода, «вымывает» из организма человека необходимые ему минеральные соли.

Свойства воды.
Одним и важных свойств воды является растворимость в ней других веществ. При этом все вещества делят на несколько типов: растворимые , малорастворимые и практически нерастворимые .
Итак, вода является реакционной средой , фактором диссоциации , транспортом веществ , катализатором и реагентом .

Гидратация, что это?
Растворы делят на молекулярные, ионные и ионно-молекулярные. Даже в молекулярных растворах веществ содержатся уже совсм не те молекулы, из которых было построено исходное вещество. Эти молекулы окружены оболочкой из молекул воды, их называют гидратированными. Они предствляют собой результат взаимодействия воды с молекулами растворяемого вещества-процесса гидратиции.

Что же для электролитов?
Электролиты- это вещества, которые в растворах распадаются на ионы- диссоциируют. Все электролиты диссоциируют по-разному, это зависит от степени электролитической диссоциации, ею называют отношение числа молей вещества, распавшегося на ионы, к общему количеству растворенного вещества.
По величине их разделяют на сильные и слабые.

Типы электролитов.
- Кислоты - это электролиты, диссоциирующие на катионы водорода и анионы кислотного остатка.
- Основания - это электролиты, диссоциирующие на катионы металла (аммония или органические основания) и гидроксид-анионы.
- Соли - это электролиты, диссоцииирующие на катионы металла (аммония или органического основания) и анионы кислотного остатка.

Некоторые факты
- В составе мантии Земли воды содержится в 10-12 раз больше, чем в Мировом океане.
- Если бы все ледники растаяли, то уровень воды в земных океанах поднялся бы на 64 м и около 1/8 поверхности суши было бы затоплено водой.
- При определённых условиях (внутри нанотрубок) молекулы воды образуют новое состояние, при котором они сохраняют способность течь даже при температурах, близких к абсолютному нулю.
- Вода отражает 5 % солнечных лучей, в то время как снег — около 85 %. Под лёд океана проникает только 2 % солнечного света.
- Синий цвет чистой океанской воды в толстом слое объясняется избирательным поглощением и рассеянием света в воде.
- Вода — это одно из немногих веществ в природе, которые расширяются при переходе из жидкой фазы в твёрдую (кроме воды, таким свойством обладают сурьма, висмут, галлий, германий и некоторые соединения и смеси).
- Вода и водяной пар горят в атмосфере фтора фиолетовым пламенем. Смеси водяного пара со фтором в пределах взрывчатых концентраций взрывоопасны. В результате этой реакции образуются фтороводород и элементарный кислород.



























