
Жидкие вещества
Химия 11 класс

Цель урока: изучить жидкое состояние вещества, а именно воду.
План урока:
- Круговорот воды в природе
- Водные ресурсы
- Потребление воды на производстве и в быту
- Жесткость воды
- Способы устранения жесткости воды
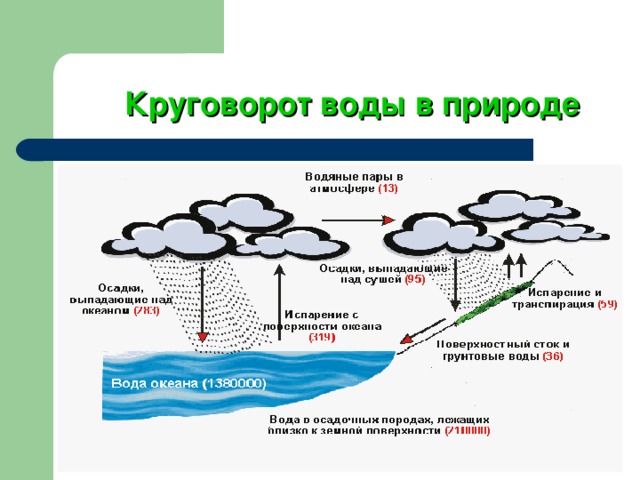
Круговорот воды в природе

Круговорот воды -
Это хорошо отрегулированный механизм, который беспрерывно «качает» воду из океана на материки и обратно, при этом вода очищается.
Ежегодно испаряется 453000 км 3 воды, а выпадает в виде осадков 525000 км 3 .
Как вы думаете, почему происходит превышение показателей?

Водные ресурсы
Вода
Соленая
97,2% - от общего запаса воды Мирового океана(1345 млн.км 2 )
Пресная
2,8% - с ледниками
0,3% - без полярных ледников
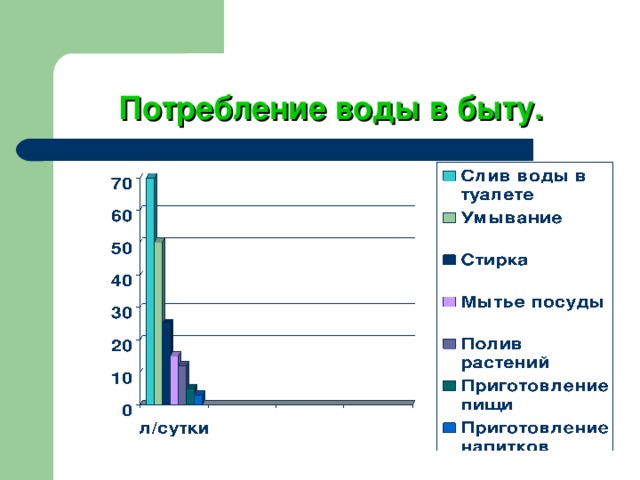
Потребление воды в быту.

Значение воды в промышленности
- Теплоноситель
- Растворитель
- Сырье
- Катализатор
- Для охлаждения реагентов

Потребление воды на производстве
В металлургии для выплавки:
1т чугуна – 300т воды
1т меди – 500т воды
1т никеля – 4000т воды
При производстве синтетических материалов:
1т лавсана – 4200т воды
1т капрона – 5600т воды
1 т бумаги – 246т воды

Жесткость воды
Жесткость – это свойство воды, обусловленное наличием в ней растворимых солей кальция и магния.
Жесткость
Временная
Содержание кислых солей – гидрокарбонатов кальция и магния
Постоянная
Содержание других растворимых солей кальция и магния

Кислые соли
- это продукты неполного замещения атомов водорода в молекуле кислоты на металл.
Н 2 СО 3 :
- Na 2 CO 3 - карбонат натрия – средняя соль
- NaHCO 3 - гидрокарбонат натрия – кислая соль.
Эти соли хорошо растворимы и диссоциируют, обусловливая жесткость воды:
Ca(HCO 3 ) 2 → Ca +2 + 2HCO - 3
Почему в жесткой воде мыло не мылится? Что такое мыло?

Мыла
- это натриевые (твердые) или калиевые (жидкие) соли жирных кислот. RCOOK и RCOONa .
Мыло не пенится, т.к. соли жирных кислот взаимодействуют с катионами кальция и магния. Пока все ионы кальция и магния не будут переведены с помощью мыла в осадок, оно стирать и мыть не будет:
2RCOO - + Ca +2 → (RCOO) 2 Ca↓

Способы устранения жесткости воды:
Кипячением устраняется временная жесткость воды. Именно так образуется накипь в чайниках, трубах центрального отопления, паровых котлах и т.д.
Ca(HCO 3 ) 2 → CaCO 3 + H 2 O + CO 2 ↑
С помощью соды и извести устраняется и временная и постоянная жесткость.
CaCl 2 + Na 2 CO 3 → CaCO 3 + 2NaCl

Продолжите следующие химические реакции:
Ca(HCO 3 ) 2 + Na 2 CO 3 →
Mg(HCO 3 ) 2 + Na 2 CO 3 →
MgCl 2 + Na 2 CO 3 →
Ca(HCO 3 ) 2 + Ca(OH) 2 →
Mg(HCO 3 ) 2 + 2Ca(OH) 2 →
MgCO 3 + Ca(OH) 2 →

Проверка
Ca(HCO 3 ) 2 + Na 2 CO 3 → С aCO 3 ↓ + 2NaHCO 3
Mg(HCO 3 ) 2 + Na 2 CO 3 → MgCO 3 + 2NaHCO 3
MgCl 2 + Na 2 CO 3 → MgCO 3 + 2NaCl
Ca(HCO 3 ) 2 + Ca(OH) 2 → 2CaCO 3 + 2H 2 O + CO 2
Mg(HCO 3 ) 2 + 2Ca(OH) 2 → Mg(OH) 2 + 2CaCO 3 + 2H 2 O
MgCO 3 + Ca(OH) 2 → Mg(OH) 2 + CaCO 3

Вывод:
Вода – уникальное и самое важное вещество на нашей планете
- Животные и растения на 70% состоят из воды
- Вода в очень больших количествах используется в быту и на производстве
- Важной характеристикой для потребителя является жесткость воды, обусловленная содержанием солей кальция и магния. В жесткой воде мыло не мылится, при стирке повышается расход моющих средств, волосы секутся.
- Жесткость воды удаляется с помощью физических и химических методов

Литература
- Габриелян О.С Химия 11 класс, М.: Дрофа, 2014.
- Илышева А.Н Вода: строение, свойства, применение, Петрозаводск, 2003

Автор презентации
Учитель химии МКОУ «Чёлмужская СОШ»
Елена Борисовна Щегелева
































