Просмотр содержимого документа
«Алкены непредельные углеводороды»

АЛКЕНЫ
НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ

Алкены – углеводороды, содержащие в молекуле одну двойную связь между атомами углерода и имеющие общую формулу С n Н 2n , где n ≥ 2
Алкены относятся к непредельным углеводородам, так как их молекулы содержат меньшее число атомов водорода, чем насыщенные
Свое второе название — «олефины» — алкены получили по аналогии с жирными непредельными кислотами (олеиновая, линолевая), остатки которых входят в состав жидких жиров — масел (от англ. oil — масло)

Для простейших алкенов применяются также исторически сложившиеся названия: этилен (этен), пропилен (пропен), бутилен
Номенклатура алкенов
- По систематической номенклатуре названия алкенов производят от названий соответствующих алканов (с тем же числом атомов углерода) путем замены суффикса –ан на –ен :
С 2 Н 4 - _ эт ен ; С 3 Н 6 -проп ен и т.д.
- Главная цепь выбирается таким образом, чтобы она обязательно включала в себя двойную связь .
- Нумерацию углеродных атомов начинают с ближнего к двойной связи конца цепи. Цифра, обозначающая положение двойной связи, ставится обычно после суффикса –ен.
Например

Гомологический ряд алкенов Общая формула С n Н 2n
- C₂H₄ → эт ен
- C₃H₆ → проп ен
- C₄H₈ → бут ен - 1
- C₅H₁₀ → пент ен - 1
- C₆H₁₂ →гекс ен - 1
- C₇H₁₄ → гепт ен - 1

Изомерия алкенов
Для алкенов возможны два типа изомерии:
1-ый тип – структурная изомерия :
- углеродного скелета
- положения двойной связи
- межклассовая
2-ой тип – пространственная изомерия : геометрическая
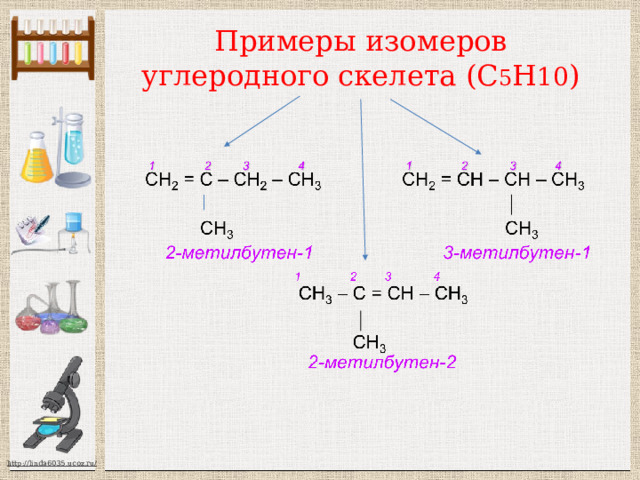
Примеры изомеров углеродного скелета (С 5 Н 10 )
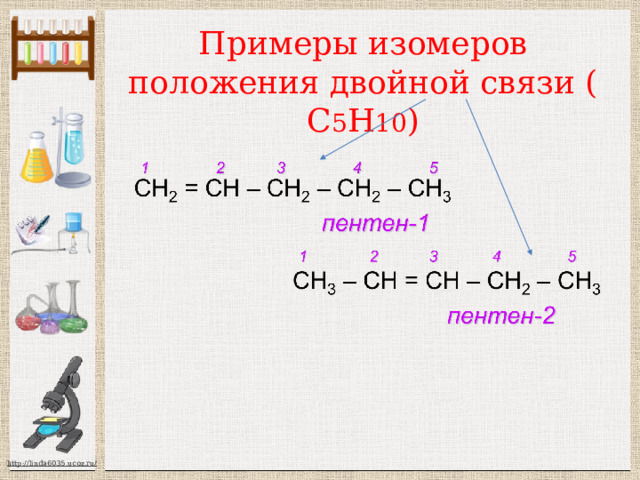
Примеры изомеров положения двойной связи ( С 5 Н 10 )
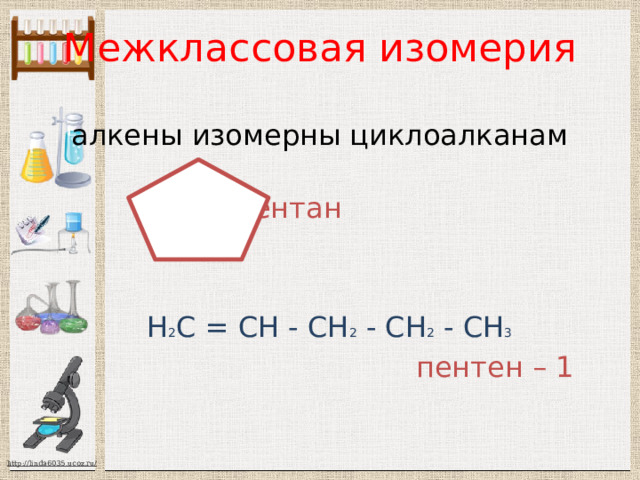
Межклассовая изомерия алкены изомерны циклоалканам
циклопентан
Н 2 С = СН - СН 2 - СН 2 - СН 3
пентен – 1
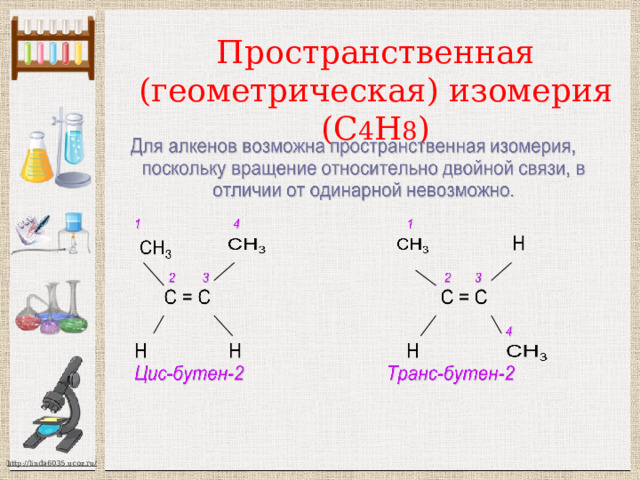
Пространственная (геометрическая) изомерия (С 4 Н 8 )
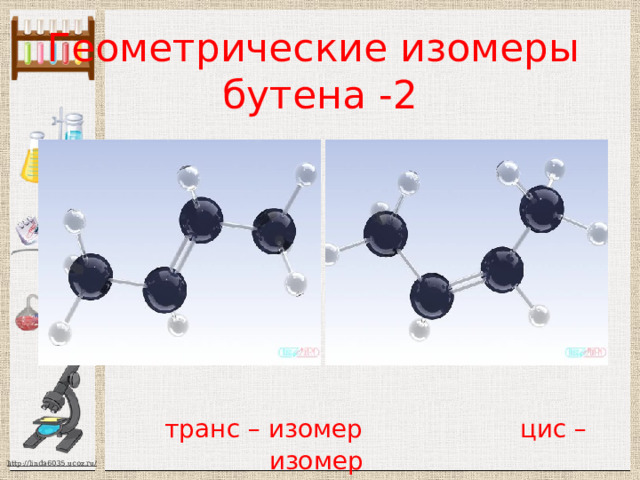
Геометрические изомеры бутена -2 транс – изомер цис – изомер

Получение алкенов
В природе алкены встречаются в меньшей степени, чем предельные углеводороды, вследствие своей высокой реакционной способности. Поскольку алкены являются ценным сырьем для промышленного органического синтеза, поэтому их получают с использованием различных реакций

Получение алкенов
- Дегидрирование алканов (отщепление водорода)

Получение алкенов
3. Гидрирование алкинов (присоединение молекулы водорода)
Ni, Pt
CH₃ - C C - CH₃ + H₂ CH₃ - CH = CH - CH₃

Получение алкенов
В лаборатории
Дегидратация спиртов (отщепление молекулы воды)
этанол

Физические свойства
- Алкены плохо растворимы в воде, но хорошо растворяются в органических растворителях
- С 17 … - твёрдые вещества
- С увеличением молекулярной массы алкенов, в гомологическом ряду, повышаются температуры кипения и плавления, увеличивается плотность веществ






























