Экзаменационная работа по химии для учащихся 8 класса
Вариант 1
1. Сколько электронов находится на внешнем уровне элемента с порядковым номером 13?
1) 3 2) 5 3) 8 4) 13
2. В ряду элементов B – C - N уменьшается:
1) электроотрицательность 2) заряд ядра
3) высшая степень окисления 4) радиус атома
3. Химическая связь в кристалле оксида кальция:
1) ковалентная неполярная 2) ковалентная полярная
3) металлическая 4) ионная
4. Положительную степень окисления атом кислорода имеет в соединении:
1) Н2О 2) Н2О2 3) F2O 4) Fe3O4
5. Сложным является каждое из двух веществ:
1) нитрат калия и хлор 2) белый фосфор и озон
3) гидроксид калия и аргон 4) угарный газ и аммиак
6. Водород массой 2 г полностью провзаимодействовал с 16 г кислорода. На основании закона сохранения массы можно утверждать, что масса полученной при этом воды равна:
1) 2 г 2) 16 г 3) 18 г 4) 14 г
7. Определите тип химической реакции: Fe + CuSO4 = Cu + FeSO4:
1) разложение 2) соединение 3) замещение 4) обмена
8. Правая часть уравнения электролитической диссоциации нитрата железа(II):
1)  2)
2) 
3)  4)
4) 
9. Взаимодействию хлорида железа(III) и гидроксида калия соответствует сокращённое ионное уравнение:
1)  2)
2) 
3)  4)
4) 
10. Оксид серы(IV) реагирует с:
1) сульфидом меди(II) 2) углеродом
3) кислородом 4) хлоридом железа(II)
11. С раствором карбоната калия реагирует:
1) HCl 2) KOH 3) Na2SO4 4) O2
12. Верны ли суждения о способах разделения смесей?
А. Очистить морскую воду от растворённых в ней солей можно с помощью фильтрования.
Б. Перегонка является химическим способом разделения смесей.
1) верно только А 2) верно только Б
3) верны оба суждения 4) оба суждения неверны
13. Установите соответствие между схемой химической реакции и изменением степени окисления окислителя в ней.
| СХЕМА РЕАКЦИИ | ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ ОКИСЛИТЕЛЯ |
| A) | 1) 0 → -1 |
| Б)  | 2) +1 → 0 |
| B) 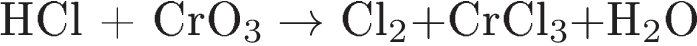 | 3) +2 → +3 |
|
| 4) +6 → +3 |
|
| 5) +7 → +2 |
14. На какой диаграмме распределение массовых долей элементов соответствует  ?
?

15. В ряду химических элементов N – O – F:
1) наибольший радиус имеют атомы азота
2) наибольшую электроотрицательность имеет кислород
3) увеличивается высшая степень окисления
4) увеличивается число электронов во внешнем электронном слое
5) уменьшается кислотность водородных соединений
16. При пропускании газа через трубку с раскалённой медью цвет порошка изменился с красного на чёрный. О каком газе идёт речь?
1) водород 2) кислород 3) аммиак 4) углекислый газ
17. Установите соответствие между названием вещества и реагентами, с которыми это вещество может взаимодействовать.
НАЗВАНИЕ ВЕЩЕСТВА РЕАГЕНТЫ
А) серная кислота 1) BaCl2, NaOH
Б) оксид натрия 2) HCl, SO2
В) хлорид алюминия 3) KOH, AgNO3
4) HNO3, Cu
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
18. Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой: 
Определите окислитель и восстановитель.
19. После пропускания через раствор гидроксида калия 4,48 л сернистого газа (н. у.) получили 252,8 г раствора сульфита калия. Вычислите массовую долю соли в полученном растворе.
20. Дана схема превращений:

Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Первое превращение рассмотрите с позиции ОВР. Для второго превращения составьте полное и сокращённое ионные уравнения реакций.


















