МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ
РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ
ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ
«СЕВЕРО-КАВКАЗСКАЯ ГОСУДАРСТВЕННАЯ АКАДЕМИЯ»
СРЕДНЕПРОФЕССИОНАЛЬНЫЙ КОЛЛЕДЖ
ИНДИВИДУАЛЬНЫЙ ПРОЕКТ
по учебной дисциплине «Физика»
На тему: «Изопроцессы и их графики. Газовые законы»
Автор индивидуального проекта
Преподователь физики Ижаева Ф.А. ________________
подпись
Черкесск, 2025
Содержание
Содержание 1
Определение и особенности изопроцессов 4
Изотермический процесс 6
Изобарный процесс 10
Изохорный процесс 13
Графическое представление газовых законов 17
Применение универсального газового закона 20
Проблемы обучения термодинамике 22
Заключение 24
Список литературы 27
Введение
Термодинамика, как раздел физики, изучает законы, управляющие тепловыми процессами и поведением веществ в различных состояниях. Важнейшей частью термодинамики является изучение газов, которые, благодаря своей простоте и универсальности, служат идеальными моделями для понимания более сложных систем. В рамках данной работы я сосредоточился на изопроцессах — термодинамических процессах, в которых один из макроскопических параметров газа остается постоянным. Это исследование имеет особую актуальность, поскольку понимание изопроцессов является ключевым для изучения термодинамики и позволяет глубже осознать поведение газов в различных условиях.
Изопроцессы делятся на три основных типа: изотермический, изобарный и изохорный. Каждый из этих процессов характеризуется уникальными условиями, которые влияют на поведение газа. Изотермический процесс происходит при постоянной температуре, что позволяет исследовать зависимость между давлением и объемом газа. Изобарный процесс, в свою очередь, осуществляется при постоянном давлении, что открывает возможности для анализа изменений температуры и объема. Изохорный процесс, где объем остается неизменным, позволяет изучать зависимость давления от температуры. Эти три типа изопроцессов образуют основу для понимания более сложных термодинамических явлений и законов.
Важным аспектом моего исследования станет графическое представление газовых законов, которые описывают поведение газов в рамках изопроцессов. Графики, иллюстрирующие зависимости между давлением, объемом и температурой, не только облегчают восприятие теоретических концепций, но и служат практическим инструментом для решения задач, связанных с термодинамикой. Я создам графики для каждого из типов изопроцессов, что позволит наглядно продемонстрировать их особенности и взаимосвязи.
Кроме того, в рамках работы будет рассмотрено применение универсального газового закона, который связывает давление, объем и температуру идеального газа. Этот закон является основополагающим в термодинамике и находит широкое применение в различных областях науки и техники. Я проанализирую, как универсальный газовый закон может быть использован для решения конкретных задач, что поможет закрепить теоретические знания на практике.
Однако, несмотря на важность термодинамики и изопроцессов, существует проблема недостатка представления о термодинамических процессах среди студентов и обучающихся. Это может быть связано с недостаточной наглядностью учебных материалов, а также с отсутствием практических примеров, которые могли бы помочь в усвоении теории. В моей работе я постараюсь не только осветить основные параметры изопроцессов, но и предложить решения для улучшения понимания термодинамических процессов в образовательном процессе.
Таким образом, данное исследование направлено на углубленное изучение изопроцессов и их графиков, а также на применение универсального газового закона в практических задачах. Я надеюсь, что результаты моей работы помогут не только в учебных целях, но и в дальнейшем развитии термодинамики как науки, способствуя более глубокому пониманию поведения газов и их свойств. В заключение, работа будет включать обсуждение проблем обучения термодинамике, что позволит выявить возможные пути улучшения образовательного процесса в этой области.
Определение и особенности изопроцессов
Изопроцессы представляют собой термодинамические процессы, в которых один из основных макроскопических параметров (давление, объем или температура) остаётся неизменным. Эти процессы довольно актуальны для термодинамики и физики, так как позволяют исследовать особенности поведения газов под различными условиями. Основными видами изопроцессов являются изобарный, изохорный и изотермический процессы.
Изобарный процесс, в котором давление остаётся постоянным (p = const), демонстрирует, как при увеличении объема газа его температура изменяется. Этот процесс иллюстрируется законом Гей-Люссака, который утверждает, что при постоянном давлении объём газа пропорционален его температуре в абсолютных единицах [1]. Это правило показывает, как количество молекул газа влияет на его состояние.
Изохорный процесс, в свою очередь, характеризуется постоянным объемом (V = const). В этих условиях изменение давления газа связано с температурой, согласно закону Шарля: при увеличении температуры отмечается рост давления [2]. Изохорные процессы важны, например, в биологических системах, где увеличение температуры может приводить к реакциям, происходящим при постоянном объёме.
Изотермический процесс (T = const) проходит при неизменной температуре, что связано с обеспечением энергии для выполнения работы. Закон Бойля-Мариотта, утверждающий, что при постоянной температуре произведение давления на объём газа остаётся постоянным, иллюстрирует поведение газа в этих условиях [3]. Это важно, особенно в термодинамических системах, где работа системы зависит от свойств исследуемого газа.
Каждый из названных изопроцессов основан на основных принципах термодинамики, где первый закон термодинамики применяется для анализа сохранения энергии в процессе. Эти процессы позволяют обеспечить понимание о том, как фиксированные параметры влияют на теплообмен и механическую работу в системах [4]. Необходимость изучения изопроцессов актуальна как в теоретической, так и в практической физике, поскольку они являются основой для понимания более сложных процессов.
Применение изопроцессов в нашей действительности можно встретить в различных технологических и естественных системах. Например, изобара может встречаться в процессе сжатия и расширения газов в двигателях [5]. Кроме того, знание о поведении газов в этих условиях помогает в разработке новых технологий и при оптимизации существующих процессов.
Разнообразие изопроцессов и их понимание создают прочный фундамент для дальнейшего изучения термодинамики и других физических явлений. Исследование этих процессов позволяет реализовать более глубокое понимание, как физические параметры взаимодействуют друг с другом, создавая условия для многопланового анализа и технологической реализации.
Изотермический процесс
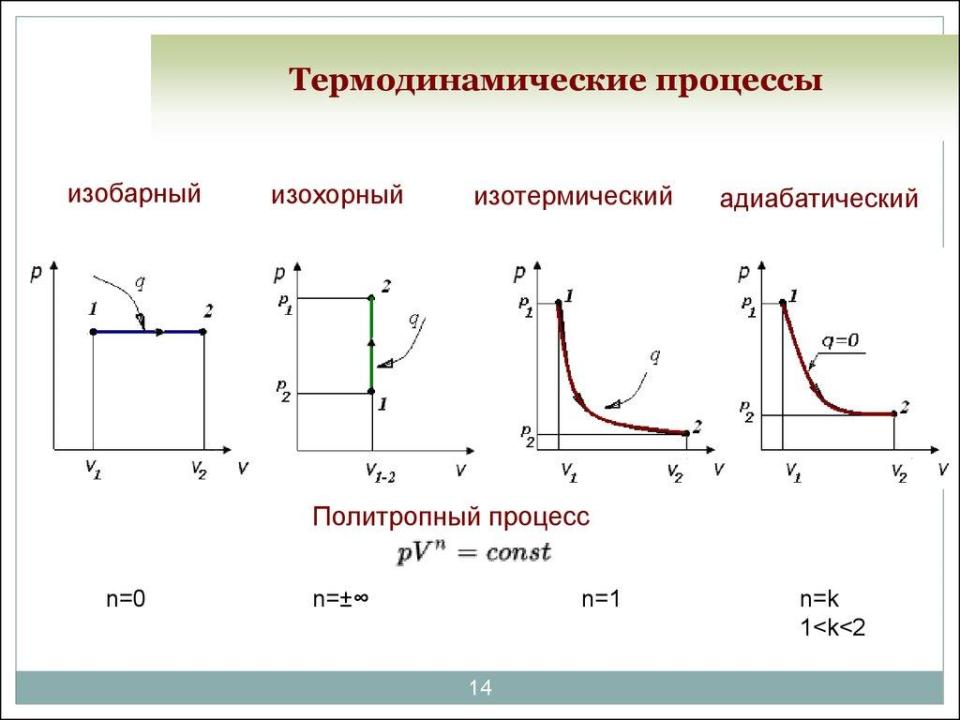 Рисунок 1. Графическое представление изотермического процесса и других изопроцессов
Рисунок 1. Графическое представление изотермического процесса и других изопроцессов
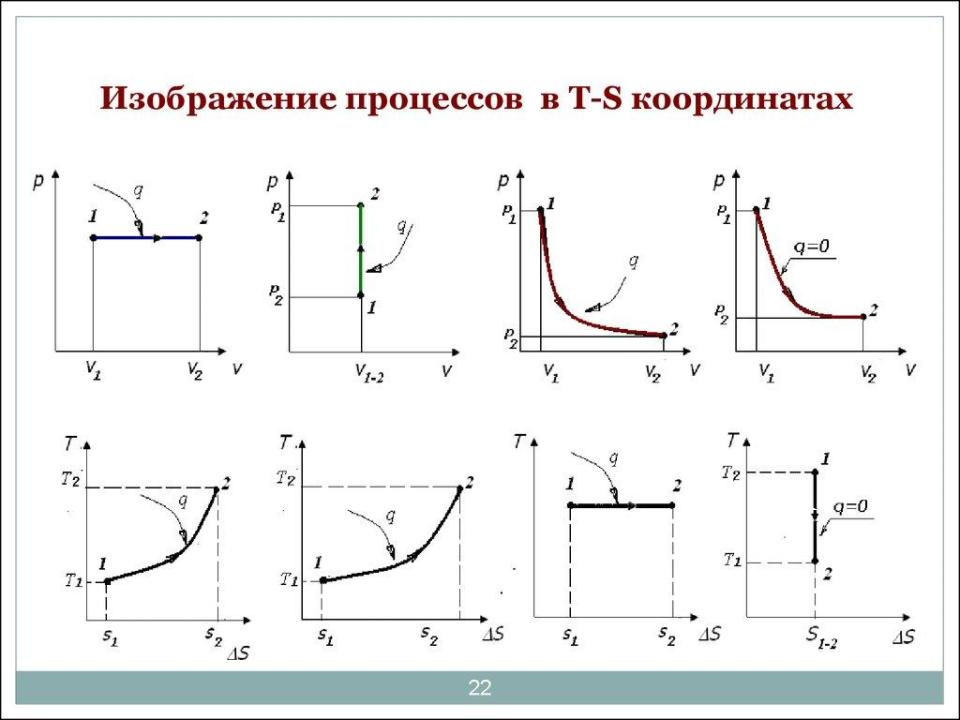 Рисунок 2. Графическое представление изотермического процесса и других изопроцессов
Рисунок 2. Графическое представление изотермического процесса и других изопроцессов
Изотермический процесс представляет собой один из важнейших типов термодинамических процессов, происходящих при постоянной температуре. В таких условиях, при изменении объема газа, наблюдается соответствующее изменение его давления, что может быть выразимо через уравнение состояния идеального газа PV = nRT, где P — давление, V — объем, n — количество вещества, R — универсальная газовая постоянная, а T — абсолютная температура [6].
Графически изотермические процессы изображаются на P-V диаграммах, где кривая, представляющая этот процесс, является гиперболой. Она указывает на взаимосвязь между давлением и объемом при фиксированной температуре. Разные температуры будут соответствовать различным гиперболическим линиям на графике, что является важным аспектом анализа изотермических процессов. Кривые, представляющие более высокие температуры, располагаются выше на графике, что отражает рост давления при увеличении температуры для фиксированного объема [7].
Одним из ключевых свойств изотермического процесса является работа, которую выполняет газ, что может быть рассчитано через интеграл по изменению объема. При этом работа газа в процессе сжатия или расширения может быть найдена по формуле, полученной из уравнений состояния. При изотермическом расширении работы будет больше, чем при сжатии, поскольку газ совершает работу против внешних сил [8].
Изменения давления и объема при постоянной температуре могут также быть проиллюстрированы с помощью различных практических примеров. Например, работу изотермического процесса можно наблюдать в процессе, когда газ нагревается и расширяется в цилиндре с поршнем. Чем больше объем, тем меньше давление, и наоборот, при фиксированной температуре. Это точно соответствует уравнению состояния идеального газа, которое служит основой для молекулярно-кинетической теории [9].
В термодинамике изотермический процесс часто служит моделью для объяснения других процессов. Например, в реальных приложениях, таких как холодильники или кондиционеры, процессы изотермического сжатия и расширения газа играют важную роль в их работе. Исследования показывают, что более глубокое понимание изотермических процессов помогает в оптимизации таких систем, приводя к повышению их эффективности [10].
Одним из важных аспектов, о котором стоит упомянуть, является то, что идеальные гипотетические процессы не всегда соответствуют реальному поведению газов. На практике, при проведении экспериментов можно наблюдать отклонение от идеального поведения из-за взаимодействия молекул и неидеальных условий. Тем не менее, модель идеального газа все равно является полезной для описания поведения газов вблизи комнатной температуры и давления [6].
Также стоит отметить, что для газов, отличающихся от идеального, изотермические процессы могут быть описаны с помощью различных уравнений состояния, которые учитывают взаимодействие молекул и силы, действующие на них. Подходы к описанию такого поведения варьируются, и их применение зависит от конкретных характеристик последующего газа [9].
Вклад изотермических процессов в термодинамику и молекулярную физику невозможно переоценить. Понимание их механизма важно не только для физиков, но и для специалистов, занимающихся инженерией, экологическими науками и множеством других областей. Оптимизация процессов охлаждения и нагрева, разработка новых мест хранения энергии, а также множество других приложений остаются активными областями исследований, которые опираются на принципы, вытекающие из анализа изотермических процессов. Таким образом, изучение и понимание этих процессов служат основой для многих практических приложений и теоретических исследований в области термодинамики и физики в целом [8].
Изобарный процесс
 Рисунок 3. Графическое представление изобарного процесса и его характеристики
Рисунок 3. Графическое представление изобарного процесса и его характеристики
Изобарный процесс характеризуется тем, что давление газа остается постоянным, тогда как его объем и температура могут меняться. В рамках этого процесса выполняется закон Бойля-Мариотта, который гласит, что при постоянной температуре и массе газа, произведение давления и объема остается постоянным. Однако, в случае изобарного процесса к ним добавляется и температурный аспект. Важно отметить, что данный процесс нередко рассматривается в термодинамике и используется для анализа разнообразных газовых систем.
Что касается графического представления, изобарный процесс часто отображается на диаграмме, где по одной оси откладывается объем, а по другой - температура или давление. Линия, соединяющая точки в диаграмме, будет горизонтальной, то есть будет отражать постоянное значение давления. В таком графике можно увидеть, как объем газа изменяется в ответ на изменение температуры, поддерживая постоянное давление [6]. Это удобно для понимания процессов, происходящих с газами при нагреве или охлаждении.
В процессе изобарной смены состояния происходит выполнение первого закона термодинамики. Этот закон может быть выражен как изменение внутренней энергии системы, равное работе, совершенной системой, плюс теплота, полученная или отданная системой. В этом контексте работа, выполненная газом, фиксируется и вычисляется как произведение давления на изменение объема. При увеличении температуры газа его объем также увеличивается, что подтверждает термодинамические релевантные описания процессов [12].
Изобарные процессы также могут наблюдаться в реальных условиях, например, в атмосфере, где давление остается статичным в течение определенного времени. При анализе этих процессов в идеальных газах используется уравнение состояния, которое связывает давление, объем и температуру. Это уравнение помогает предсказать поведение газа в различных условиях и показывает, как изменение температуры влияет на объем при постоянном давлении [11]. Применение этих базовых принципов позволяет проводить сравнительные исследования и практические эксперименты в классической механике и термодинамике.
Еще одной важной особенностью изобарного процесса является то, что работа, совершаемая газом, является максимальной, если система достаточно медленно расширяется. Это связано с тем, что при медленной компрессии или расширении возможен обмен теплом с окружающей средой, что позволяет эффективно поддерживать постоянное давление [10]. А в случае быстрого расширения газа, работа будет минимальной, так как система не успевает обменяться теплом с окружающей средой.
Знание о том, как происходит изобарный процесс, позволяет применять эти принципы в инженерных сферах, например, в тепловых машинах или холодильных системах. В данных устройствах управление давлением и температурой газа критично для их корректной работы; именно поэтому понимание, как физические законы действуют в рамках изобарного процесса, открывает путь для дальнейших разработок [12].
В заключение можно отметить, что изобарный процесс — важный компонент изучения термодинамики, который проявляется в практике. Он помогает объяснить многие физические явления, что делает его незаменимым в образовательных программах по физике и инженерии.
Изохорный процесс
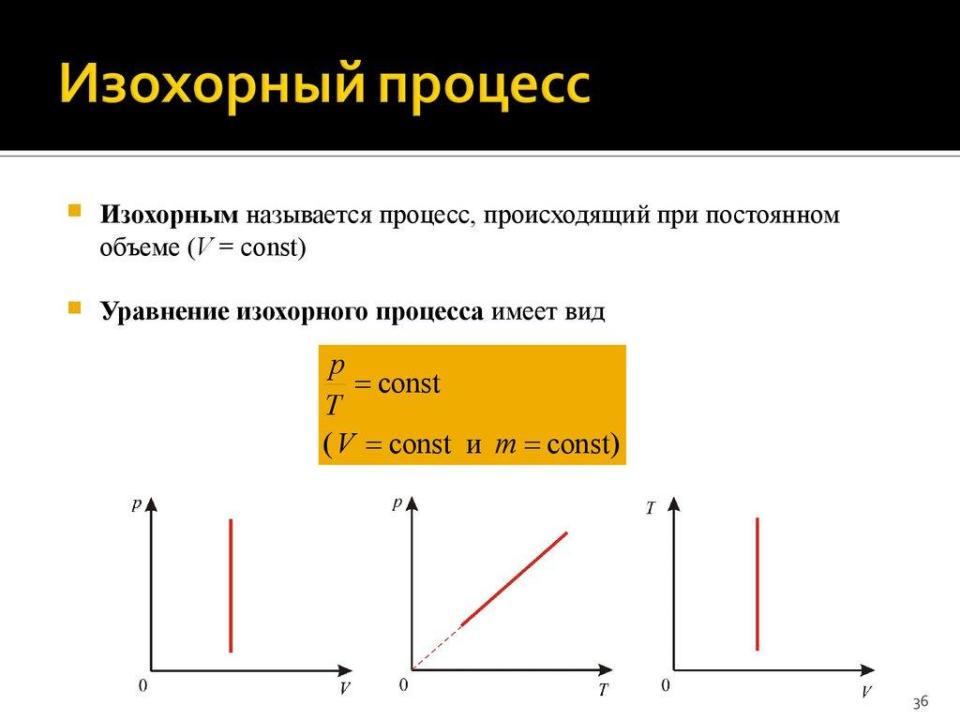 Рисунок 4. Графики и условия изохорного процесса
Рисунок 4. Графики и условия изохорного процесса
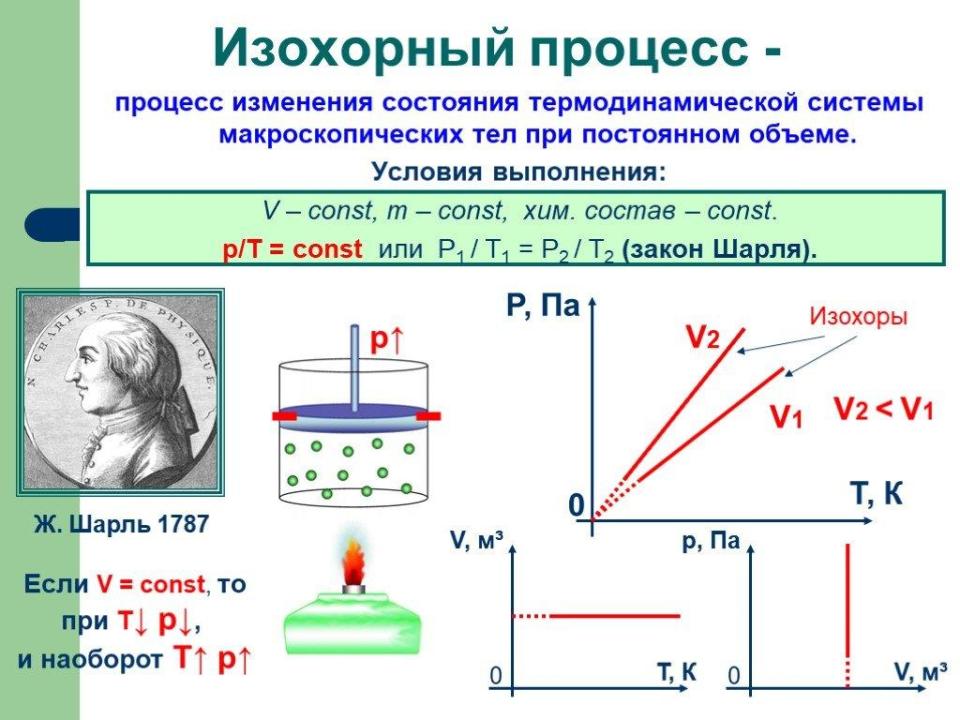 Рисунок 5. Графики и условия изохорного процесса
Рисунок 5. Графики и условия изохорного процесса
Изохорный процесс характеризуется изменением температуры и давления газа при фиксированном объеме. В таких условиях работа газа не совершается, что следует из определения работы в термодинамике, так как работа представляет собой результат изменения объема. Если объем газа остается постоянным, то работа равна нулю. Этот процесс описывается уравнением состояния идеального газа, где температура и давление связаны через объем, который в данном случае остаётся неизменным [13].
В процессе изохорного сжатия и расширения газа, его температура изменяется в зависимости от изменения давления. Это может быть представлено уравнением состояния идеального газа PV = nRT, где P - давление, V - объем, n - количество вещества, R – универсальная газовая постоянная и T – температура в кельвинах. При фиксированном V, если давление увеличивается, температура также должна увеличиваться, и наоборот. Это явление можно легко продемонстрировать в лабораторных условиях, используя простое оборудование, такое как манометр и термометр [14].
На графиках изохорного процесса обычно изображают зависимость давления от температуры. Эта зависимость будет линейной, поскольку по мере увеличения температуры будет происходить пропорциональный рост давления. Для идеального газа отношение P/T будет постоянным при фиксированном объеме, что также легко вывести из термодинамических уравнений. Таким образом, каждое значение давления соответствует определённой температуре [6].
Обратим внимание на различные виды процессов, происходящие в условиях постоянного объема. При резком нагреве газа может произойти стремительный рост давления, что может привести к его разрушению, если сосуд, содержащий газ, не сможет этого выдержать. Это критически важно учитывать при проектировании и эксплуатации газовых систем, например, в промышленных установках или при использовании газовых баллонов [13].
Изохорные процессы также можно наблюдать в естественных явлениях. Например, когда литиевая батарея (в которой также содержатся газы) нагревается, происходит изменение давления, что обусловлено повышением температуры. В этом случае важно следить за безопасностью, так как высокое давление может вызвать разрыв батареи [7].
Теоретически изохорный процесс можно провести и в более сложных условиях, например, в системах, где происходят химические реакции. В таких случаях изменение температуры и давления может быть вызвано не только физическими, но и химическими процессами. Это показывает, как разнообразны и многогранны могут быть изохорные явления, от простых моделей до сложных систем, где соприкасаются механика и термодинамика [14].
Графически этот процесс хорошо иллюстрируется. Например, в зависимости от туда, куда направлена ось Y (давление) и ось X (температура), точки, соответствующие состояниям газа, формируют прямую линию, показывая линейную зависимость по законам Бойля-Мариотта и Гей-Люссака [6]. Эти графики могут использоваться для аналитической работы и в образовательных целях, позволяя нам и исследователям визуально осваивать принципы термодинамики.
Очевидно, что понимание изохорного процесса — это следствие необходимости в различных науках, таких как инженерия, физика и химия. Знание о термодинамических процессах позволяет создавать более эффективные машинные механизмы, разрабатывать новые технологии хранения и использования энергии, а также повышать безопасность многообразных систем [7].
Таким образом, изучение изохорных процессов, включая их предсказание и управление, имеет значение не только в традиционных системах, но и в инновационных приложениях, связанных с возобновляемыми источниками энергии и новыми материалами. В конечном итоге, это может открывать возможности для развития новых технологий и улучшения существующих систем, что особенно важно в контексте современных вызовов и угроз.
Графическое представление газовых законов
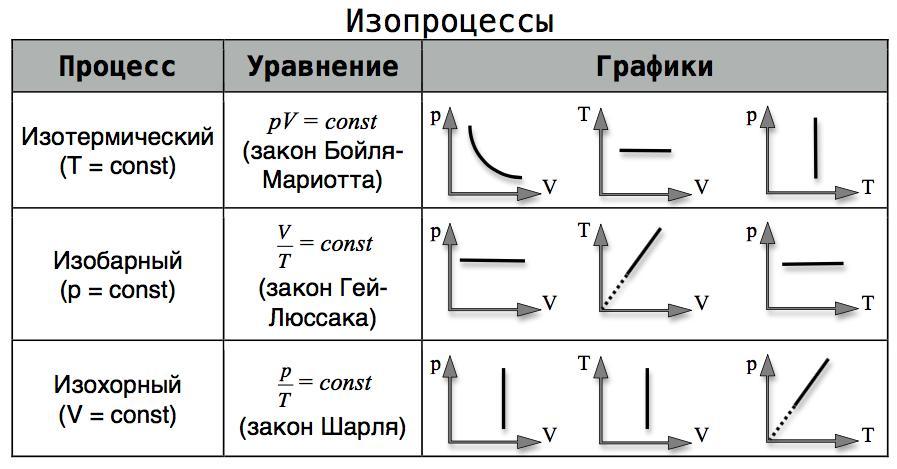 Рисунок 6. Графическое представление изопроцессов: изотермический, изобарный и изохорный процессы
Рисунок 6. Графическое представление изопроцессов: изотермический, изобарный и изохорный процессы
Для изучения газовых законов и их графического представления важно понимать, как различные процессы связаны друг с другом, а также как они визуализируются в виде графиков. Основными из них являются изотермические, изобарные и изохорные процессы, каждый из которых имеет свои уникальные характеристики и графические представления.
Изотермический процесс осуществляется при постоянной температуре. В этом случае график зависимости давления от объема (p-V) принимает форму гиперболы, что иллюстрирует закон Бойля-Мариотта, согласно которому pV = const. График показывает, что, увеличивая объем, давление газа уменьшается, и наоборот. Каждый уровень температуры соответствует своей гиперболе; при повышении температуры гиперболы смещаются вверх [6]. Объяснение этого эффекта заключается в том, что при высокой температуре молекулы газа обладают большей энергией, в результате чего давление увеличивается при увеличении температуры.
Изобарный процесс проходит при постоянном давлении. В этом случае зависимость объема от температуры представляется прямой линией на графике V-T. При постоянном давлении увеличение температуры ведет к росту объема, что описывается законом Гей-Люссака (p = const). При построении графика p-V, линии будут горизонтальными, указывая на то, что давление остается постоянным [15]. Это упрощает понимание того, как газ ведет себя в закрытой системе при изменении температуры, и является важной основой для дальнейшего изучения газовых процессов.
Изохорный процесс, происходящий при постоянном объеме, отображается на графиках как вертикальная линия на p-V координатах. Здесь, несмотря на изменение давления с изменением температуры (закон Шарля), объем остается неизменным, что дает возможность четко увидеть, как давление возрастает при увеличении температуры [16]. Этот процесс подчеркивает важность понимания физических свойств газов, так как даже незначительные изменения в температуре могут привести к резким колебаниям давления.
Объединение этих трех процессов формирует универсальный газовый закон, который позволяет описывать состояние идеального газа в едином уравнении. Это уравнение, pV = nRT, связывает давление, объем, количество вещества и температуру. Графически это уравнение может быть представлено на различных координатах, таким образом демонстрируя, как изменяются свойства газа под различными условиями [17].
Понимание графиков изопроцессов сильнейшим образом обогатит представление о термодинамических процессах. Каждый из них помогает запечатлеть взаимосвязь между температурой, давлением и объемом, делая изучение двигательной силы газов более наглядным и понятным.
Таким образом, графическое представление газовых закономерностей служит мощным инструментом для визуализации процессов и исследования их взаимосвязей, что весьма актуально для образовательных и исследовательских целей в области термодинамики и молекулярно-кинетической теории [18].
Применение универсального газового закона
Применение универсального газового закона в термодинамике позволяет систематизировать знания о поведении идеальных газов, так как этот закон объединяет результаты всех основных газовых законов — Бойля, Шарля и закон Авогадро. Связь между давлением, объемом и температурой газа описывается уравнением состояния, что является основополагающим для решения практических задач в термодинамике [19].
В термодинамических процессах, таких как изотермический, изобарный и изохорный, данный закон помогает понимать, как газ реагирует на изменения внешних условий. Например, при постоянной температуре (изотермический процесс) для идеального газа при увеличении объёма происходит уменьшение давления. В таких случаях уравнение состояния PV=nRT позволяет точно производить расчеты, а понимание этого процесса критично для многих инженерных приложений [20].
В случае изучения смесей газов использование универсального газового закона становится значительно более сложным, однако этот подход все еще действенен. Вместо того чтобы применять уравнение к смеси в целом, его можно адаптировать для каждого компонента газовой смеси отдельно. Это позволяет более точно определить свойства смеси, такие как среднее давление, молекулярная масса и плотность [21]. В частности, закон Дальтона оPartial pressures может быть применен для расчета общего давления смеси газов, что играет важную роль в химических реакциях, где необходимо учитывать индивидуальные поведения компонентов.
Решение задач на применение газовых законов также обогащает практические навыки в области термодинамики. Примеры, которые требуются для решения, могут варьироваться от простейших, где необходимо рассчитать объем, давление или температуру, до более сложных, включающих многократные переходы в различных термодинамических состояниях [22]. Четкое понимание того, как каждый из этих процессов влияет на систему, помогает инженерам и ученым предсказывать поведение газов в разных условиях.
Практические занятия, где рассматриваются реальные примеры, демонстрируют, как результаты анализа идеального газа можно применить для укладки теории на практике. Например, в задачах, где газ проходит через несколько изолированных процессов, каждый этап анализируется с использованием уравнения состояния и других термодинамических законов, что обеспечивает глубокое понимание проблематики [23].
Исходя из вышесказанного, важно отметить, что работу с идеальными газами не следует ограничивать лишь расчетом параметров, но также необходимо уделять внимание интерпретации результатов. Например, при расширении газа следовало бы рассмотреть, как это расширение повлияло на его температуру и давление в зависимости от температуры окружающей среды и других факторов. Понимание этих взаимосвязей и тонкостей дает возможность избежать распространенных ошибок при моделировании термодинамических процессов в реальной жизни, обеспечивая более точные предсказания и контроль над системами, использующими газы как рабочие тела.
Таким образом, применение универсального газового закона становится основой для дальнейшего изучения термодинамических систем. Это не только помогает в решении актуальных задач, но и служит основой для более глубокого понимания воздушной динамики и кинетического молекулярного движения. Каждый этап термодинамического процесса требует внимательного анализа, и, следовательно, применение универсального газового закона становится обязательным навыком для специалистов в областях физики и инженерии.
Проблемы обучения термодинамике
Обучение термодинамике, особенно в контексте высшего образования, сталкивается с рядом сложностей. Представление о термодинамических процессах и газовых законах требует не только теоретческих знаний, но и способности применять эти знания на практике. Мужество и терпение нужны, чтобы преодолеть барьеры влияния предвзятостей в восприятии данных понятий. Основные тенденции и методические подходы к обучению термодинамике могут значительно улучшить восприятие предмета и мотивировать нас.
Проблемное обучение занимает центральное место в современных методиках. Мы должны активно участвовать в процессе освоения, разбирая не только саму термодинамику, но и критикуя свои прежние представления и ошибки. Этот подход активно демонстрирует, как важна не только поверхность темы, но и глубинные связи между её компонентами [24]. Это позволит обеспечить более качественное понимание термодинамических явлений.
Практические кейсы и активные методы обучения получают все большее признание. Они позволяют применять теоретические знания в реальных ситуациях. Например, использование задач из инженерной практики в рамках школьной программы может повысить интерес к изучению термодинамики. Эта методика связывает абстрактные концепции с конкретными примерами, показывая, как термодинамика применяется в реальной жизни [25].
Необходимость обновления учебных программ также не может быть недооценена. В условиях, когда важность термодинамики как научной дисциплины возрастает, актуально адаптировать содержание курсов к современным требованиям и технологиям. Постоянное развитие научной базы в этой области идет рука об руку с необходимостью модернизации образовательных программ, чтобы они отвечали современным вызовам [26].
Учебные методики, базирующиеся на научном подходе, тоже находят свое заслуженное место в обучении термодинамике. Они включают в себя использование экспериментальной базы и современные научные исследования, которые привносят новые знания в образовательный процесс. Такой подход может укрепить способности к критическому мышлению и анализу данных [27].
Среди существующих проблем можно выделить также необходимость профилактики стереотипов, связанных с термодинамикой, которые существуют у нас. Адаптация программ к интересам и пониманию стала важным фактором в преподавании. Способы, углубляющие понимание термодинамики как науки, раскрывают перед нами не только теоретические аспекты, но и практическое применение знаний в реальном мире [28].
Важное значение имеет и создание учебного пространства, где можно реализовать вышеупомянутые методы. Это может быть как лаборатория, так и виртуальная платформа, где мы можем экспериментировать с термодинамическими процессами, в том числе делать графические построения, видеть изменения состояния газа и понимать законы, описывающие эти изменения.
В заключение, методы преподавания термодинамики трансформируются с учетом новых требований времени и стремления адаптировать учебный процесс под наши нужды. Образовательный процесс становится более интерактивным и ориентированным на практическое применение знаний, что в свою очередь, позволяет создать более положительный опыт для изучения такой сложной темы как термодинамика.
Заключение
В заключение моего исследования, посвященного изопроцессам и их графикам, а также газовым законам, можно сделать несколько важных выводов, которые подчеркивают значимость изучения термодинамических процессов для понимания поведения газов. В ходе работы мною рассмотрены основные параметры изопроцессов, такие как температура, давление и объем, и проанализировали три ключевых типа изопроцессов: изотермический, изобарный и изохорный. Каждый из этих процессов имеет свои уникальные характеристики и закономерности, которые играют важную роль в термодинамике.
Изотермический процесс, в котором температура газа остается постоянной, демонстрирует, как изменение объема газа влияет на его давление. Этот процесс можно проиллюстрировать графически с помощью изотермических кривых, которые показывают обратную зависимость между давлением и объемом. Изучение изотермического процесса позволяет лучше понять, как газы ведут себя при постоянной температуре, что имеет практическое значение в различных областях, таких как холодильная техника и климат-контроль.
Изобарный процесс, в свою очередь, характеризуется постоянным давлением. В этом случае изменение объема газа происходит с изменением температуры. Графическое представление изобарного процесса позволяет увидеть, как при увеличении температуры объем газа также увеличивается, что иллюстрирует закон Бойля-Мариотта. Понимание изобарного процесса имеет важное значение для таких приложений, как работа поршневых двигателей и других систем, где давление играет ключевую роль.
Изохорный процесс, в котором объем газа остается постоянным, демонстрирует, как изменение температуры влияет на давление. Графики, представляющие изохорный процесс, показывают прямую зависимость между давлением и температурой, что соответствует закону Гей-Люссака. Этот процесс важен для понимания поведения газов в замкнутых системах, таких как баллоны и контейнеры, где объем не может изменяться.
Создание графиков для каждого из типов изопроцессов не только иллюстрирует теоретические аспекты, но и служит практическим инструментом для решения задач, связанных с термодинамикой. Графическое представление позволяет визуализировать зависимости между переменными параметрами, что облегчает понимание сложных процессов и способствует более глубокому усвоению материала.
Применение универсального газового закона, который связывает давление, объем и температуру идеального газа, является важным аспектом нашего исследования. Этот закон служит основой для анализа различных термодинамических процессов и позволяет решать практические задачи, связанные с поведением газов в различных условиях. Понимание универсального газового закона и его применения в реальных ситуациях помогает студентам и специалистам в области физики и инженерии более эффективно работать с газами и разрабатывать новые технологии.
Однако, несмотря на важность изучения термодинамических процессов, существует ряд проблем, связанных с обучением термодинамике. Мы сталкиваемся с трудностями в понимании абстрактных концепций и математических моделей, что может привести к недостаточному усвоению материала. Поэтому важно разрабатывать новые методы обучения, которые помогут сделать термодинамику более доступной и понятной. Использование интерактивных графиков, компьютерных симуляций и практических экспериментов может значительно улучшить процесс обучения и повысить интерес к данной области.
В заключение, моё исследование изопроцессов и газовых законов подчеркивает их значимость для понимания поведения газов и их применения в различных областях науки и техники. Глубокое понимание этих процессов не только обогащает теоретические знания, но и открывает новые горизонты для практического применения в реальной жизни. Надеюсь, что результаты моего проекта будут полезны как для студентов, так и для преподавателей, способствуя более глубокому пониманию термодинамики и ее роли в современном мире.
Список литературы
1. Изопроцессы — Википедия [Электронный ресурс] // ru.wikipedia.org - Режим доступа: https://ru.wikipedia.org/wiki/изопроцессы, свободный. - Загл. с экрана
2. Первый закон термодинамики для изопроцессов – применение... [Электронный ресурс] // obrazovaka.ru - Режим доступа: https://obrazovaka.ru/fizika/pervyy-zakon-termodinamiki-dlya-izoprocessov-primenenie.html, свободный. - Загл. с экрана
3. Газовые законы. Изопроцессы 10 класс онлайн-подготовка на... [Электронный ресурс] // lc.rt.ru - Режим доступа: https://lc.rt.ru/classbook/fizika-10-klass/osnovy-molekulyarno-kineticheskoi-teorii/6169, свободный. - Загл. с экрана
4. Закон термодинамики для изопроцессов [Электронный ресурс] // spravochnick.ru - Режим доступа: https://spravochnick.ru/fizika/termodinamika/zakon_termodinamiki_dlya_izoprocessov/, свободный. - Загл. с экрана
5. Изопроцессы - материалы для подготовки к ЕГЭ по Физике [Электронный ресурс] // ege-study.ru - Режим доступа: https://ege-study.ru/ru/ege/materialy/fizika/izoprocessy/, свободный. - Загл. с экрана
6. Графики изопроцессов 10 класс онлайн-подготовка на Ростелеком... [Электронный ресурс] // lc.rt.ru - Режим доступа: https://lc.rt.ru/classbook/fizika-10-klass/osnovy-molekulyarno-kineticheskoi-teorii/6163, свободный. - Загл. с экрана
7. Изопроцессы [Электронный ресурс] // mathus.ru - Режим доступа: https://mathus.ru/phys/isoprocesses.pdf, свободный. - Загл. с экрана
8. ЛЕКЦИЯ 4 [Электронный ресурс] // moodle.kstu.ru - Режим доступа: https://moodle.kstu.ru/pluginfile.php/269830/mod_resource/content/1/лекция 4. основные термодинамические процессы.pdf, свободный. - Загл. с экрана
9. Изотермический процесс [Электронный ресурс] // spravochnick.ru - Режим доступа: https://spravochnick.ru/fizika/molekulyarnaya_fizika/izotermicheskiy_process/, свободный. - Загл. с экрана
10. Изопроцессы в идеальном газе [Электронный ресурс] // foxford.ru - Режим доступа: https://foxford.ru/wiki/fizika/izoprocessy, свободный. - Загл. с экрана
11. Изопроцессы в идеальных газах [Электронный ресурс] // internat.msu.ru - Режим доступа: https://internat.msu.ru/media/uploads/2015/08/izoprotsessy.pdf, свободный. - Загл. с экрана
12. Изобарный процесс | GeeksforGeeks [Электронный ресурс] // tr-page.yandex.ru - Режим доступа: https://tr-page.yandex.ru/translate?lang=en-ru&url=https://www.geeksforgeeks.org/isobaric-process/, свободный. - Загл. с экрана
13. Картинки по запросу "изохорный процесс термодинамика графики" [Электронный ресурс] // yandex.ru - Режим доступа: https://yandex.ru/images/search?text=изохорный процесс термодинамика графики, свободный. - Загл. с экрана
14. Изохорный процесс — Википедия [Электронный ресурс] // ru.wikipedia.org - Режим доступа: https://ru.wikipedia.org/wiki/изохорный_процесс, свободный. - Загл. с экрана
15. Графики газовых процессов • Физика, Молекулярно-кинетическая... [Электронный ресурс] // foxford.ru - Режим доступа: https://foxford.ru/wiki/fizika/grafiki-gazovyh-protsessov, свободный. - Загл. с экрана
16. Графическое представление газовых законов - презентация... [Электронный ресурс] // ppt-online.org - Режим доступа: https://ppt-online.org/840002, свободный. - Загл. с экрана
17. Репетитор-онлайн — подготовка к ЦТ [Электронный ресурс] // vedy.by - Режим доступа: https://vedy.by/vedy/home/partitionview/16888, свободный. - Загл. с экрана
18. Физика. МКТ: Графики газовых процессов. - YouTube [Электронный ресурс] // www.youtube.com - Режим доступа: https://www.youtube.com/watch?v=piklptzj1sk, свободный. - Загл. с экрана
19. задачи на газовые законы | Методическая разработка по физике... [Электронный ресурс] // nsportal.ru - Режим доступа: https://nsportal.ru/shkola/fizika/library/2015/02/08/zadachi-na-gazovye-zakony, свободный. - Загл. с экрана
20. Первое начало термодинамики —Каталог задач по... — Школково [Электронный ресурс] // 3.shkolkovo.online - Режим доступа: https://3.shkolkovo.online/catalog/1708?subjectid=4?subjectid=4, свободный. - Загл. с экрана
21. Задачи на первый закон термодинамики [Электронный ресурс] // kornev-school.ru - Режим доступа: https://kornev-school.ru/f10_first_law_of_thermodynamics.html, свободный. - Загл. с экрана
22. ТЕРМОДИНАМИКА [Электронный ресурс] // lib.kgeu.ru - Режим доступа: https://lib.kgeu.ru/irbis64r_15/scan-new/3563.pdf, свободный. - Загл. с экрана
23. Решение задач с использованием газовых законов... [Электронный ресурс] // k-a-t.ru - Режим доступа: https://k-a-t.ru/teplotexnika/2_gaz_zakony_zadachi/index.shtml, свободный. - Загл. с экрана
24. Соколов Юрий Николаевич Методика преподавания технической термодинамики // Известия Томского политехнического университета. Инжиниринг георесурсов. 1937. №7. URL: https://cyberleninka.ru/article/n/metodika-prepodavaniya-tehnicheskoy-termodinamiki (03.03.2025).
25. Особенности изучения и преподавания раздела... [Электронный ресурс] // expeducation.ru - Режим доступа: https://expeducation.ru/article/view?id=12176, свободный. - Загл. с экрана
26. Михайловская военная артиллерийская академия, г. Санкт... [Электронный ресурс] // libeldoc.bsuir.by - Режим доступа: https://libeldoc.bsuir.by/bitstream/123456789/53493/1/ustinov_problemi.pdf, свободный. - Загл. с экрана
27. Диссертация на тему «Обучение термодинамике студентов...» [Электронный ресурс] // www.dissercat.com - Режим доступа: https://www.dissercat.com/content/obuchenie-termodinamike-studentov-tekhnicheskogo-vuza-na-osnove-metodov-nauchnogo-poznaniya, свободный. - Загл. с экрана
28. Подходы, ориентированные на студентов, в преподавании... [Электронный ресурс] // tr-page.yandex.ru - Режим доступа: https://tr-page.yandex.ru/translate?lang=en-ru&url=https://pubs.rsc.org/en/content/articlehtml/2016/rp/c6rp00049e, свободный. - Загл. с экрана
1







 Рисунок 1. Графическое представление изотермического процесса и других изопроцессов
Рисунок 1. Графическое представление изотермического процесса и других изопроцессов Рисунок 2. Графическое представление изотермического процесса и других изопроцессов
Рисунок 2. Графическое представление изотермического процесса и других изопроцессов Рисунок 3. Графическое представление изобарного процесса и его характеристики
Рисунок 3. Графическое представление изобарного процесса и его характеристики Рисунок 4. Графики и условия изохорного процесса
Рисунок 4. Графики и условия изохорного процесса Рисунок 5. Графики и условия изохорного процесса
Рисунок 5. Графики и условия изохорного процесса Рисунок 6. Графическое представление изопроцессов: изотермический, изобарный и изохорный процессы
Рисунок 6. Графическое представление изопроцессов: изотермический, изобарный и изохорный процессы









