
“ Химия – это гениальная наука, так как во-первых, охватывает и объединяет широкие области знания,
и во-вторых, развивает у человека способность к резким скачкам мысли…” (Чугуев Л.А.)

Разминка
- 1. В составе кока-колы присутствует данное вещество. Популярный напиток широко применяется для очистки канализации, заржавевших болтов.

Разминка
- 2. Это вещество, выделяемое муравьями в момент опасности, служит сигналом для всех остальных особей этого вида и является средством защиты при нападении хищников.

Разминка
- 3. С древнейших времен люди разводили виноград и запасали впрок виноградный сок.
- При хранении в сосудах сок бродил, получалось вино. Иногда вино скисало и превращалось в уксус.
- Впоследствии его научились использовать как лекарство, приправу к пище, растворитель красок.
- О чем речь?

ТЕМА УРОКА «СВОЙСТВА КАРБОНОВЫХ КИСЛОТ»

Цель урока:
- Сформировать комплекс знаний о свойствах карбоновых кислот, как представителей класса кислородсодержащих органических соединений.

План изучения темы:
1.Определение карбоновых кислот.
2.Общая формула карбоновых кислот.
3.Классификация карбоновых кислот.
4. Номенклатура карбоновых кислот.
5. Физические свойства карбоновых кислот.
6.Электролиты и неэлектролиты.
7. Химические свойства карбоновых кислот.
8.Кислоты в топливе.
9.Применение карбоновых кислот.

«От кислых яблок сразу кисну!»

1.Карбоновые кислоты-вещества, содержащие группу СООН .
- -СООН – карбоксильная группа
А. R -СООН
Б. С n H 2n+1 COOH
В. С n H 2n O 2

Формулы кислот:
- НСООН – метановая (муравьиная)
- СН 3 - СООН – этановая (уксусная)
- С 2 Н 5 - СООН – пропановая (пропионовая)
- С 3 Н 7 – СООН – бутановая (масляная)
- С 4 Н 9 – СООН – пентановая (валериановая)
- С 5 Н 11 - СООН – гексановая (капроновая)




3.Классификация карбоновых кислот
3.Классификация карбоновых кислот

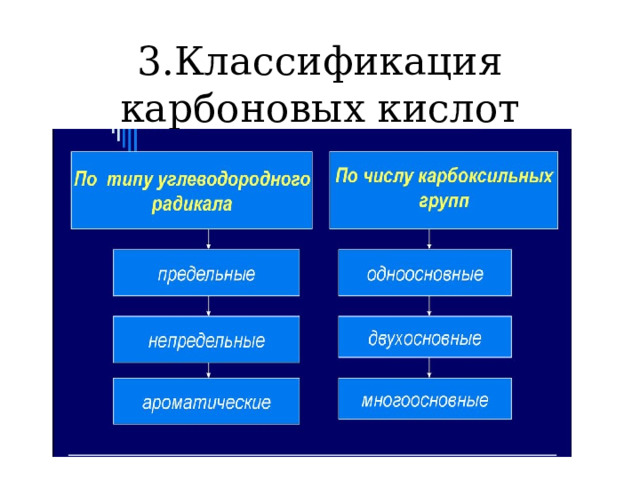
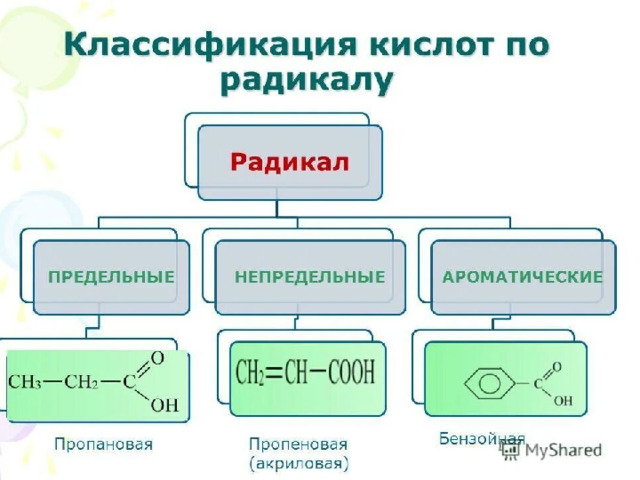
3.Классификация карбоновых кислот
1 . Предельные :уксусная,
муравьиная.
2 . Непредельная :акриловая, линоленовая.
3 . Ароматическая :бензойная, фенилуксусная..
1 . Одноосновные :муравьиная.
2 . Двухосновная : щавелевая.
3 . Многоосновные :аконитовая, янтарная.

Путешествие по станциям:
- 1.Станция Номенклатура
- 2.Станция Физическая
- 3.Станция Электролитическая
- 4.Станция Химическая
- 5.Станция Профессиональная

1.Станция Номенклатура
- Опишите алгоритм международной номенклатуры карбоновых кислот, дополнив схему последовательности действий:
- Нумеруем атомы______________, начиная с атома углерода ___________________ группы СООН.
- Если есть в молекуле радикал, то указываем его ____________________ .
- Расставляем атомы водорода Н.
- Называем кислоту.
- И по названию можно составить структурную формулу.
- Задание: Составьте структурные формулы веществ (работа в группах)

2.Станция Физическая
- Прочитайте текст и изучите свойства кислоты по плану:
- 1) Определите агрегатное состояние вещества при н. у.
- 2) Изучите цвет вещества и его прозрачность
- 3) Определите наличие запаха .
- 4) Определите растворимость кислоты в воде
- 5)Найдите температуру кипения
- Опишите результаты исследования:
1.Формула
2. Агрегатное состояние
3.Цвет
4.Запах
5.Растворимость в воде
6.Температура кипения
7.Название солей
- 1. Уксусная кислота
- 2.Муравьиная
- 3.Лимонная
- 4.Щавелевая
- 5.Аскорбиновая
- 6.Ацетилсалициловая

1.Уксусная кислота
- Уксусная кислота одноосновная без заместителей в радикале и двумя атомами углерода в молекуле.
- Как только не называли эту кислоту: «кислой влажностью», «древесной кислотой», так как долгое время ее получали из древесины.
- Она имеет широкий спектр применения – растворитель лекарств и душистых веществ, реагент в химическом синтезе. Но сейчас, как и три тысячи лет назад, уксусная кислота – один из важнейших консервантов в пищевой промышленности.

Уксусная кислота

2.Муравьиная кислота
- Муравьиная кислота в 10 раз сильнее, чем уксусная кислота за счет самого маленького углеводородного радикала.
- Муравьиная кислота содержится не только в железах муравьев, но и в волосках крапивы.
- Данная кислота обладает бактерицидными свойствами, поэтому ее применяют, как консервант. Народная медицина традиционно использовала муравьиную кислоту для лечения ревматических болей и радикулитов, а пчеловоды ценят ее как эффективное средство от болезней пчел, связанных с пчелиными клещами – паразитами.

Муравьиная кислота

3.Лимонная кислота
- Лимонная кислота является рекордсменом по плодам и ягодам, в которых она содержится: это крыжовник, листья махорки, хвоя, малина, свекловичный сок, листья хлопчатника, недозрелые лимоны и китайский лимонник (соответственно 80 и 70%).

Лимонная кислота
Лимонная кислота
Листья махорки
Лимонник китайский
1784 г К. Шееле

4.Щавелевая кислота
- Щавелевая кислота содержится в листьях щавеля, ревеня, шпината, клевера и даже плодах томата. Но с данной кислотой нужно держать «ухо в остро». Ее соли – оксалаты – нерастворимы в воде, поэтому «любители щавеля» могут заработать себе камни в почках и мочевом пузыре.

Щавелевая кислота

5.Аскорбиновая кислота
- Аскорби́новая кислота́ является одним из основных веществ в человеческом рационе, которое необходимо для нормального функционирования соединительной и костной ткани.
- Биологически активна
- один из изомеров — L- аскорбиновая кислота, называемая также витамином C . Витамин С в природе содержится во многих фруктах и овощах.
Аскорбиновая кислота

6.Ацетилсалициловая кислота
- Аспирин обладает противовоспалительным, жаропонижающим и болеутоляющим действием, поэтому его применяют при лихорадочном состоянии и ревматизме.
- Аспирин подавляет болевую чувствительность и помогает от головной боли.
- Однако у этого чудо – лекарства есть противопоказания, а именно: его нельзя применять при язве желудка.
- Вопрос: почему?
- Кислая среда, которую создает аспирин при реакции с водой, может усугубить течение болезни.

Ацетилсалициловая кислота

3.Станция Электролитическая
Электролиты- вещества, растворы или расплавы которых проводят электрический ток.
Электролитами являются вещества с сильно полярной ковалентной или ионной связью.
К ним относятся соли, щёлочи, кислоты.
Неэлектролиты - вещества, растворы или расплавы которых не проводят электрический ток.
Неэлектролитами являются вещества с неполярными или слабополярными ковалентными связями.
К ним относится глюкоза, фруктоза, сахароза, этанол, глицерин, сера, алмаз, азот, кислород и др.

Электролитическая диссоциация
Шведский физико-химик Сванте Аррениус, исследуя электропроводность водных растворов, высказал предположение, что в таких растворах вещества распадаются на заряженные частицы – ионы, которые могут передвигаться к электродам – отрицательно заряженному катоду и положительно заряженному аноду.
Данный процесс получил название электролитической диссоциации

Примеры электролитов:
Примеры Сильных электролитов:
1) все растворимые соли;
2) сильные кислоты, например: H 2 SO 4 , HCl, HNO 3 ;
3) все щелочи, например: NaOH, KOH.
Примеры Слабых электролитов:
1) Слабые кислоты – H 2 S, H 2 CO 3 , CH3-COOH;
2) водный раствор аммиака NH 3 *H 2 O;
3) вода.

Электролиты
«Среди карбоновых кислот
Известных "лиц" невпроворот.
В кислотах - группы карбоксильные,
Но все кислоты здесь – несильные!»

3.Станция Электролитическая
Ответьте на вопросы:
1.Почему лимонную кислоту не используют в аккумуляторах, предпочитая ей серную неорганическую кислоту?
2. Почему при данном эксперименте используют два различных металла?
3. Почему при данном эксперименте используют два лимона?
4. Почему при данном эксперименте используют именно цветной и черный металлы?

Объяснение опыта :
- Лимонная кислота, вступая в химическую реакцию с цинком, растворяет его.
- В результате от цинковой пластины отделяются положительно заряженные ионы и оседают на медной пластине, которая в свою очередь приобретает положительный заряд.
- Важно помнить, что подобные эксперименты не заменят настоящих источников электроэнергии.
4. Станция Химическая
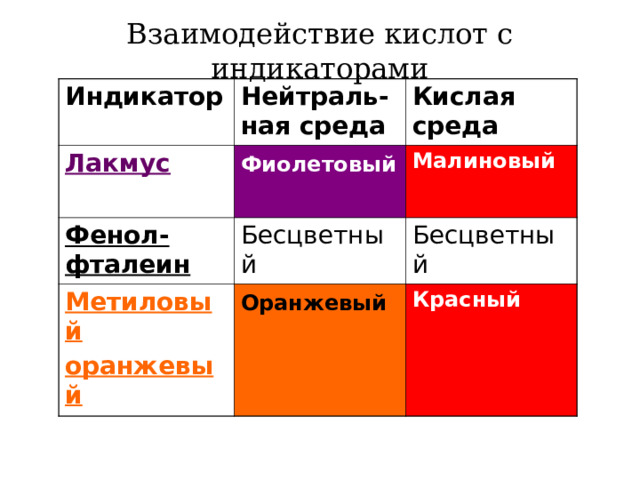
Взаимодействие кислот с индикаторами
Индикатор
Нейтраль-ная среда
Лакмус
Кислая среда
Фиолетовый
Фенол-фталеин
Малиновый
Бесцветный
Метиловый
оранжевый
Бесцветный
Оранжевый
Красный

4.Станция Химическая
- 1) Почему в алюминиевой кастрюле нельзя варить кислые щи или компот из свежих ягод?
- 2) При добавлении в тесто уксусной кислоты , гашенной содой (NaHCO 3 ), тесто становится пышнее. Чем это можно объяснить?
- 3) Для чего на ржавую гайку кладут тряпку, смоченную в уксусной кислоте?
- 4) Определить, в какой из пробирок находится кислота?
- 5) Почему нельзя употреблять сладкие газированные напитки людям с заболеваниями ЖКТ?
- 6) Почему после того, как вы съели апельсин, нельзя чистить зубы?

5.Станция Профессиональная
- топливо (бензин, дизельное топливо, сжиженный нефтяной газ, сжатый природный газ);
- смазочные материалы (моторные, трансмиссионные и специальные масла, пластичные смазки);
- специальные жидкости (тормозные и охлаждающие).

Основные эксплуатационные требования к топливу :
- - должно иметь высокую теплоту сгорания его рабочей смеси, обеспечивающую высокую экономичность двигателя;
- - должно обладать хорошими смесеобразующими свойствами, обуславливающими легкий запуск двигателя, его плавный переход с одного режима работы на другой;
- - не должно образовывать нагароотложений на деталях, приводящих к перегреву, а также не вызывать повышения износов двигателя;
- - должно быть стабильным при транспортировке и хранении, т. е. не изменять своих первоначальных свойств после их получения;
- - должно иметь антикоррозионные свойства , т. е. не вызывать коррозии деталей как при непосредственном контакте с топливом, так и от образующихся продуктов сгорания.

В основе принципа работы любого двигателя внутреннего сгорания лежит воспламенение небольшого количества топлива, обязательно высокоэнергетического, в небольшом замкнутом пространстве.

Влияние кислот на топливную систему автомобиля
- Органические кислоты, не полностью удаленные из бензина при его производстве и образующиеся в нем при длительном хранении, дают с медными и железными сплавами мыльный осадок .
- Содержание серы, неорганических водорастворимых кислот и щелочей в топливах вызывают коррозию и увеличивают износ деталей двигателя .

кислоты
- вызывают очень сильную химическую коррозию нижнего пояса гильзы цилиндра
- попадая с отработавшими газами в картер двигателя
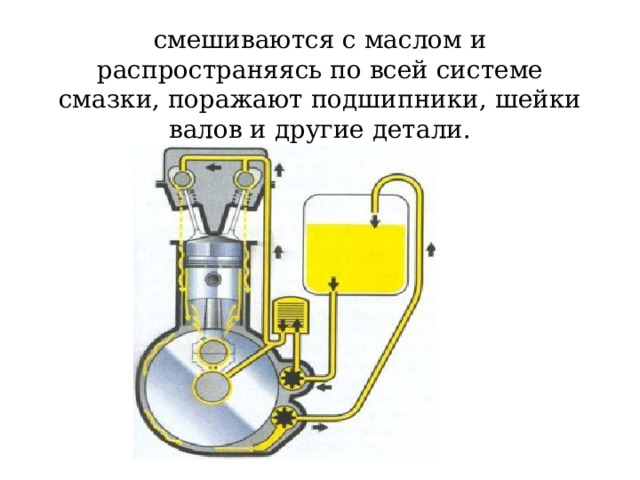
смешиваются с маслом и распространяясь по всей системе смазки, поражают подшипники, шейки валов и другие детали.

5.Станция Профессиональная
Просмотрите эксперимент «Определение кислот в ГСМ»
Ответьте на вопросы:
- 1.Влияют ли кислоты на свойства топлива и каким образом?
- 2. Влияют ли кислоты на работу двигателя и каким образом?
- 3. Должны ли находиться в качественном топливе кислоты?
- 4. Всегда ли в бензине содержатся кислоты?
- 5. Какие виды кислот могут находиться в бензине?
- 6.Влияют ли кислоты на составные части топливной системы и каким образом?

Лабораторный опыт «Определение кислот в ГСМ»
- Цели : Определить содержание кислот в вытяжке бензина и синтетического масла.
- Оборудование : пробирки, водные вытяжки ГСМ: синтетическое масло, бензин АИ-92, индикаторы: лакмус и метил оранжевый, пипетки.
- Инструкция к выполнению:
- Сущность метода заключается в извлечении водорастворимых кислот и щелочей из ГСМ водой и определения реакции среды с помощью индикатора.
- 1. В пробирку с вытяжкой бензина опустите лакмус. Наблюдайте за изменением окраски индикатора.
- 2. В пробирку с вытяжкой синтетического масла опустите лакмус. Наблюдайте за изменением окраски.
- 3.В пробирку с вытяжкой бензина добавить 3 капли индикатора метил оранжевого. Наблюдайте за изменением окраски. Наблюдения внесите в таблицу.
- 4. В пробирку с вытяжкой синтетического масла добавить 3 капли индикатора метил оранжевого. Наблюдайте за изменением окраски.
- Наблюдения внесите в таблицу.
Название
Окраска лакмуса
1.Водная вытяжка бензина АИ-92.
Окраска метилоранжевым
2.Водная вытяжка синтетического масла.


Вывод: Поскольку минеральные кислоты и щелочи, находящиеся в горюче-смазочных материалах, являются одной из причин, вызывающих коррозию деталей двигателя , то горюче-смазочные материалы, содержащие их, непригодны к эксплуатации !


9.Применение кислот


Контрольные вопросы
- Какое вещество вызывает жалящее действие крапивы и стрекательных клеток медуз:
а)муравьиная кислота, б) муравьиный альдегид.
2. Как снять боль от ожога, вызванного выделениями крапивы :
а) смыть водой, б) смыть слабым раствором щелочи,
в) смыть слабым раствором уксусной кислоты.
3. Структурную формулу муравьиной кислоты можно записать и таким образом НО-СОН. Следовательно, эта кислота будет являться веществом с двойственной функцией. Как можно назвать ее:
а) спирт, б) альдегидоспирт, в) кислота
4. Можно ли рассматривать переход количественных отношений в качественные на примере изменения физических свойств карбоновых кислот в гомологическом ряду?

5. Выберите формулы карбоновых кислот из предложенных формул и назовите их:
СН 3 , СН 3 СООН, С 2 Н 5 ОН, СН 3 СОН, С 2 Н 4 , С 15 Н 31 СООН, С 6 Н 6 , С 5 Н 11 СООН, С 3 Н 7 СООН
6. С какими веществами будет взаимодействовать уксусная кислота:
а) цинк, оксид натрия, гидроксид магния, карбонат натрия, спирт (этиловый)
б) цинк, оксид натрия, гидроксид магния, карбонат натрия, метан

Рефлексия:
У Вас «Алканы» на столе,
Таблица Менделеева на стене,
Формулы все изучены!

Рефлексия:

Домашнее задание :
- 1. Провести мини-исследование :
“ Царица Клеопатра по совету придворного медика растворила в уксусе самую крупную из известных ювелирам жемчужину, а затем принимала внутрь полученный раствор в течение некоторого времени.”
а) Какие вещества образуются при взаимодействии уксуса с жемчугом?
б) Несут ли пользу продукты данной реакции для организма?
в) Насколько реален данный исторический факт?
Аргументируйте свой ответ “за” или “против”.
- 2. Составить кроссворд из 10 слов по теме «Электролиты и неэлектролиты»

«Ни один сосуд не вмещает больше своего объема,
кроме сосуда знаний, он постоянно расширяется…»
(Арабская пословица)

Благодарим за внимание!
















































































