План урока:
I. Вступление учителя.
II. Методы изучения строения белков. (Просмотр видеофильма)
Белки в природе (сообщение учащегося)
Состав и строение белков.
V. Физико-химические свойства.
Функции белков.
Занимательные вопросы (проверка знаний).
Ход урока.
I. Вступление учителя.
С чем связана тайна жизни? Что же отличает живые тела от неживых? «Вопросов полон мир, - кто даст на них ответ?» - написал десять веков назад Омар Хайам, ученый и поэт.
И как бы в ответ прозвучали слова другого ученого и поэта Сьюрри Стурлусона (исландца). Много нужно иметь знаний, чтобы поведать об этом.
Когда двести лет назад химики начали изучать белки, они и не подозревали, что берут в руки ключ к целому неизвестному миру - миру живой клетки, такому же неисчерпаемому, как и мир атома. И уже довольно скоро ученые поняли, что самую важную, самую главную роль во всех жизненных процессах играют белки, именно белки лежат в основе всего живого. Вспомните крылатую фразу Ф. Энгельса: «Жизнь есть способ существования белковых тел...»
Нам известно, что белки содержаться в любой клетке живого организма, но обнаружить, изучить белки стало возможным только с появлением микроскопа, и особенно детально изучить их строение, хим. состав с помощью электронного микроскопа и метода центрифугирования.
II. Просмотр видеофильма о методах изучения строения белков. Ш. Сообщение учащегося о местонахождении белков в природе, с использованием наглядных природных материалов
белок куриного яйца - альбумин
белок кератин (рога, копыта, когти, волосы)
белок вибрион (ткани натурального шелка)
белок зерна (клейковина)
Русский хлеб отличается высоким содержанием и уникальным составом белков.
Подводя итог своего рассказа, необходимо спросить «Где же встречаются белки в природе» ( в живых организмах). Что же собой представляют по составу белки?
IV. Состав и строение белков. J_. состав
Белки - это сложные органические соединения, состоящие из углерода, водорода, кислорода и азота (в некоторых содержится и сера). Часть белков
образует комплекс с другими молекулами, содержащими фосфор, железо, цинк и медь. Белки - это биополимеры, молекулами которых являются аминокислоты. Молекулярные формулы некоторых белков поражают своей грандиозностью: А также в
А также в
связи с этим большая молекулярная масса, например, белок куриного яйца -36000, белок мышц - 1500000. Итак, белки - необычайно сложные вещества. В результате гидролиза белков получают 20 различных аминокислот. Из них 11 аминокислот могут синтезироваться в организме. Остальные 9 должны обязательно поступать в организм животного и человека в виде пищи. Поэтому они получили название незаменимых аминокислот. Все эти 20 аминокислот,
1 S
соединяясь, друг с другом могут образовать 2,4*10 различных комбинаций
белков.
2^ «Какова же структура белка?»
Для того, чтобы разобраться в укладке (архитектуре) белковой макромолекулы, следует рассмотреть несколько уровней её организации.
ПЕРВИЧНАЯ, самая простая структура - полипептидная цепь - нить аминокислотных остатков. Пептидные связи достаточно жесткие, и они придают молекулам определенную стабильность. Первыми выяснили принцип построения белка из аминокислот и определили структуру белка Э. Фишер и Ф. Сэнгер.
Например: давайте посмотрим, как же образуется первичная структура белка (учащийся записывает на доске)
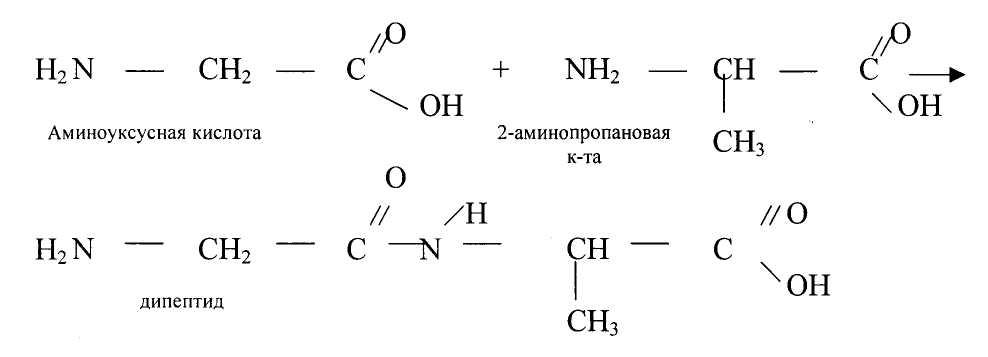
Образование из двух молекул АМК называется дипептид, из трех -трипептид и т.д.
ВТОРИЧНАЯ. В 1951г. Полинг и Кори доказали, что благодаря образованию водородных связей между расположенными группами -СО- и -NH, происходит дальнейшая укладка белковой молекулы. В результате образуется спираль. За счёт вторичной структуры, длина полимерной цепи сокращается в 4 раза. Такая структура спирали была обозначена как ct-структура.
Имеется и более сложная складчатая Р-конфигурация, напоминающая по форме гармошку. Возможны превращения из одной структуры
молекулы белка в другую за счет перестройки водородных связей. Такого рода превращения свойственны белку волос - кератину.
Белок волос может существовать как в виде а- спирали (волнистый волос), так и в виде (3-складчатого слоя (прямой волос). Причем при растягивании завитка волос водородные связи рвутся, спираль разрушается, затем вновь восстанавливается.
ТРИТИЧНАЯ структура - конфигурация, которую принимает в пространстве закрученная в спираль полипептидная цепь. Эта структура определяет форму молекулы белка: глобулярную (клубок) и фибриллярную (нити).
Тритичная структура поддерживается за счет связей: S-S дисульфидные мостики, СООН и ОН сложноэфирные мостики, СООН и NH2 солевые мостики.
ЧЕТВЕРТИЧНАЯ структура - объединение белковых молекул в крупные агрегаты (гемоглобин). V. Физико-химические свойства.
по растворимости делятся: растворимые и нерастворимые
под действием различных факторов белки теряют свои свойства,
нарушается структура. Данный процесс называется денатурацией.
Факторы, вызывающие денатурацию делятся: физические (температура) и
химические (действия кислот, щелочей и т.д.).
Иногда наблюдается растворение выпадающего осадка при избытке воды. Данный процесс называется ренатурацией.
3. цветные реакции на белки.
Лабораторная работа Тема: Цветные реакции на белки
Цель: С помощью цветных реакций доказать наличие в белках тех или иных аминокислот. Ход работы:
| Что делали | Что наблюдали | Вывод |
| 1. Влить в пробирку 2-3 | Красно-фиолетовая | Окраска доказывает |
| мл. раствора белка и | окраска | наличие пептидных |
| добавить несколько |
| групп в белках |
| мл. раствора |
|
|
| гидроксида натрия, а |
|
|
| затем раствора |
|
|
| сульфата меди |
|
|
| 2. В пробирку налить 2- | Желтая окраска | Окраска доказывает |
| 3 мл. раствора белка |
| наличие остатков |
| и добавить 0,5 мл. |
| ароматических кислот. |
| концентрированной |
|
|
| азотной кислоты |
|
|
| (осторожно) |
|
|
Вывод: наличие белков в пищевых продуктах можно доказать с помощью цветных реакций, сущность их заключается в доказательстве наличия тех или иных аминокислот.
VI. Белок - это жизнь, поэтому функций белков в организме
очень много (сообщение учащегося). Одна из функций - каталитическая.
Лабораторная работа
Тема: Расщепление пероксида водорода ферментом каталазой. Цель: Определить действие фермента на примере картофеля. Учитель. Сведения о ферменте:
фермент каталаза имеется в каждой растительной и животной
клетке
каталаза расщепляет пероксид водорода с образованием молекулы
воды и кислорода. Одна молекула в одну секунду расщепляет сто
тысяч молекул пероксида водорода.
каталаза, расщепляя пероксид водорода, играет защитную роль,
т. к. пероксид водорода - яд, который непрерывно образуется в
клетке в процессе жизнедеятельности.
Ход работы:
Прилить по 2 мл. пероксида водорода в пробирку с сырым и вареным
картофелем.
Что наблюдаете? (пузырьки газа, которые образуются при расщеплении)
В каких пробирках (в пробирках с сырым картофелем)
Почему в пробирке с вареным картофелем не наблюдается расщепление
пероксида водорода (т.к. произошла денатурация каталазы при варке
картофеля)
Вывод: Во всех клетках живых организмов есть фермент каталазы. Выделение кислорода при действии на пероксид водорода каталазы свидетельствует о проявлении каталитической функции белка - фермента. УЦ. Занимательные вопросы.
Почему при работе с азотной кислотой иногда наблюдаются
желтые пятна на коже рук? (произошла ксантопротеиновая реакция
- реакция на наличие в белках ароматических кислот)
Как извлечь белок из яйца, не разбивая его? (опустить яйцо в
уксусную кислоту)
При заболевании у больного повышается температура. Как
объяснить, что при высокой температуре врач назначает
жаропонижающие лекарства, а при низкой - нет? (потому что при
высокой температуре происходит денатурация белка).
Что происходит с шерстяными вещами при стирке и почему?
(изменяется вид, уменьшается размер, т. к. произошла денатурация
белка кератина).
50
Творческие:
При заболевании у больного повышается температура. Как объяснить,
что при высокой температуре врач назначает жаропонижающие средства, а при
низкой нет?
Что происходит с шерстянными вещами при стирке? И почему?
Приложение №3
Эксперимент по практикуму, разработанному автором Л. С. Гузей. Изучение воздействия веществ на живые организмы.
1. Название опыта: Окисление спирта в альдегид.
Используется в теме: «Химические свойства спиртов и фенолов»
Цель: осуществить превращение этилового спирта в ацетальдегид и установить его наличие в реакционной смеси.
Ход работы:
Налить в пробирку около 1 мл. этилового спирта. Зажечь горелку, в верхнюю часть пламени внести скрученный в спираль конец медной проволоки и прокалить, пока медь не покроется слоем оксида. Не охлаждая, перенести проволоку в пробирку со спиртом.
Вопрос к учащимся: Что вы наблюдаете?
Ответ: Спираль становится блестящей, появляется специфический, неприятный запах.
Добавить в пробирку немного фуксинсерной кислоты.
Вопрос: Что вы наблюдаете?
Ответ: Появляется розовая окраска.
Вопрос: Как вы думаете, о чем говорит розовая окраска?
Ответ: Окраска доказывает наличие образовавшегося альдегида.
Составьте уравнение реакции окисления этилового спирта оксидом меди

Вопрос: Исходя из наблюдений опыта, какой же вывод можно сделать?
Вывод: В ходе лабораторного опыта нам удалось осуществить превращение этилового спирта в ацетальдегид и доказать его наличие с помощью фуксинсерной кислоты.
Образовавшийся уксусный альдегид является первичным продуктом метаболизма этанола на пути превращения в уксусную кислоту. 2. Название опыта:«Исследование растворимости жиров, доказательство их непредельности»
Тема урока: «Жиры»
Цель:
Исследовать растворимость жиров в воде и органических растворителях. Определить отношение жиров к раствору перманганата калия.
Ход работы:
38


















