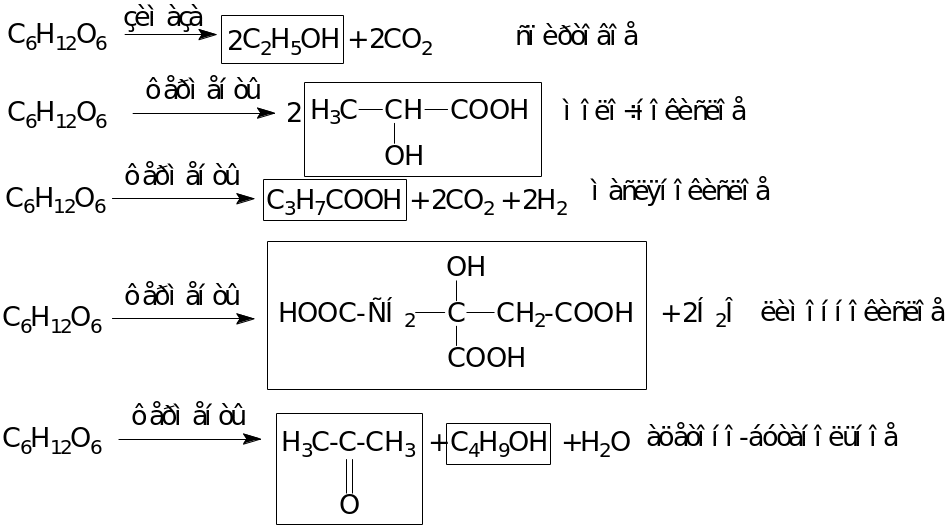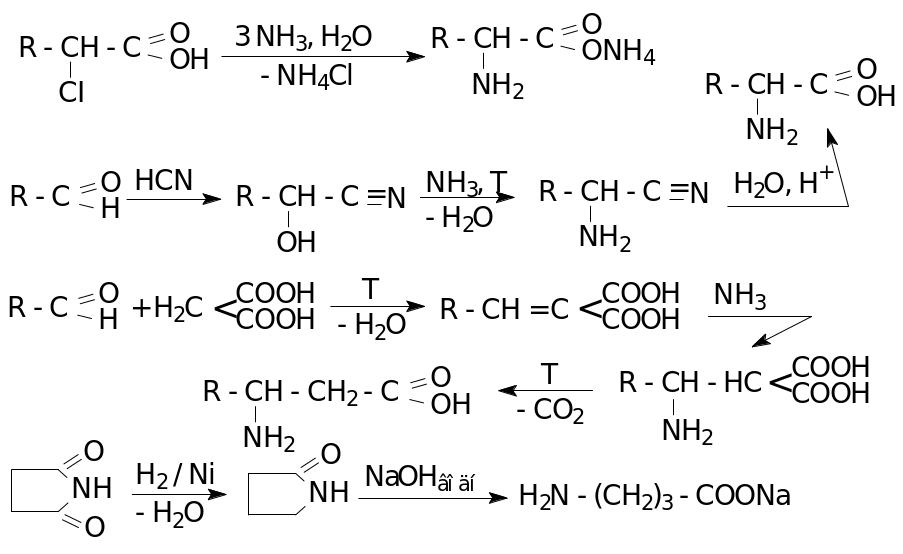СОДЕРЖАНИЕ
| Предисловие Номенклатура Алканы Алкены Алкины Алкадиены Галогенпроизводные углеводороды Одноатомные предельные спирты Одноатомные непредельные спирты Многоатомные спирты Серусодержащие соединения Простые эфиры Внутренние эфиры Альдегиды Кетоны Одноосновные предельные карбоновые кислоты Одноосновные непредельные карбоновые кислоты Двухосновные предельные карбоновые кислоты Двухосновные непредельные карбоновые кислоты Оксикислоты Оксокислоты Углеводы Амины Аминокислоты. Белки Список литературы Приложения | 4 5 9 11 12 13 14 15 16 17 18 19 19 20 21 22 23 24 24 25 26 27 31 32 33 34
|
Предисловие
Данное пособие предназначено для студентов химических и биологических специальностей, изучающих органическую химию. В нем в виде схем и таблиц представлены основные способы получения и химические свойства разных классов органических соединений алифатического ряда.
Представленный в пособии материал позволяет оперативно получать наглядную информацию по изучаемым в курсе органической химии процессам и может быть использован студентами при подготовке к контрольным работам, семинарским и практическим занятиям.
Разумеется, использование предложенного материала возможно только наряду с учебниками по органической химии, с предлагаемыми лектором учебными материалами, но не вместо них. Фактически в данном пособии сделана попытка разработать краткий конспект курса органической химии, а, как известно, конспект ни при каких условиях не может заменить самого конспектируемого материала.
В состав авторского коллектива вошли трое выпускников биолого-химического факультета 2010 г. Аккуратов А.В., Мумятов А.В., Орлов П.В., поэтому авторы надеются, что представленный в пособии материал будет понятен студентам.
Авторы заранее благодарны читателям за замечания и пожелания, которые в дальнейшем позволят усовершенствовать данное пособие.
Номенклатура
Правила построения названия органического соединения
| Историческая |
| Систематическая |
| Рациональная |
|  
|
| 
|
|
| название строят без системы – можно только заучить |
| название строят в соответствии с правилами IUPAC 1965 г. | выбирают базовый фрагмент (родоначальник) и заместители при нем |
Тривиальные (исторические) названия
некоторых заместителей
| С Н3- Н3- СН3СН2- СН3СН2СН2- (СН3)2-СН- СН3СН2СН2СН2- (СН3)2-СН-СН2- 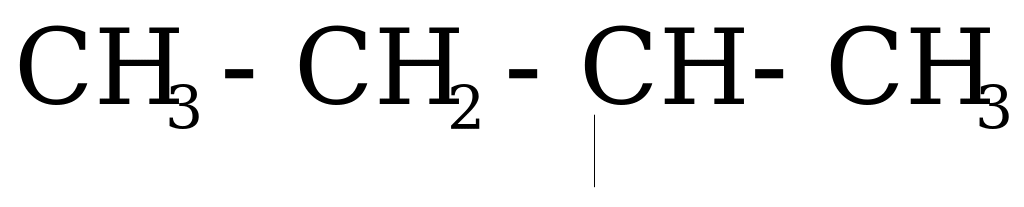
| метил этил н-пропил изопропил н-бутил изобутил втор.бутил |
| (СН3)3-С- СН3СН2СН2СН2СН2- (СН3)2СН2СН2СН2- 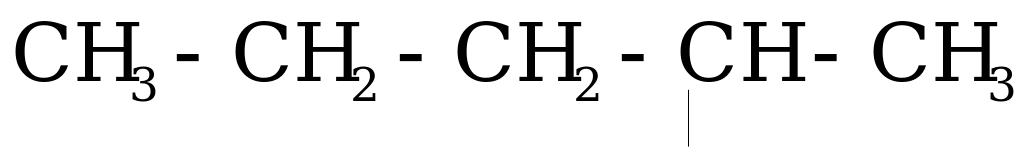 СН2=СН- СН2=СН- СН2=СН-СН2- (СН3)3-С-СН2- | трет.бутил н-амил изоамил втор.амил винил аллил неоамил |
*другие заместители называют по системе, представленной ниже
Правила названия заместителя (радикала)
Нумеруется углеродная цепь радикала, начиная с атома, по которому идет замещение. Все остальное, как в номенклатуре IUPAC для алканов (см. стр. 6), окончание -ил, название заместителя заключается в скобки.
Порядок перечисления заместителей (старшинство) определяется наименьшей молекулярной массой. При равной массе – наибольшей разветвленностью углеродной цепи (например, изопропил будет называться раньше н-пропила).
Пример названия заместителя:

Правила рациональной номенклатуры
В
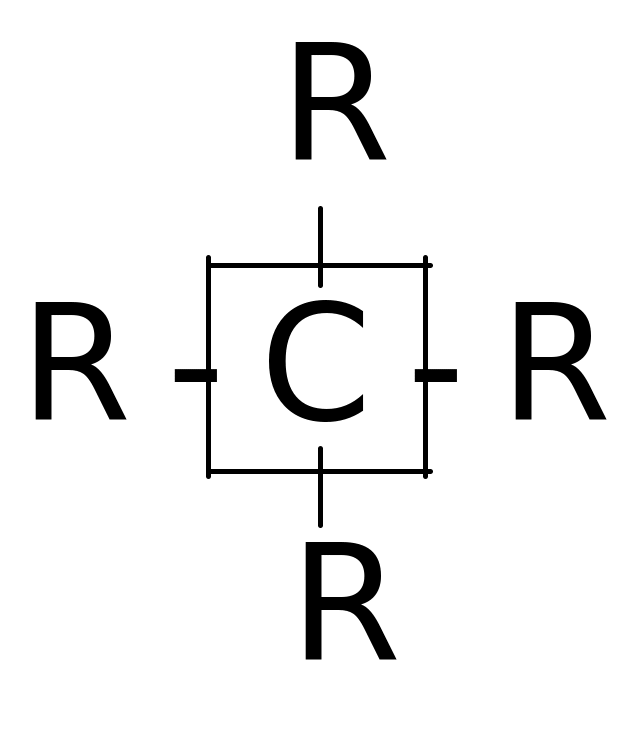
ыбирается базовый фрагмент (родоначальник): для алканов рекомендуется самый разветвленный атом углерода (метан). Строится название: для алкана – называются радикалы (при наличии одинаковых заместителей, используют приставки ди-, три-, тетра-), окончание – метан.
Распространенные базовые фрагменты органических молекул:
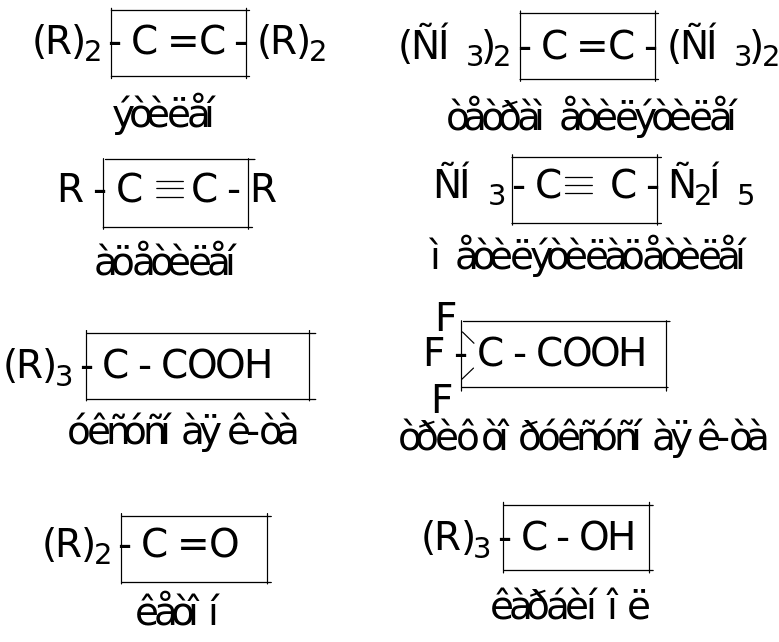
Правила систематической номенклатуры (IUPAC)
Насыщенные УВ (алканы)
Выбирается самая длинная углеродная цепь (при равных условиях выбирают вариант с максимальным числом заместителей).
Выбирается начало углеродной цепи: сумма цифр, указывающих местоположение заместителей, должна быть минимальной.
Нумеруется углеродная цепь (название алкана определяется количеством атомов углерода в главной цепи, окончание -ан).
Строится название алкана: цифрами указывается место присоединения заместителей (каждому заместителю должна соответствовать цифра, даже если они находятся у одного атома углерода); при наличии одинаковых радикалов используют приставки ди-, три-, тетра-, пента- и т. д.; заместители перечисляются в порядке возрастания молекулярной массы, при равенстве массы – более разветвленные радикалы.
Пример:
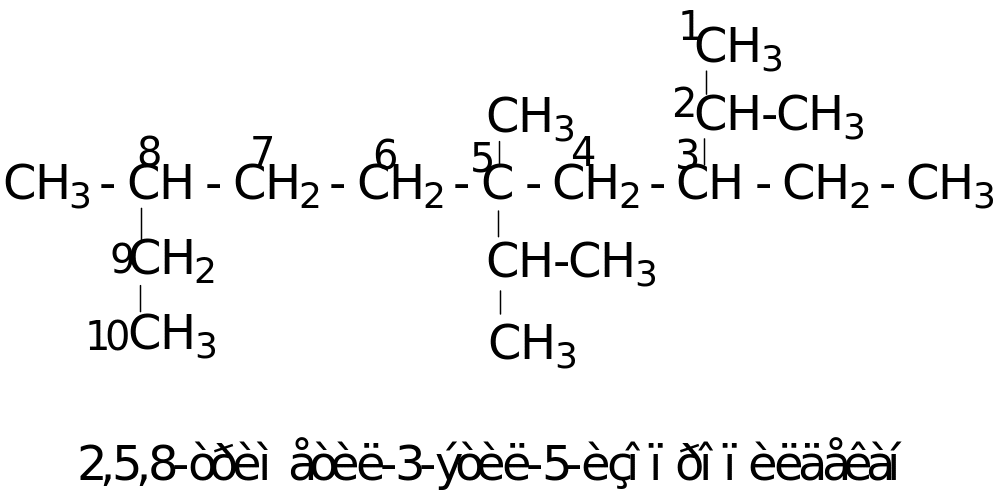
Соединения, содержащие функциональные группы
Выбирается самая длинная углеродная цепь, содержащая функциональную группу либо максимальное количество функциональных групп.
Выбирается начало углеродной цепи: определяется близостью функциональной группы по их старшинству (Приложение 1).
Строится название соединения: цифрами и префиксами указывается место присоединения радикалов и функциональных групп в порядке их старшинства. Класс соединения указывается суффиксом и цифрой места положения его функциональной группы либо перед, либо после корня главной цепи. Наличие в главной углеродной цепи нескольких фрагментов, соответствующих классам, фиксируется цифрой и суффиксом.
Пример:
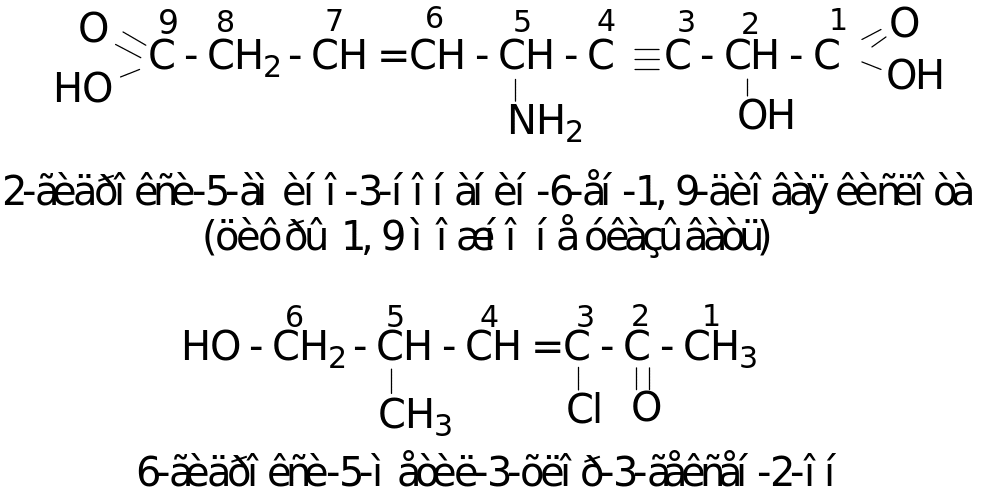
Так как в соединениях, приведенных в примере, содержится двойная связь, то для них характерна цис-транс-изомерия.
АЛКАНЫ
Способы получения
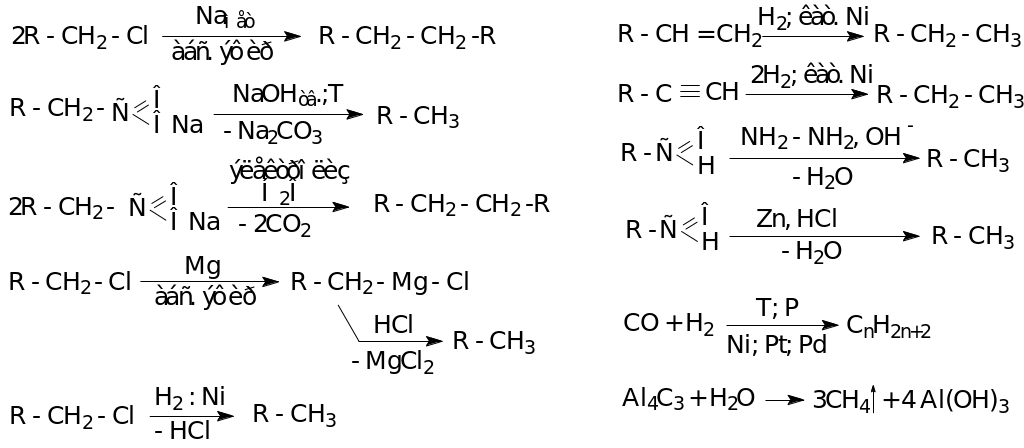
Химические свойства

Механизмы реакций алканов
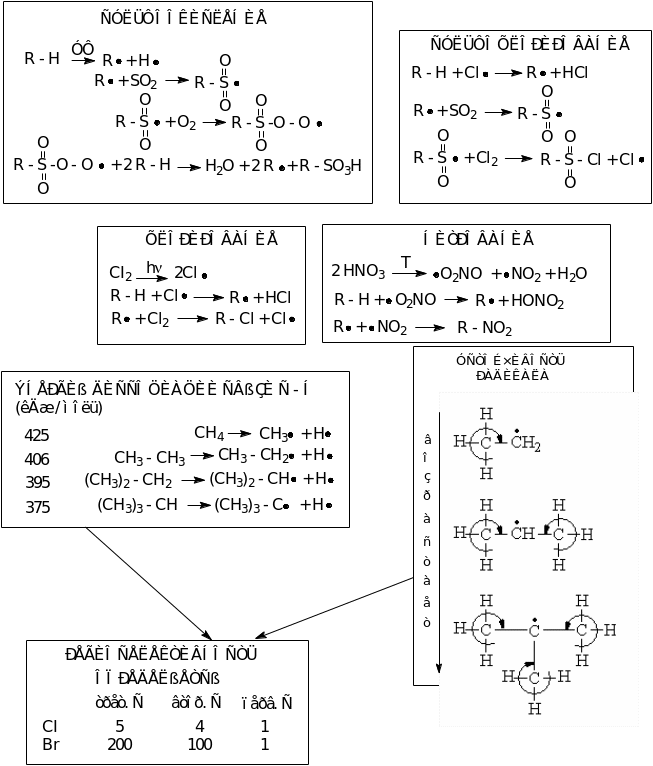
АЛКЕНЫ
Способы получения
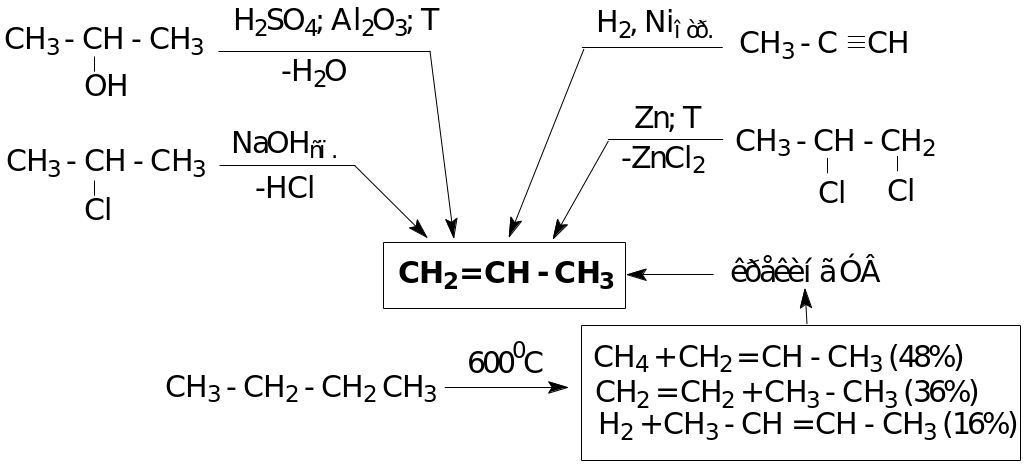
Химические свойства

АЛКИНЫ
Способы получения

Химические свойства
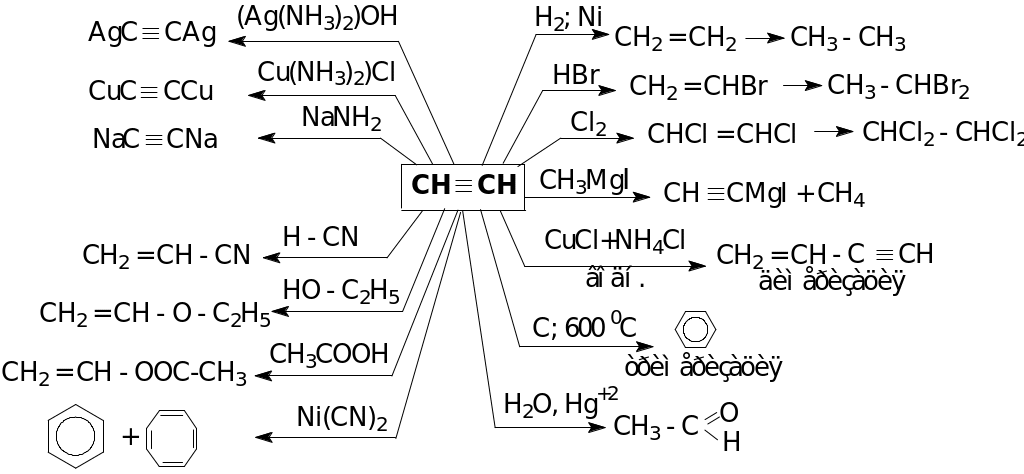
АЛКАДИЕНЫ
Способы получения
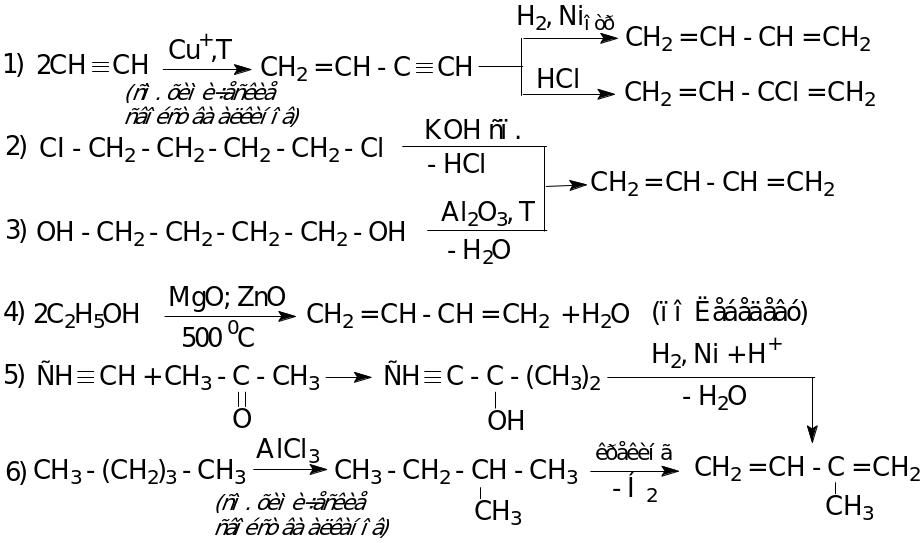
Химические свойства
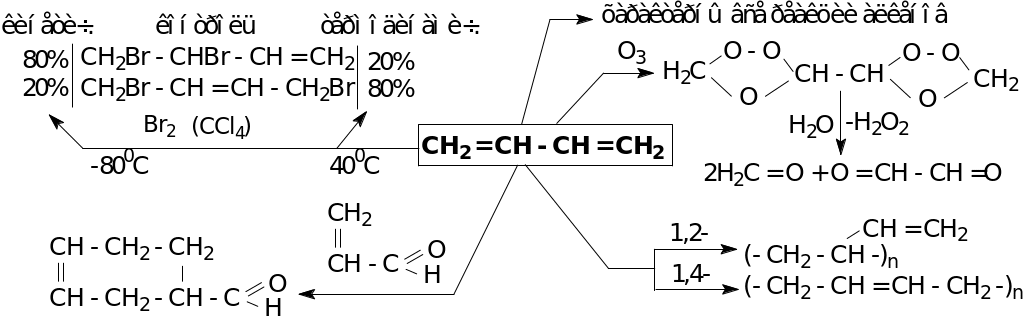
ГАЛОГЕНПРОИЗВОДНЫЕ УГЛЕВОДОРОДЫ
Способы получения
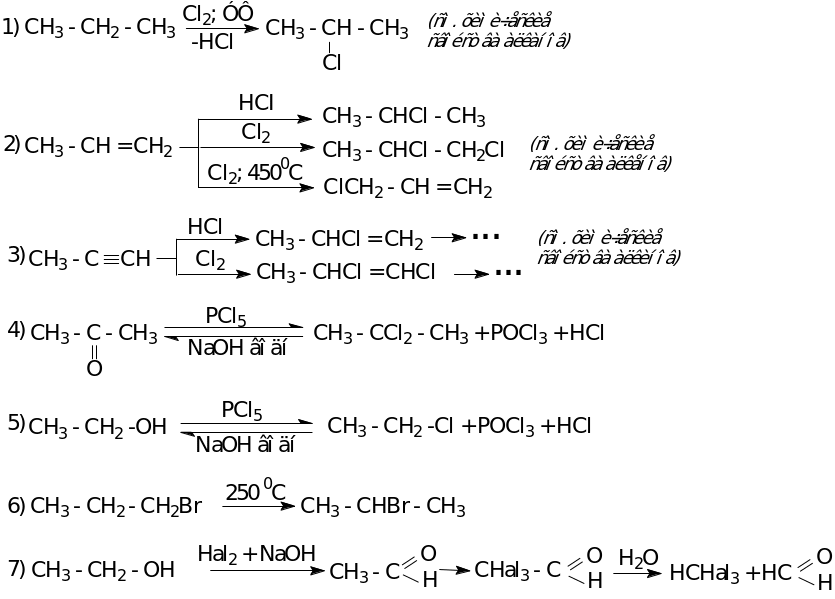
Химические свойства
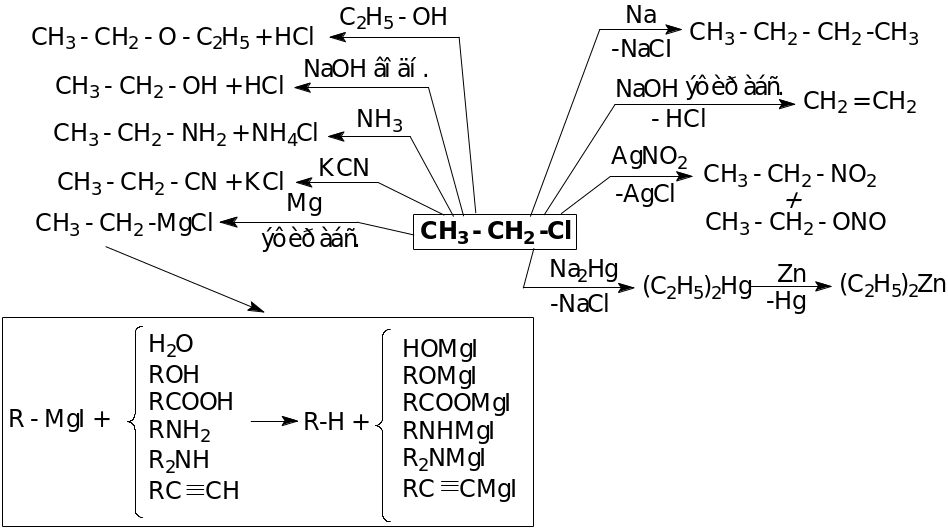
ОДНОАТОМНЫЕ ПРЕДЕЛЬНЫЕ СПИРТЫ
Способы получения
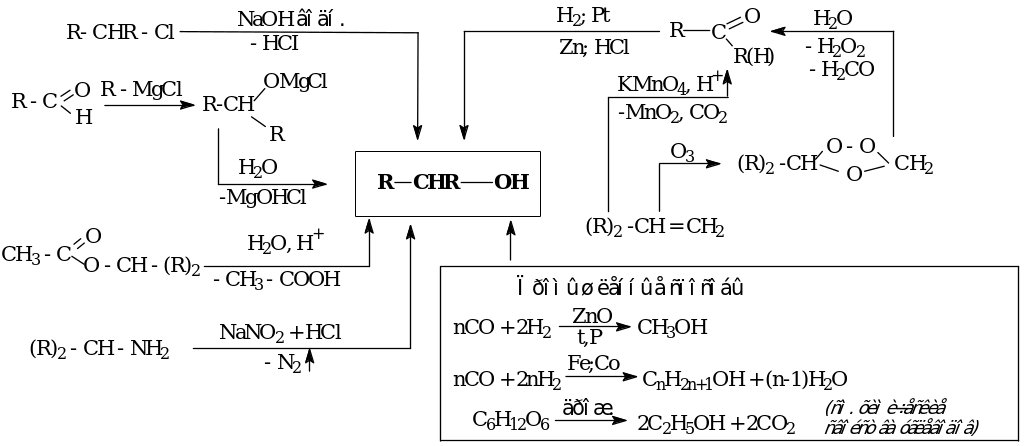
Химические свойства
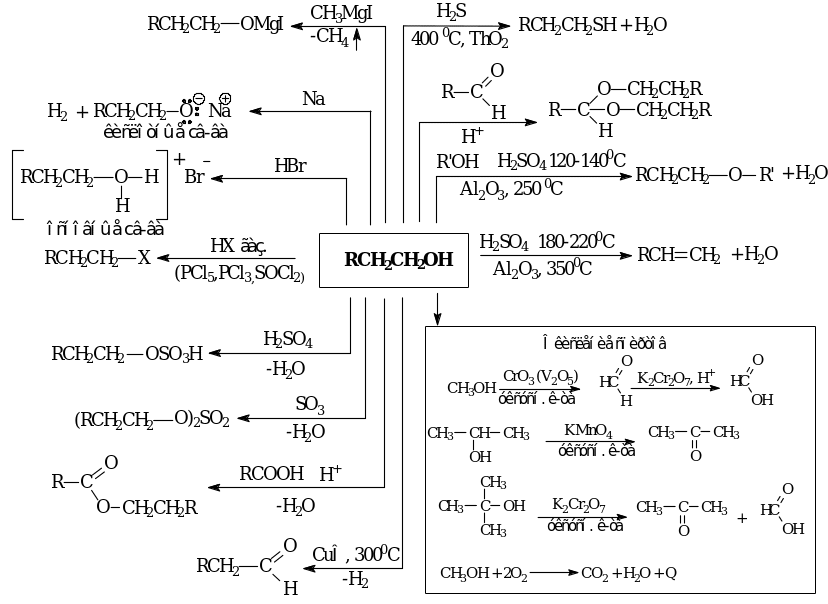
ОДНОАТОМНЫЕ НЕПРЕДЕЛЬНЫЕ СПИРТЫ
Способы получения
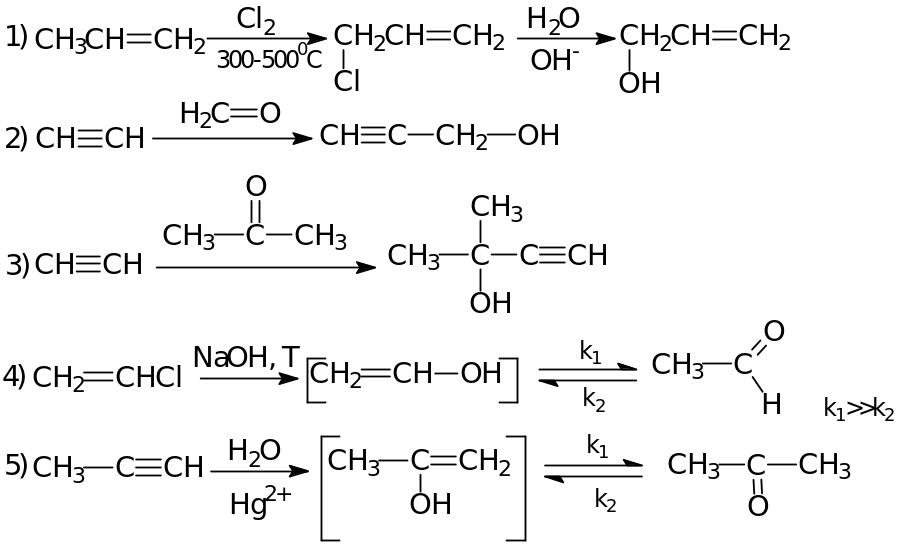
Химические свойства
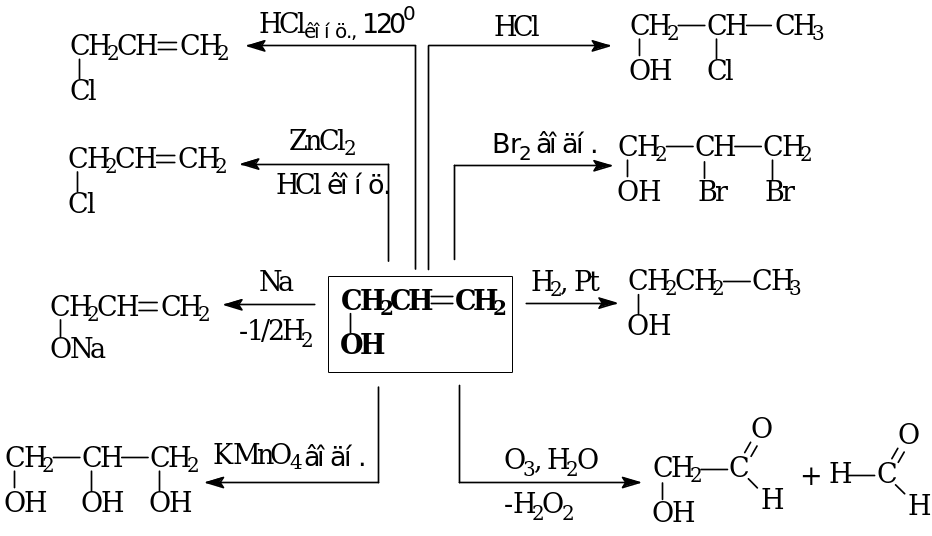
МНОГОАТОМНЫЕ СПИРТЫ
Способы получения
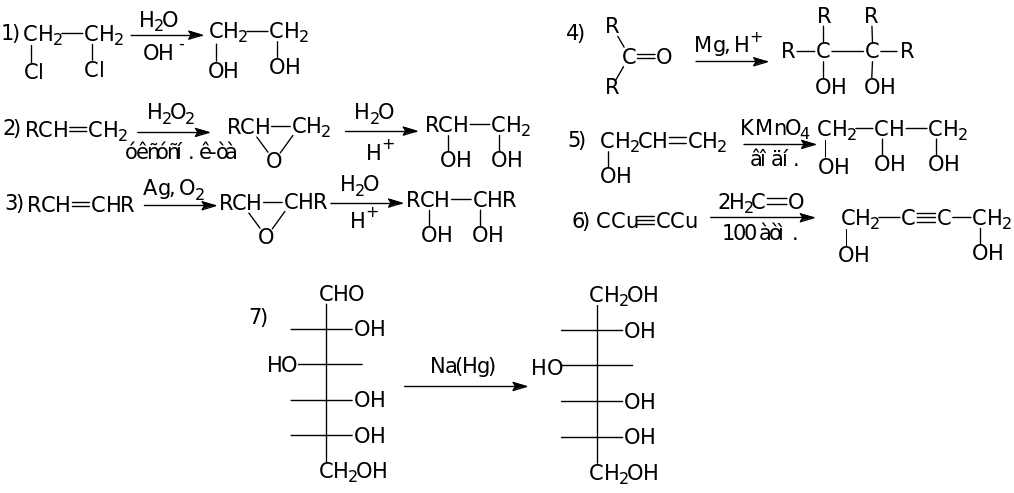 Химические свойства
Химические свойства

СЕРУСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
Способы получения
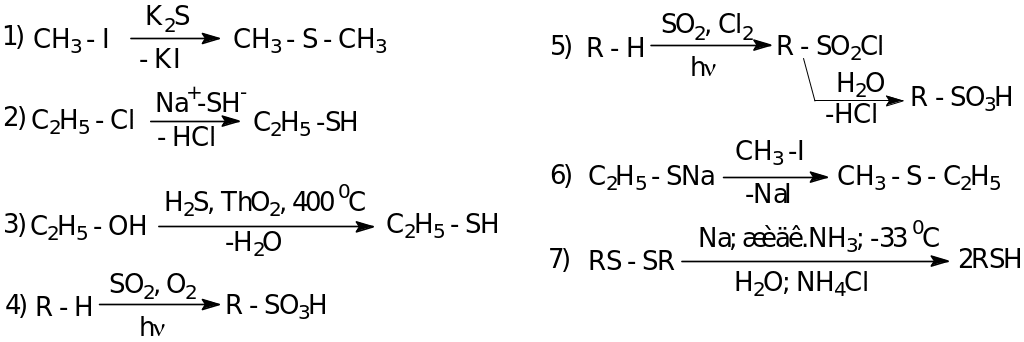
Химические свойства

ПРОСТЫЕ ЭФИРЫ
Способы получения
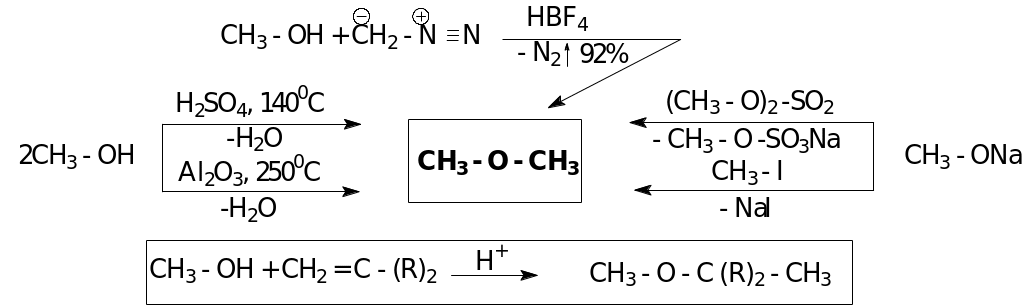
Химические свойства
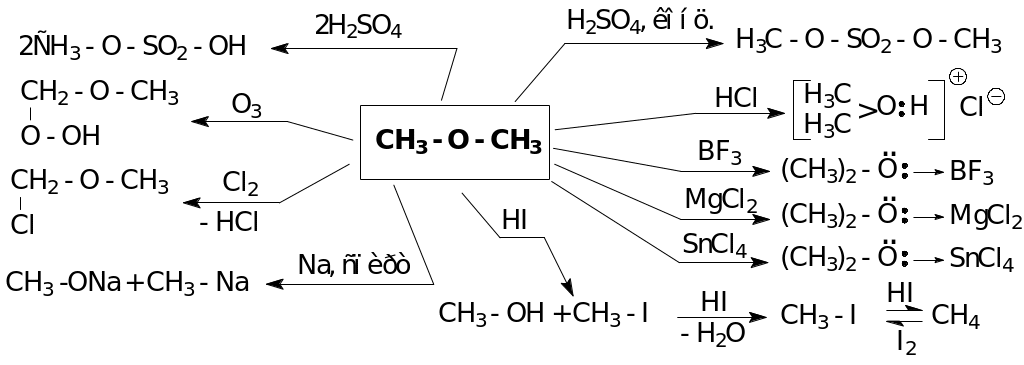
ВНУТРЕННИЕ ЭФИРЫ
Свойства и получение
АЛЬДЕГИДЫ
Способы получения

Химические свойства
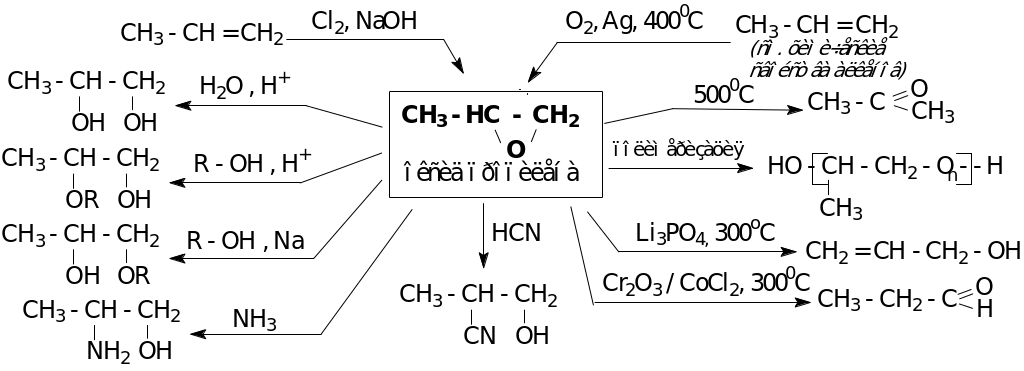
КЕТОНЫ
Способы получения
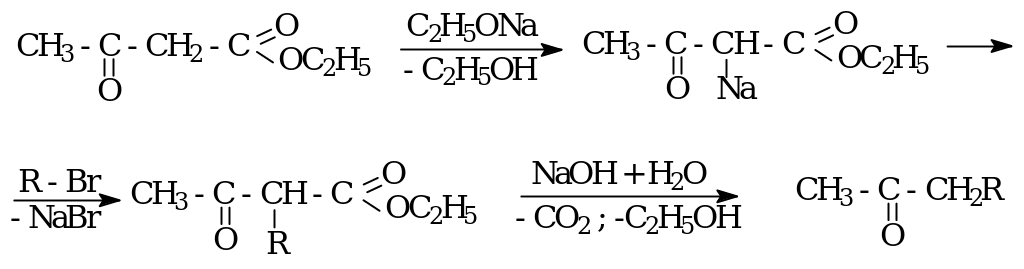
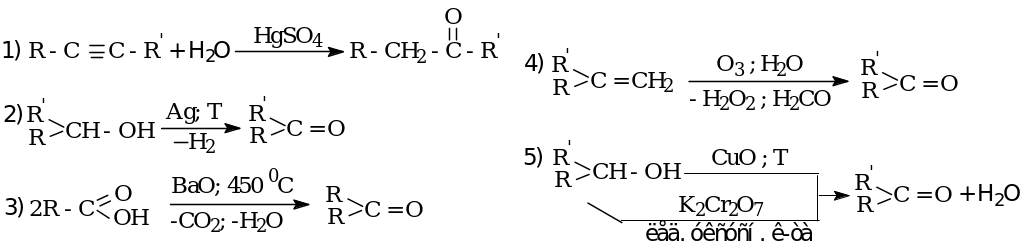 Кетонное расщепление ацетоуксусного эфира
Кетонное расщепление ацетоуксусного эфира
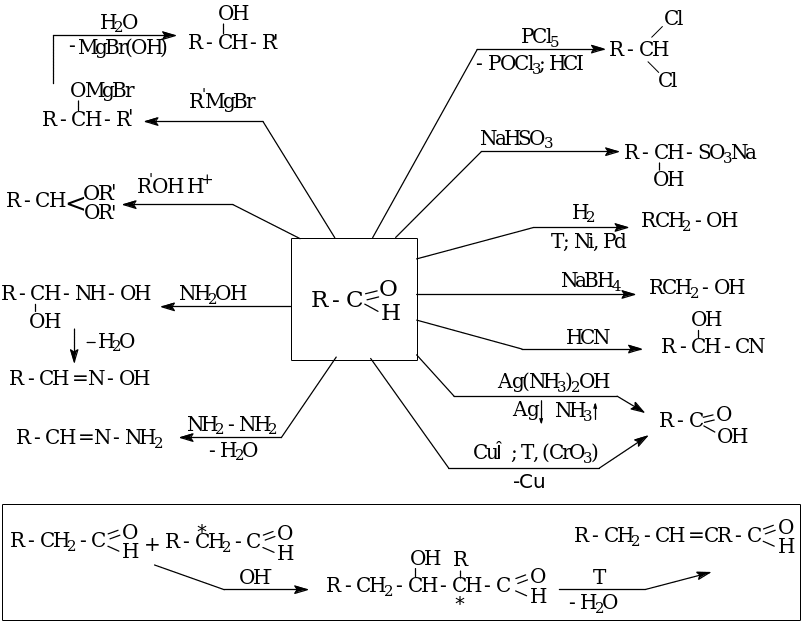
Химические свойства
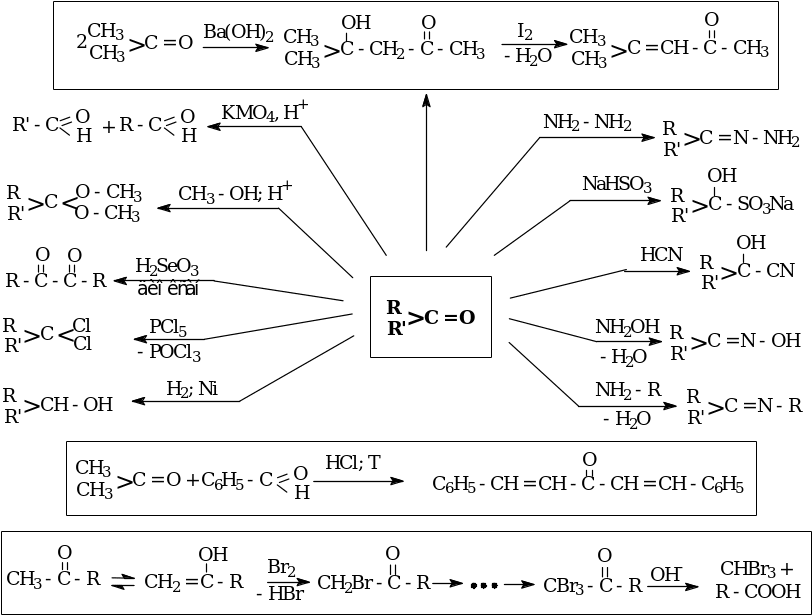
ОДНООСНОВНЫЕ ПРЕДЕЛЬНЫЕ
КАРБОНОВЫЕ КИСЛОТЫ
Способы получения
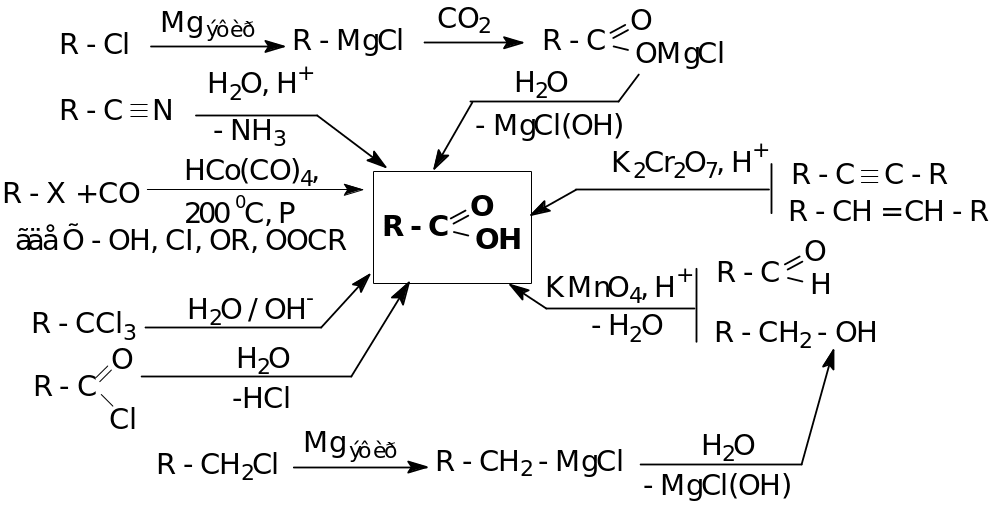
Химические свойства
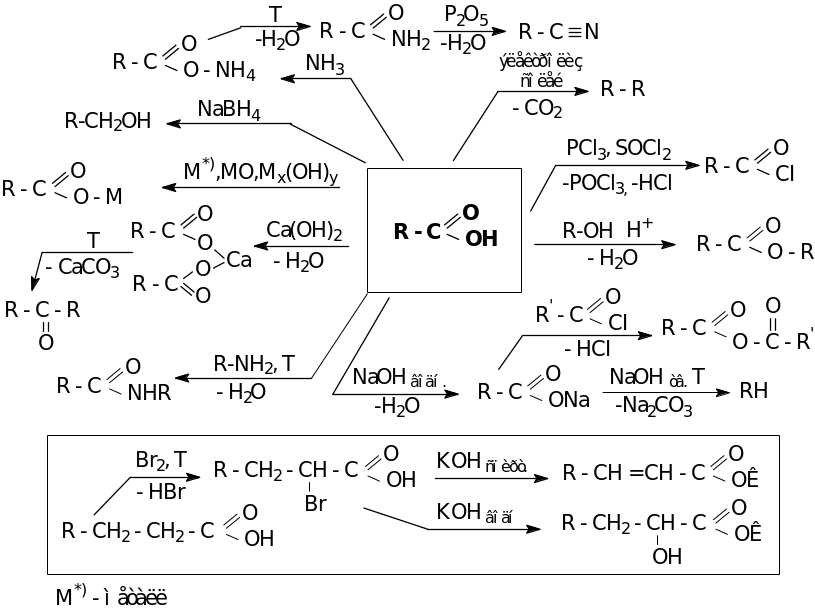
ОДНООСНОВНЫЕ НЕПРЕДЕЛЬНЫЕ
КАРБОНОВЫЕ КИСЛОТЫ
Способы получения
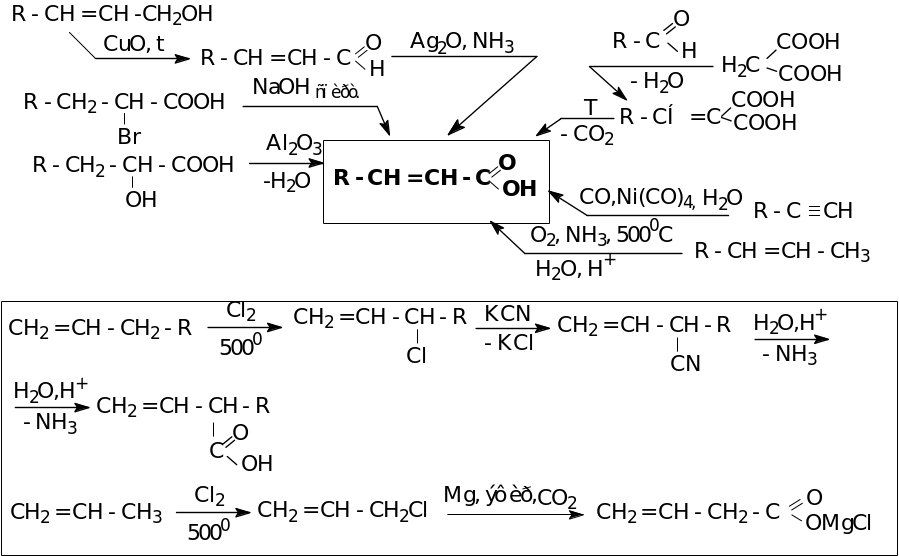
Химические свойства
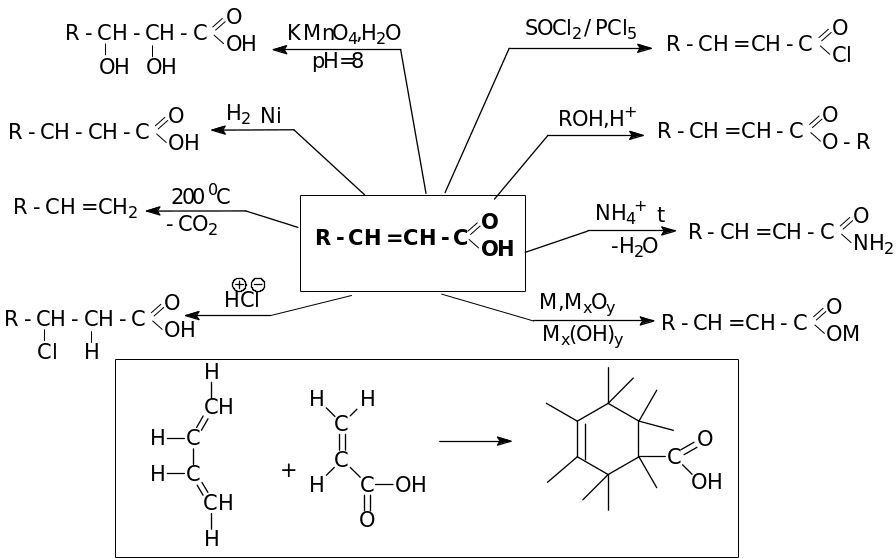
ДВУХОСНОВНЫЕ ПРЕДЕЛЬНЫЕ
КАРБОНОВЫЕ КИСЛОТЫ
Химические свойства
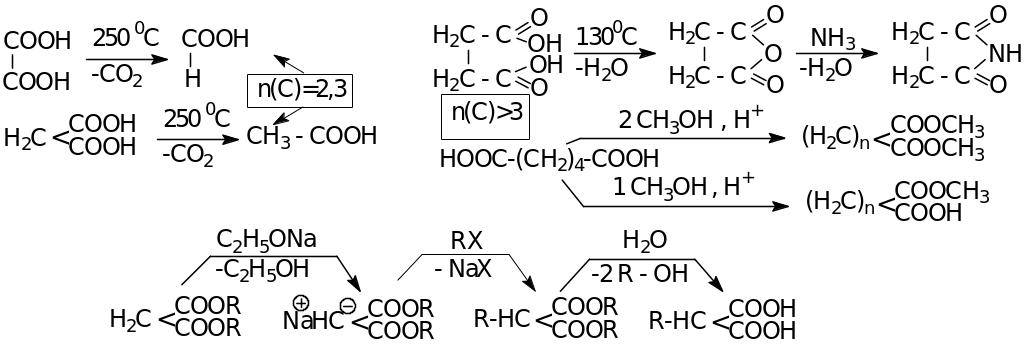
ДВУХОСНОВНЫЕ НЕПРЕДЕЛЬНЫЕ
КАРБОНОВЫЕ КИСЛОТЫ
Способы получения

ОКСИКИСЛОТЫ
Способы получения

Химические свойства
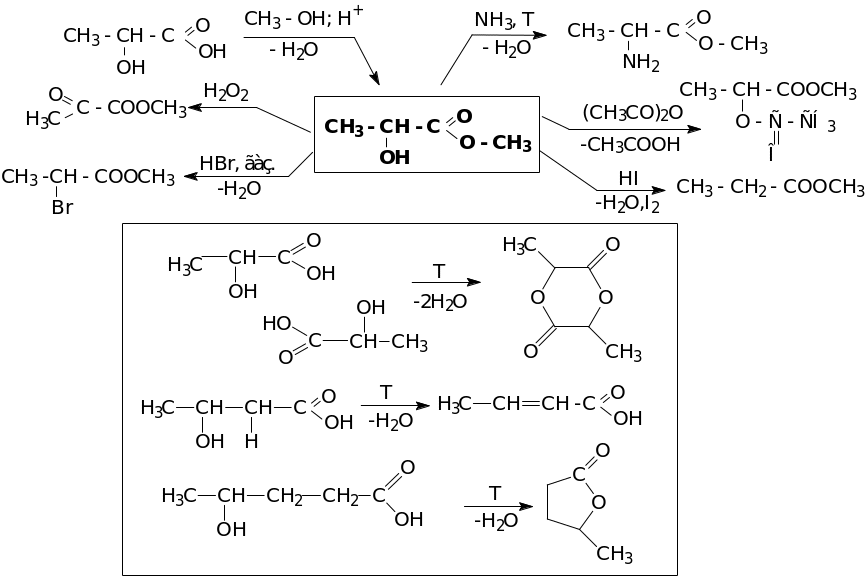
ОКСОКИСЛОТЫ
Химические свойства

УГЛЕВОДЫ
Способы получения
Гидролиз полисахаридов (крахмала).
Осторожное окисление многоатомных спиртов, при котором одна спиртовая группа окисляется в альдегидную.
Наращиванием цепи:
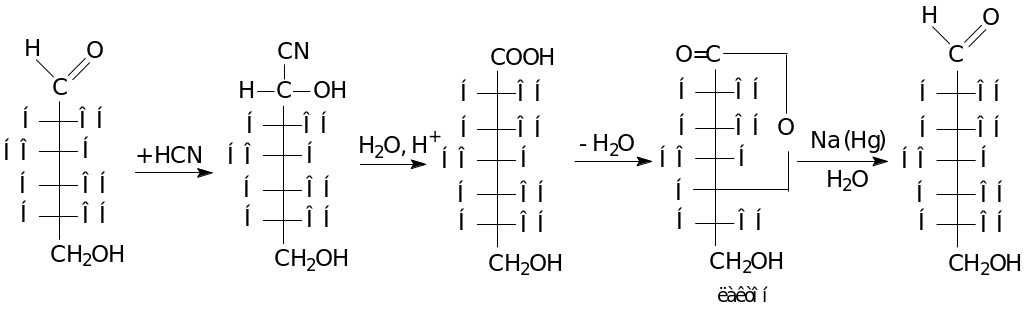
Деструкцией (укорачиванием) цепи:
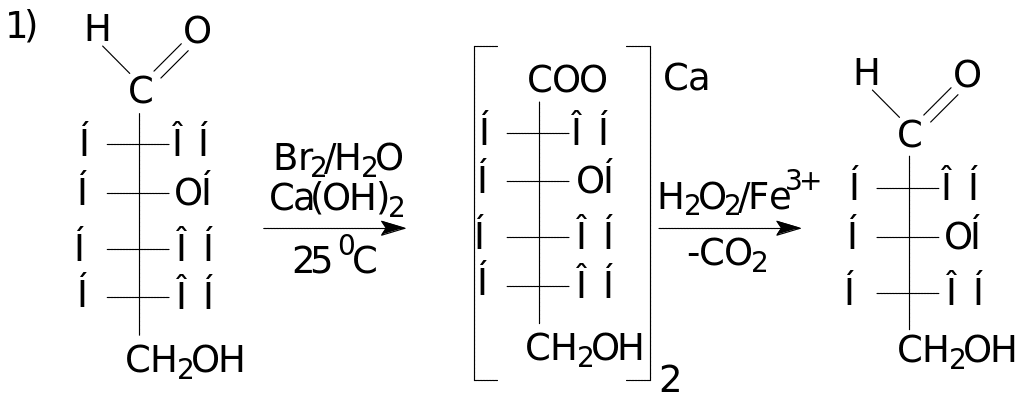
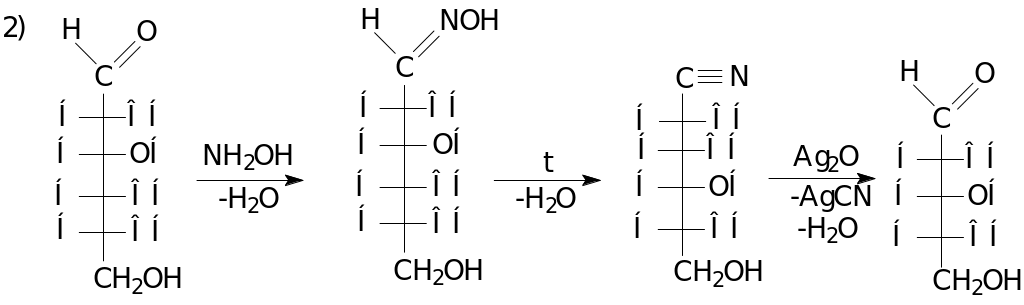
Химические свойства
Брожение
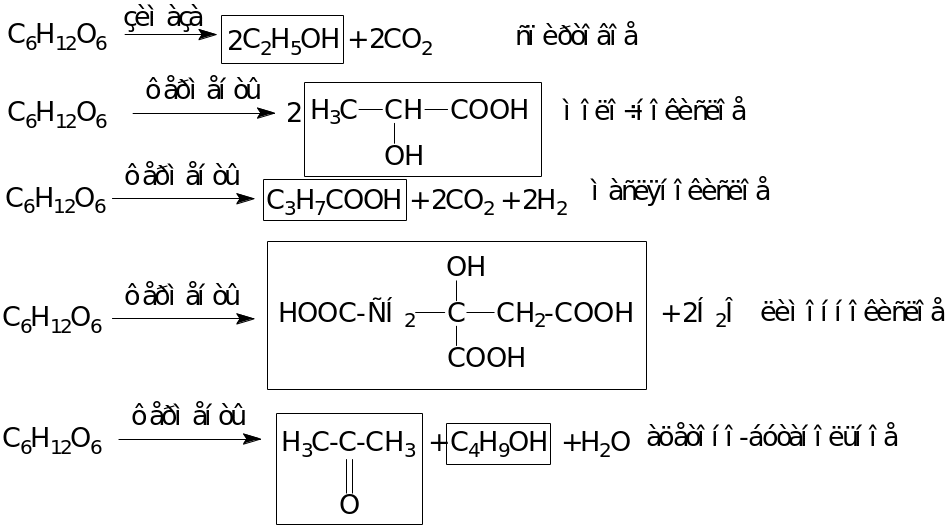
Восстанавливающие дисахариды

Невосстанавливающие дисахариды
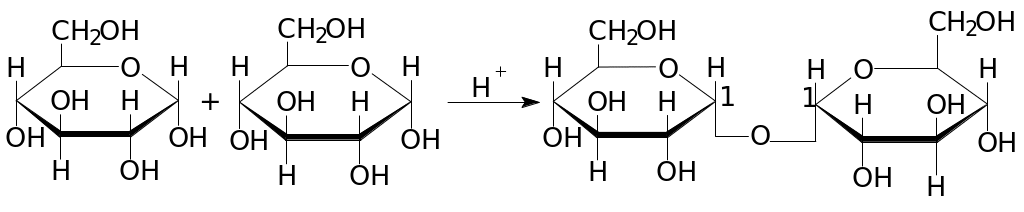
Химические свойства
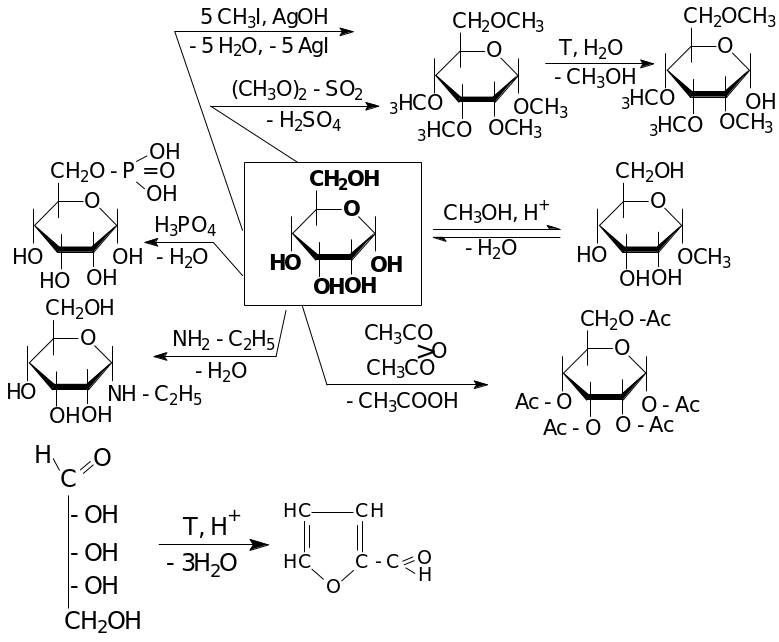
Если структура углевода нециклическая, то его химические свойства аналогичны свойствам спиртов и альдегидов:
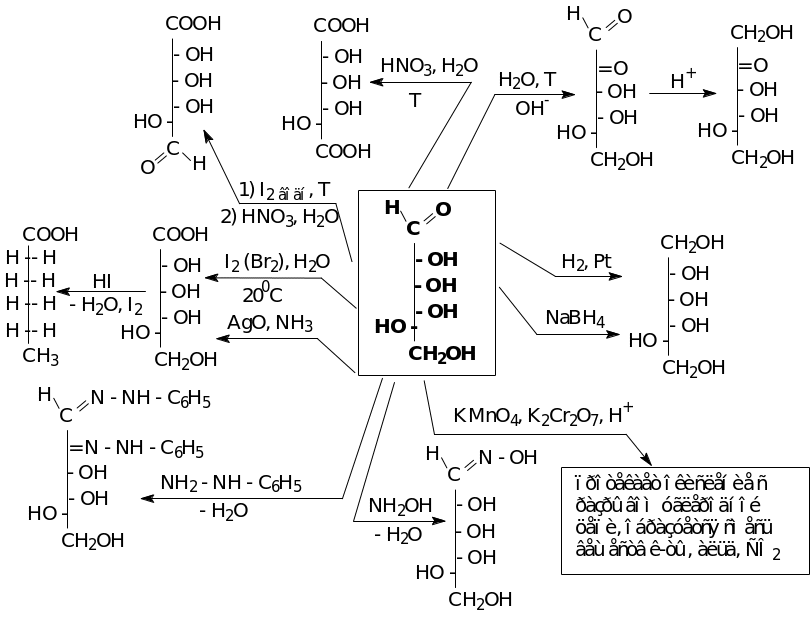
Мутаротация
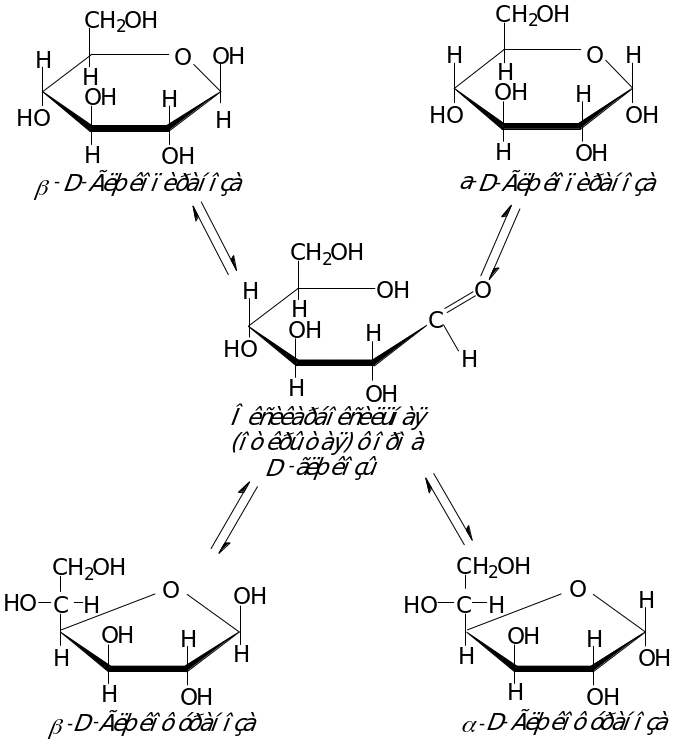
+ 112,2 0С + 52,7 0С + 18,7 0С
-глюкопираноза – 36 % -глюкопираноза
100 % – 64 % 100 %
АМИНЫ
Способы получения
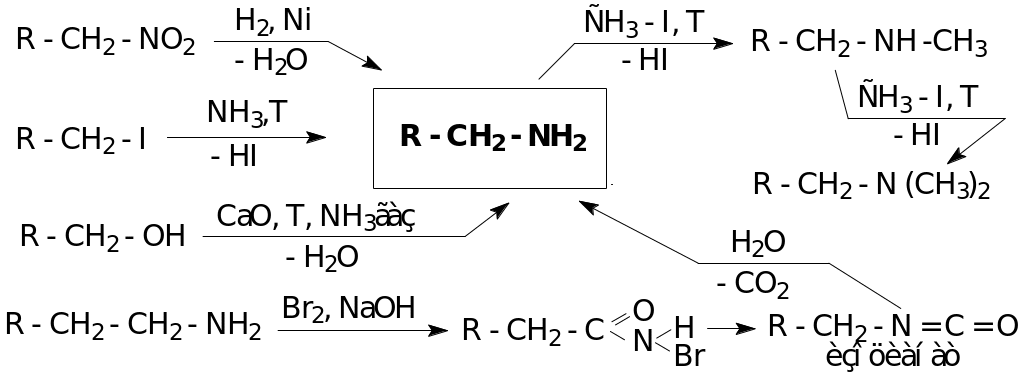
Химические свойства

АМИНОКИСЛОТЫ. БЕЛКИ
Способы получения
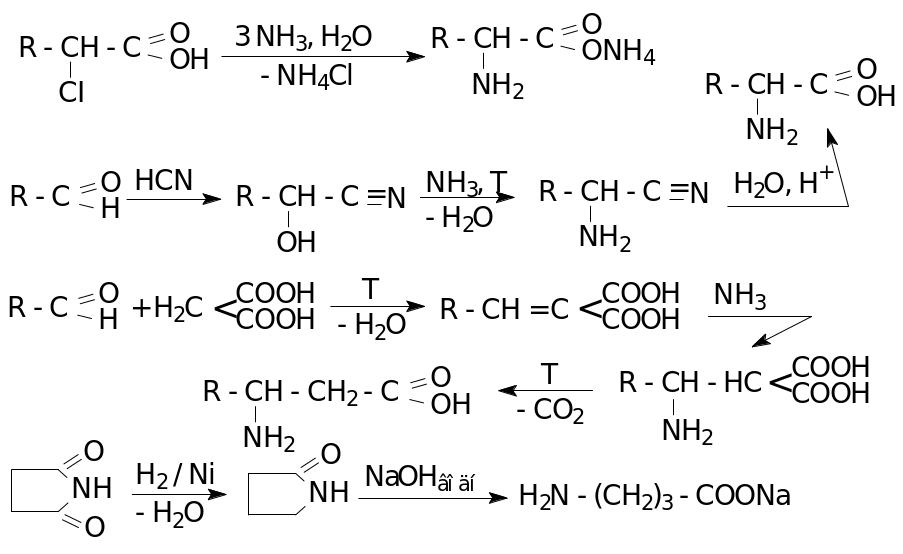
Химические свойства
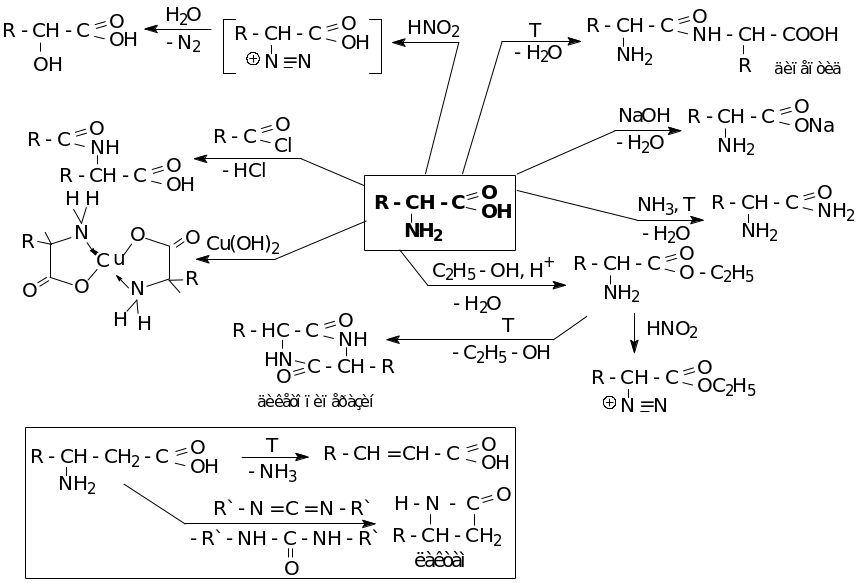
СПИСОК ЛИТЕРАТУРЫ
Рекомендуемая литература (основная):
В.В. Перекалин, С.А. Зонис. Органическая химия. М.: Просвещение, 1977.
Дж. Робертс, М. Кассерио. Основы органической химии. Т. 1 и 2. М.: Мир, 1978.
А. Терней. Современная органическая химия. М.: Мир, 1981.
О.А.Реутов, А.Л. Курц, К.П. Бутин. Органическая химия. Т.1-4, М. "Мир" 1999-2002 год.
Р.Моррисон, Р. Бойд. Органическая химия. М., "Мир", 1974 год.
А.Н.Несмеянов, Н.А.Несмеянов. Начала органической химии. Т. 1,2, М., "Мир", 1974.
А.А. Петров, Х.В. Бальян, А.Т. Трощенко. Органическая химия. М.: Химия, 1977.
О.Я. Нейланд. Органическая химия. М.: Высшая школа, 1990.
Лабораторные работы по органической химии. Под ред. О.Ф.Гинзбурга. М.: Высшая школа, 1970.
Н.В.Васильева и др. Органический синтез. М.: Просвещение, 1986.
Дополнительная литература:
J.Clayden, N.Greeves, S.Warren, P.Wothers. Organic Chemistry. Oxford Univ.Press. 2001.
А.С. Днепровский. Теоретические основы органической химии. Л.: Химия, 1979.
Дж. Марч. Органическая химия. Т. 1,2,3,4. М.: Мир, 1987.
П. Сайкс. Механизмы реакций в органической химии. М., "Химия", 1991 год.
В.М.Родионов, Б.М.Богословской, А.М.Федорова. Лабораторное руководство по химии промежуточных продуктов и красителей. М., 1948.
М.Н.Храмкина Практикум по органическому синтезу. Л.: Химия, 1974.
Воскресенский П.И. Техника лабораторных работ. Л.: Химия. 1970.
Берлин А.Я. Техника лабораторных работ в органической химии. М.:Химия. 1973.
Приложение 1
Таблица окончаний и приставок,
используемых в номенклатуре (IUPAC)
(приведены в порядке уменьшения старшинства)
| Класс | Формула | Префикс | Суффикс |
| Карбоновая к-та | -СООН | нет | -овая к-та |
| Сульфоновая к-та | -SO3H | сульфо- | -сульфоновая к-та |
| Сложный эфир | -СООR | R-оксикарбонил | R-карбоксилат |
| Галогенангидрид к-ты | -СО-Hal | галформил- | -оилгалид |
| Амид к-ты | -СО-NH2 | карбамоил- | амид к-ты. |
| Нитрилы | -СN | циано- | -нитрил (к-ты) |
| Альдегид | -СН=О | оксо- | -аль |
| Кетоны | С =О | оксо- | -он |
| Спирты, фенолы | -ОН | гидрокси- | -ол |
| Тиолы | -SH | меркапто- | -тиол |
| Галогенпроизводные углеводороды | Hal (-Br, -Cl, -F, -I) | бром-, хлор-, фтор-, йод- | нет |
| Нитрозо- | -NO | нитрозо- | нет |
| Нитро- | -NO2 | нитро- | нет |
| Амины | -NH2 | амино- | -амин |
| Имины | =NH | имино- | -имин |
| Эфиры простые | -OR | R-окси- | нет |
| Сульфиды | -SR | R-тио- | нет |
Приложение 2
Кислотность рКА некоторых органических кислот (Н2О, 25 0С)
| НСООН | 3,75 | СCl3-COOH | 0,08 |
| СН3СООН | 4,76 | CH3-CHCl-COOH | 2,80 |
| С2Н5СООН | 4,87 | CH2Cl-CH2-COOH | 4,10 |
| С3Н7СООН | 4,82 | HO-CH2-COOH | 3,83 |
| (СН3)3ССООН | 5,03 | HS-CH2-COOH | 3,55 |
| СН2F-COOH | 2,66 | NC-CH2-COOH | 2,44 |
| СН2Cl-COOH | 2,81 | O=CH-COOH | 3,30 |
| СН2Br-COOH | 2,87 | HOOC-CH2-COOH | 2,80 |
| СН2I-COOH | 3,13 | H2C=CH-COOH | 4,26 |
| СНCl2-COOH | 1,29 | C6H5-CH2-COOH | 4,31 |
Приложение 3
Альдозы D-ряда
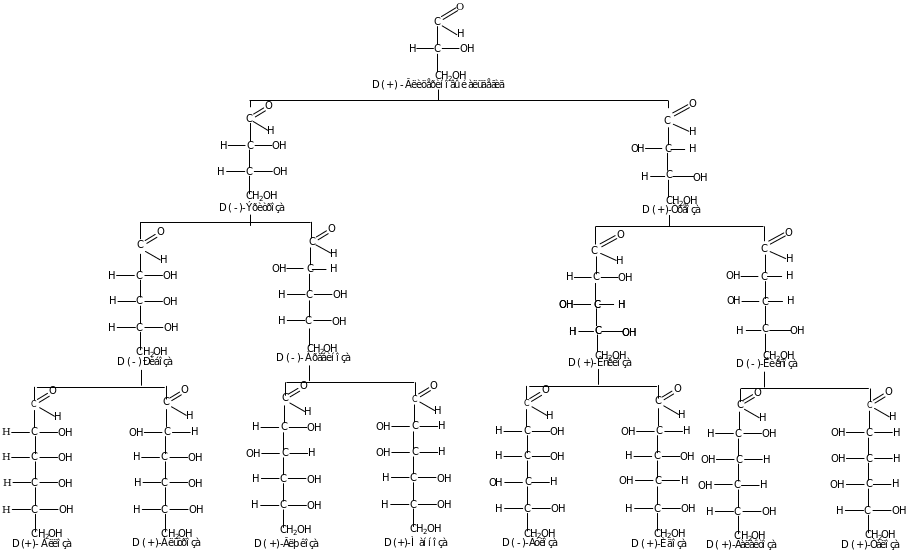
42







 Н3-
Н3-

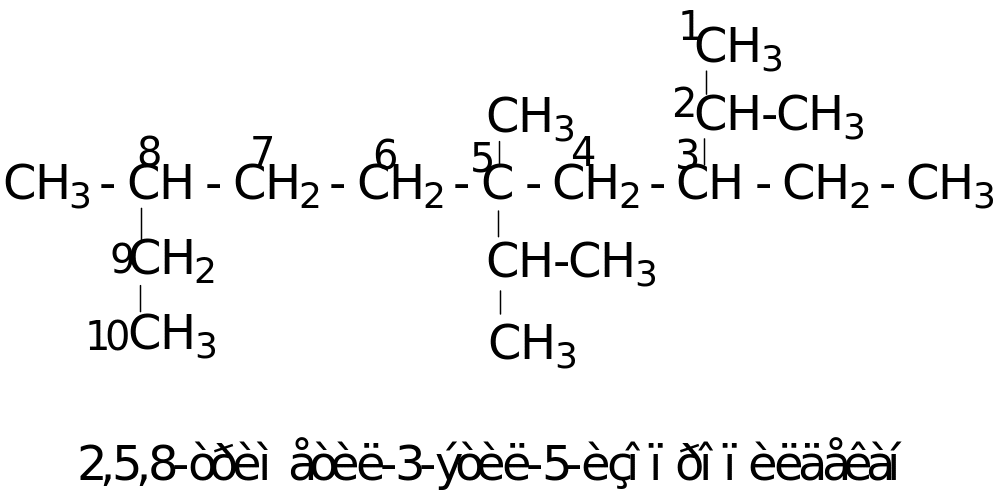
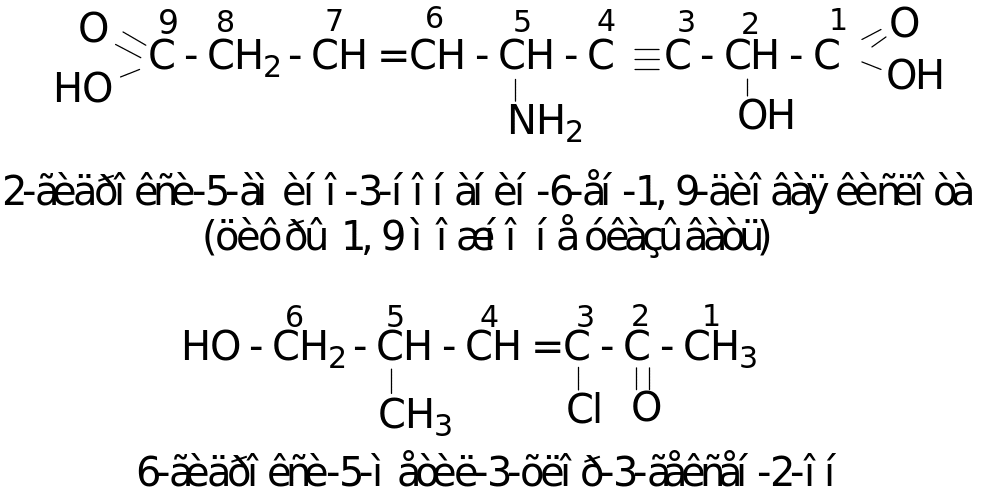
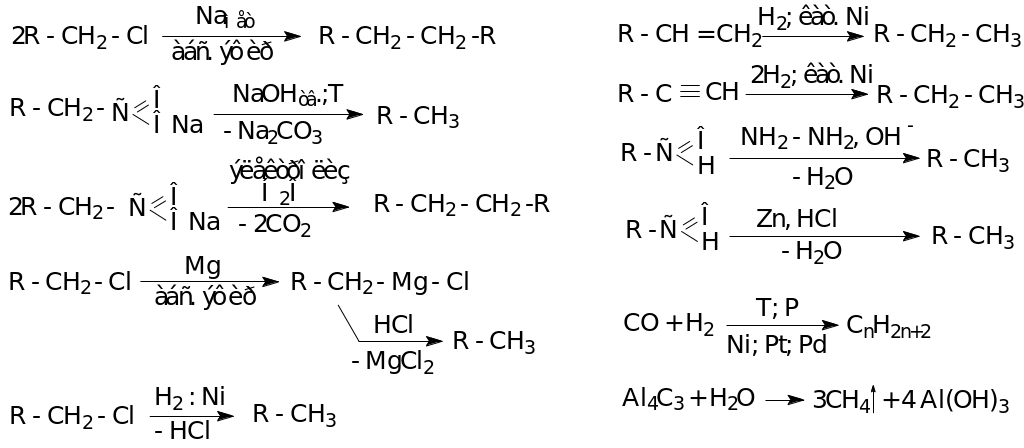






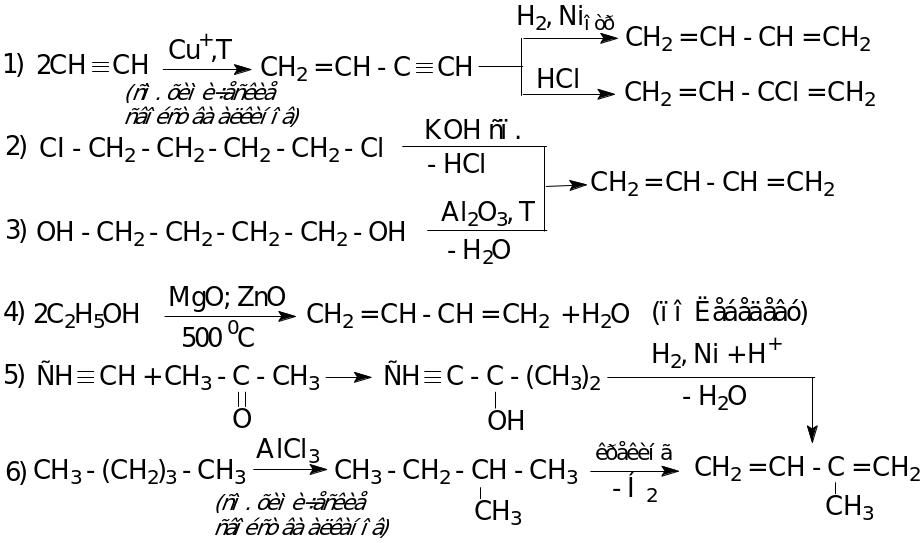

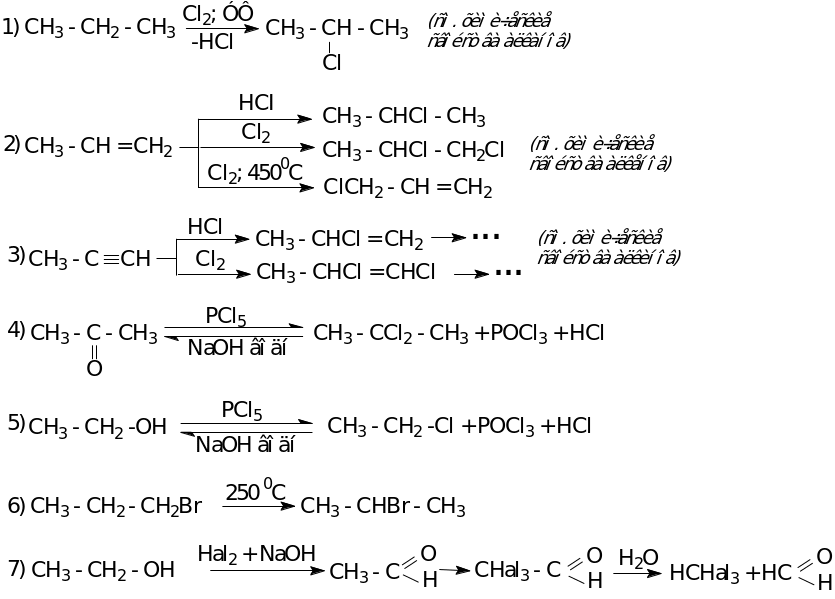





 Химические свойства
Химические свойства







 Кетонное расщепление ацетоуксусного эфира
Кетонное расщепление ацетоуксусного эфира