Просмотр содержимого документа
«Презентация к уроку "Химические свойства алкенов"»

Непредельные углеводороды АЛКЕНЫ
Химические свойства алкенов
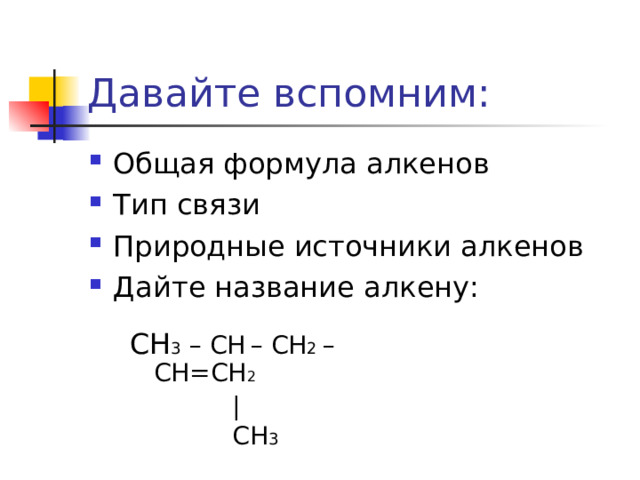
Давайте вспомним:
- Общая формула алкенов
- Тип связи
- Природные источники алкенов
- Дайте название алкену:
СН 3 – СН – CH 2 – CH=CH 2
|
CH 3

Проверьте себя:
- Общая формула алкенов С n H 2n , где n ≥2
- Тип связи двойная ( Ϭ - и π -связи)
- Природные источники алкенов нефть, газ
- Дайте название алкену:
5 4 3 2 1
СН 3 – СН – CH 2 – CH=CH 2
|
CH 3
4 – метилпент ен -1

Химические свойства
I. Реакции присоединения:
Почему для алкенов характерны именно реакции присоединения?
1.Гидрирование (присоединение водорода)
CH 2 =CH-CH 3 + Н-Н →
CH 3 -CH 2 -CH 3
пропен
пропан
Запишите уравнение реакции в молекулярном виде.
С 4 Н 8 + Н 2
С 4 Н 10

Химические свойства
I. Реакции присоединения:
Назовите простые вещества - галогены
2.Галогенирование (присоединение галогенов)
CH 2 =CH-CH 3 +C l-Cl →
CH 2 Cl-CHCl-CH 3
дихлорпропан
Запишите уравнение реакции в молекулярном виде.
С 6 Н 12 + Cl 2
С 6 Н 1 2 Cl 2

Химические свойства
I. Реакции присоединения:
Предположите: гидрогалогенирование – это …
3.Гидрогалогенирование (присоединение Н Hal )
CH 2 =CH-CH 3 +Н -Cl →
CH 3 -CHCl-CH 3
хлорпропан
Запишите уравнение реакции в молекулярном виде.
С 5 Н 10 + Н Cl
С 5 Н 11 Cl

Правило Марковникова
- Водород присоединяется к наиболее гидрогенизированному атому (т.е. туда, где уже больше водорода)
CH 3 -CH 2 -CH=CH 2 +Н- F →
CH 3 -CH 2 -CH F- CH 3
фторбутан
CH 3 -CH 2 -CH F- CH 3
CH 3 -CH=CH-CH 3 +Н- F →
CH 3 -CH F -CH 2 - CH 3
Химические свойства
I. Реакции присоединения:
Вспомните: на что распадается Н 2 О
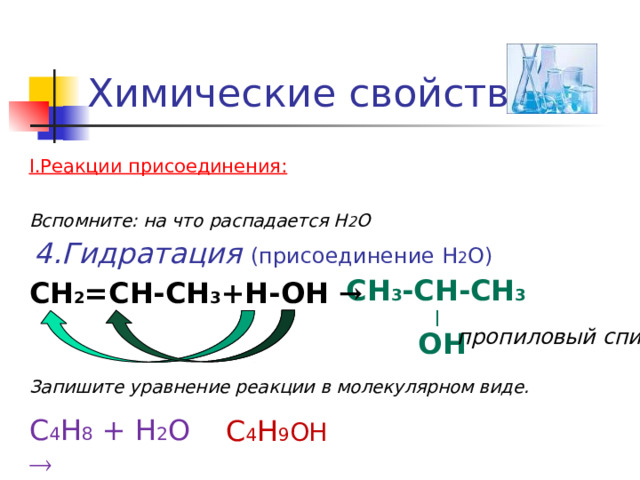
4.Гидратация (присоединение Н 2 О)
CH 3 -CH-CH 3
|
ОН
CH 2 =CH-CH 3 +Н - ОН →
пропиловый спирт
Запишите уравнение реакции в молекулярном виде.
С 4 Н 8 + Н 2 О
С 4 Н 9 ОН

Химические свойства
I. Реакции присоединения:
5.Полимеризация (присоединение друг к другу)
-( CH 2 -CH ) -
|
CH 3
n CH 2 =CH-CH 3 →
полипропилен
Можно ли записать уравнение реакции в молекулярном виде?
-( CH-CH ) -
| |
CH 3 CH 3
n CH 3 -CH=CH-CH 3 →
полибутен

Химические свойства
II. Реакции окисления:
1.Полное окисление (горение):
Вспомните, что выделяется при горении углеводородов?
3 О 2 → 2 СО 2 + 2 Н 2 О
С 2 Н 4 +
9 О 2 → 6 СО 2 + 6 Н 2 О
С 6 Н 12 +

Химические свойства
II. Реакции окисления:
2.Неполное окисление :
3 С 2 Н 4 + 2 KMnO 4 + 4 Н 2 О → → 3 HOCH 2 -CH 2 OH+ 2 MnO 2 + 2 KOH
этилен
перманганат калия
этиленгликоль
Качественная реакция на двойную связь :
обесцвечивание перманганата калия

Обесцвечивание перманганата калия

Оцените себя:
- 9-10 «+» = 5
- 7-8 «+» = 4
- 5-6 «+» = 3

C пасибо за внимание!
Домашнее задание
Применение этилена
(сообщение или презентация)






























