Технологическая карта урока по химии в 8-ом классе
на тему «Бинарные соединения»
| ПЛАНИРУЕМЫЕ ОБРАЗОВАТЕЛЬНЫЕ РЕЗУЛЬТАТЫ |
| Предметные | Метапредметные | Личностные |
| Умения определять понятия «бинарные соединения», составлять формулы и названия бинарных соединений; описывать свойства отдельных представителей бинарных соединений, умение использовать «электро-отрицательность», «валентность», «степень окисления», «ряд ЭО химических элементов». | Умения использовать знаково-символические средства для решения задач; проводить наблюдение; создавать обобщения, устанавливать аналогии, осуществлять классификацию, делать выводы, составлять проект, выступать перед аудиторией
| Понимание значимости естественнонаучных знаний в повседневной жизни, технике, медицине, для решения практических задач. Умение грамотно обращаться с веществами в химической лаборатории и в быту
|
| Цели урока | Определять бинарные соединения; Называть бинарные соединения; Писать формулы бинарных соединений |
| Авторы УМК: | Химия. 8 класс : учебник-навигатор/ О.С Габриелян, В.И.Сивоглазов, С.А. Сладков. – 6-е издание стереотип. - М. : Дрофа, 2018. 190 с. |
| Основные понятия, изучаемые на уроке | Бинарные соединения, степень окисления, валентность, электроотрицательность |
| Оборудование
| Образцы бинарных соединений, шаростержневые модели бинарных соединений. |
| Образовательные ресурсы
| Универсальные (электронные книги, компьютер, проектор) |
| ОРГАНИЗАЦИОННАЯ СТРУКТУРА УРОКОВ |
| 1. Этап мотивации (самоопределения) к учебной деятельности. 2. Этап актуализации и фиксирования индивидуального затруднения в пробном действии. Диалог на уроке |
| Формирование конкретного образовательного результата /группы результатов | Внутренняя и внешняя оценка результатов, обнаружение субъективного незнания
|
| Длительность этапа
| 5-7 минут |
| Основной вид учебной деятельности, направленный на формирование данного образовательного результата | Внутренняя и внешняя оценка результатов учебной деятельности. Фронтальные устные ответы на вопросы учителя
|
| Методы обучения | Систематизирующая беседа |
| Форма организации деятельности обучающихся | Индивидуальная и коллективная мыслительная деятельность
|
| Функция / роль учителя на данном этапе | Организаторская, корректирующая. Учитель корректирует ответы обучающихся |
| Основные виды деятельности учителя
| Коррекция, координация деятельности обучающихся
|
| ЭТАП 3. Организация и самоорганизация обучающихся в ходе дальнейшего усвоения материала Работа в группа |
| Формирование конкретного образовательного результата / группы результатов | Умение систематизировать изученный и новый материал. Умение составлять формулы и названия бинарных соединений и описывать их свойства
|
| Длительность этапа | 25—30 минут |
| Основной вид учебной деятельности, направленный на формирование данного образовательного результата | Самостоятельное выполнение заданий в группах.
|
| Методы обучения | Самостоятельная групповая работа с последующей само- и взаимопроверкой и коррекцией допущенных ошибок |
| Форма организации деятельности обучающихся | Индивидуальная и коллективная мыслительная деятельность
|
| Функция / роль учителя на данном этапе | Организаторская, контролирующая, корректирующая |
| Основные виды деятельности учителя | Координация, контроль, коррекция (случае необходимости) деятельности обучающихся |
| ЭТАП 4. Подведение итогов, домашнее задание
|
| Формирование конкретного образовательного результата /группы результатов | Обобщение. Устный ответ на проблемный вопрос уроков
|
| Длительность этапа | 3—5 минут |
| Форма организации деятельности обучающихся | Индивидуальная, коллективная
|
| Функция / роль учителя на данном этапе | Организация самоконтроля обучающихся с последующей самооценкой |
| Основные виды деятельности учителя | Координирует деятельность обучающихся
|
| Рефлексия по достигнутым или недостигнутым образовательным результатам
| Обучающиеся оценивают свою работу на уроке, выполняют взаимную проверку, учитель выставляет отметки за конкретные виды работы обучающимся на основе их самооценки. Дифференцированное домашнее задание с комментариями. |
ХОД УРОКА
1. Этап мотивации (самоопределения) к учебной деятельности.
Вопросы и задания
Какие классы веществ вы знаете? Чем отличаются простые вещества от сложных? Что объединяет эти вещества? (слайд 1)
Углекислый газ
Вода
Галенит, свинцовый блеск
2. Этап актуализации и фиксирования индивидуального затруднения в пробном действии.
Смогли определить, что объединяет эти вещества? Для подсказки давайте вспомним молекулярные формулы данных веществ (слайд 2)
Углекислый газ – СО2
Вода - Н2О
Сероводород - Н2S
(Учащиеся определили, что в состав данных соединений входят атомы 2-х элементов, такие соединения называются - бинарные соединения. Учащиеся сообщают тему урока, формулируют определение бинарных соединений) (слайд 3).
Ребята, как вы думаете, какие учебные задачи мы будем решать на уроке, изучая бинарные соединения?
Учащиеся определяют учебные задачи.
Я сегодня научусь:
Определять бинарные соединения;
Называть бинарные соединения;
Писать формулы бинарных соединений.
Ребята, решать эти задачи на уроке мы будем индивидуально и по парам.
Для работы вам нужно вспомнить материалы предыдущих уроков. Учитель организует работу с понятиями «электроотрицательность (ЭО)», «валентность», «степень окисления», «ряд ЭО химических элементов». Учащиеся дают определения (слайд 3).
Электроотрицательность (ЭО)– способность атома в молекуле смещать к себе электронные пары
Ряд ЭО химических элементов:

Валентность – способность атома образовывать определенное число химических связей
Степень окисления – условный заряд атома в соединении.
3. Этап организации и самоорганизации обучающихся в ходе дальнейшего усвоения материала. Работа в группах.
Формирование умения составлять формулы и названия бинарных соединений; описывать свойства отдельных представителей оксидов и летучих водородных соединений.
Новый учебный материал раскрывается с опорой на содержание параграфа по учебнику «Химия» в 8 классе, авторы: О.С.Габриелян, В.И.Сивоглазов, С.А.Сладков и текстовые задания (См. приложения).
1 задание
Выберите формулы соединений, относящиеся бинарным соединениям.
CaCl2 O2 H2CO3 HCl SO2 KNO3 H2O
Привести свои три примера бинарных соединений …………………………………
Дать веществам названия.
2 задание
Изучите правила составления названий бинарных соединений (См. опорные схемы. Приложение). Дайте названия следующим соединениям:
| KCl - CaS - Mg3N2 - Al4C3 - Na2O - NaH - | Mg3P2 - NaF - Al2S3 - BaI2 - CaH2 - LiBr - |
(слайд 5-6).
3 задание
Определите степени окисления химических элементов в бинарных соединениях и дайте им названия. Используйте в ответе таблицы №3.
| CaBr2 - MgS - P2O5 - Na2S - | KF - Li3N - SO3 – FeCI3 - |
ПОМНИТЕ, что в названиях бинарных соединении с элементом с постоянной валентностью (степенью окисления) в названии не указывается валентность. Пример: Na2O - оксид натрия.
В бинарном соединений с переменной валентностью в названии указывают валентность в конце названия в скобках в виде римской цифры. Пример: Fe+2O-2 – оксид железа (II), Fe2+3O3-2 - оксид железа (III), (слайд 7-8).
4 задание
Работа с текстом (приложение).
Решите задание. Напишите химическую формулу хлорида натрия. Найдите степени окисления и валентности химических элементов, составьте структурную и шаро-стержневую модель молекулы соли.
ПОМНИТЕ! Формулы бинарных соединений записываются в следующем порядке: вначале элемент с положительной степенью окисления Са+2, а затем элемент с отрицательной степенью окисления O-2. Пример: Са+2О-2 (исключением из правил являются гидриды неметаллов: С-4Н+14 - СН4, N-3H+13 - NH3).
Когда дается название соединению сначала называют латинское название элемента с отрицательной степенью окисления в родительном падеже с добавлением суффикса: -ид, а затем название элемента с положительной степенью окисления в именительном падеже: Са+2О-2 – оксид кальция.
После каждого этапа работы учащиеся оценивают свою деятельность (приложение 4). В середине урока проводится физминутка.
4. Этап первичного закрепления с проговариванием во внешней речи. Публичные выступления групп. Учащиеся внимательно слушают выступление групп, задают вопросы.
5. Этап рефлексии учебной деятельности на уроке.
Организуется рефлексия и самооценка учениками собственной учебной деятельности на уроке. Учащиеся соотносят цель и результаты своей учебной деятельности и фиксируют степень их соответствия. Намечаются цели дальнейшей деятельности и определяются задания для самоподготовки (дифференцированное домашнее задание с элементами выбора, творчества) (приложение 4,5).
Домашнее задание: § 19, выполнить задания по выбору:
Минимальный уровень
1. По формулам определите бинарные соединения: К2О, KCI, NO2, HNO3, КОН, MgSO4, HCI, CuSO4, Са(ОН)2. Выпишите их.
Общий уровень
1. По названиям веществ определите бинарные соединения: серная кислота, оксид магния, хлорид железа (III), нитрат алюминия, оксид кальция, азотная кислота, сульфат калия. Напишите формулы этих соединений.
Продвинутый уровень
1. Используя Периодическую систему химических элементов Д.И. Менделеева, составьте формулы пяти бинарных соединений. Укажите степени окисления элементов.
Назовите вещества.
2. Определите степени окисления элементов в соединениях по их формулам: Na2S, CuO, SiH4, СO2, Ba3N2.
Приложение 1
Маршрутный лист Дата: Класс:
| Распределение ролей в группе | Лидер - _________________ (отвечает за работу группы в целом) Секретарь - ____________(записывает идеи и решения) Критик - __________________ (высказывает противоположную точку зрения, приводит новые идеи) Дизайнер - ______________ (дополняет рисунком, схемой, художественно оформляет работу) Чтец - __________________(читает вслух) |
| В группе я сегодня научусь:
| Определять БС; Называть БС; Писать формулы БС. |
| Тема учебного проекта | Бинарные соединения (БС) |
| Проблема |
|
| Цель учебного проекта |
|
| Проектный продукт | Опорная схема по теме «Бинарные соединения» |
| План работы над проектом | 1) 2) 3) 4) |
| РАБОТА ГРУППЫ НАД ПРОЕКТОМ |
| Достигла ли цели группа? |
|
| Где можно использовать ваш проектный продукт? Что в основу взяли? Будет ли интересен и понятен для других? |
|
| Какой другой вариант проектного продукта можете предложить для работы по данной теме урока? |
|
| ОТВЕЧАЕТ ЛИДЕР: Как вы оцениваете работу группы в целом? Какую работу проделал каждый член группы при оформлении проектной работы? Кто хорошо справился со своей ролью, кто не очень? |
|
П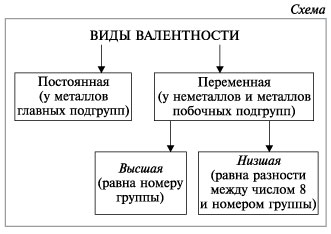 риложение 2. Опорные схемы.
риложение 2. Опорные схемы.
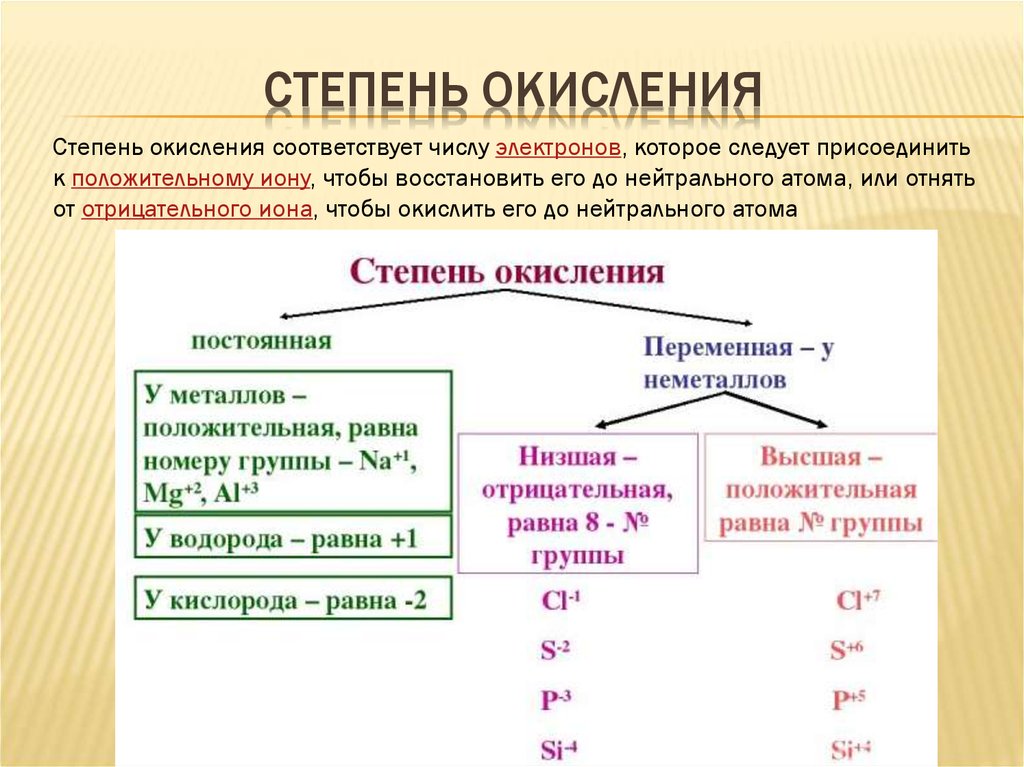

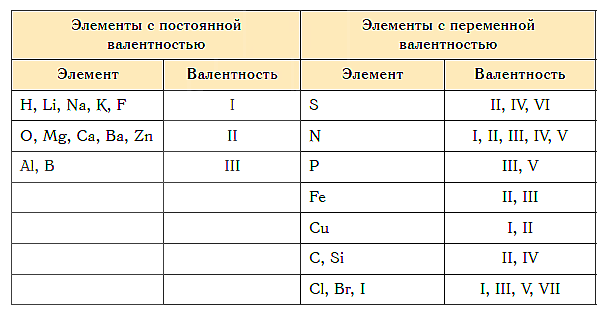

4 задание
Прочитайте текст.
Кремнезем, опал, яшма, сердолик, кварц – вот некоторые красивые названия минералов, которые образует соединение, имеющее химическое название - оксид кремния (IV). Оксид кремния используется в химической промышленности, строительстве, медицине. Производство стекла, цемента, изготовление фаянсовых и фарфоровых изделий, кирпича – это отрасли керамического производства. Галька, речной песок – незаменимые строительные материалы, а также они используются при укладке асфальта. Минералы оксида кремния используются как поделочные камни в изготовлении ювелирных изделий, кварц – при изготовлении кварцевых ламп.
Решите задание. Напишите химическую формулу оксида кремния (IV). Найдите степени окисления и валентности химических элементов, составьте структурную и шаро-стержневую модель молекулы оксида кремния (IV).
ПОМНИТЕ! Формулы бинарных соединений записываются в следующем порядке: вначале элемент с положительной степенью окисления Са+2, а затем элемент с отрицательной степенью окисления O-2. Пример: Са+2О-2 (исключением из правил являются гидриды неметаллов: С-4Н+14 - СН4, N-3H+13 - NH3).
Когда дается название соединению сначала называют латинское название элемента с отрицательной степенью окисления в родительном падеже с добавлением суффикса: -ид, а затем название элемента с положительной степенью окисления в именительном падеже: Са+2О-2 – оксид кальция.


Приложение
Оцени себя Ф.И._________________________________
| № | Задания | Поставь себе баллы, если… |
| Сделал (а) без ошибок - 3 балла | допустил (а) 1-2 ошибки – 2 балла | допустил (а) 3 и более ошибок - 1 балл |
| 1 | Задание на определение формулы соединений, относящиеся БС |
|
|
|
| 2 | Задание на составление названий БС. |
|
|
|
| 3 | Определение степени окисления по химическим формулам БС. |
|
|
|
| 4 | Составление химической формулы БС. |
|
|
|
|
| Итого (найди сумму баллов) и ставь отметку: 11-12 баллов – «5» 9-10 баллов – «4» 7-8 баллов – «3» |
|
Приложение
Рефлексия









 риложение 2. Опорные схемы.
риложение 2. Опорные схемы. 
















