
Исследовательская работа
«Газовые законы»
Газовые законы представляют собой фундаментальные законы физики, которые описывают поведение газов в различных условиях. Эти законы были открыты и сформулированы в XIX веке и с тех пор нашли широкое применение в различных научных и практических областях, таких как физика, химия, инженерия, метрология и многие другие.
Цель работы – исследование газовых законов теоретически и уравнения состояния, проверка их выполнения с помощью опытов.
Задачи:
- Изучить основные термины и определения молекулярной физики, связанных с изучением газовых законов.
- Познакомиться с историей открытия газовых законов.
- Изучить график изопроцесса.
- Заполнить систематизирующую таблицу по изопроцессам.
- Провести практическую работу по исследованию газовых законов.
Область исследования – молекулярная физика.
Предмет исследования – идеальный газ, газовые законы.
Изучение газовых законов имеет практическую ценность во многих областях жизнедеятельности человека, например, в образовании: изучение газовых законов имеет огромное значение для образования студентов в области физики, химии и техники, а также для учащихся средних школ.
Таким образом, изучение газовых законов имеет огромную практическую ценность и является основой для понимания и работы с газовыми процессами.

1. Закон Бойля-Мариотта
2. Закон Шарля
3. Закон Гей-Люссака
Обобщение газовых законов
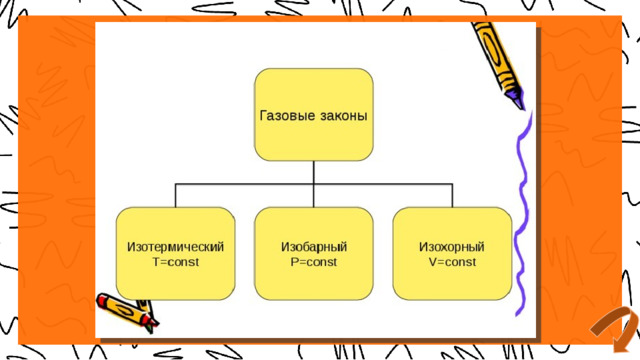

1. Закон Бойля-Мариотта
История открытия закона
Биография Мариотта
Формулиро-вка закона
Биография Бойля
График изопроцесса
Эксперимент

Бойль Роберт (1627—1691), английский химик и физик.
Родился 25 января 1627 г. в замке Лисмор (графство Уотерфорд, Ирландия).
В восемь лет поступил в колледж в Итоне.
В 1638 г. Бойль вместе с наставником отправился в путешествие по странам Европы, учился во Флоренции и в Женеве.
В 1662 г. открыл закон изменения объёма воздуха с изменением давления, который независимо от него установил в 1676 г. французский физик Э. Мариотт (закон Бойля — Мариотта).
Умер 31 декабря 1691 г. в Лондоне.

Эдм Мариотт (1620 г. – 12 мая 1684 г.)
Эдм Мариотт – французский физик, один из основателей (1666) и первых членов Парижской академии наук. Родился в Дижоне. Был настоятелем монастыря Святого Мартина близ Дижона.
Научные работы относятся к механике, теплоте, оптике. В 1676 г. установил закон изменения объёма данной массы газа от давления при постоянной температуре (закон Бойля – Мариотта; этот закон был открыт и опубликован в 1662 г. Р. Бойлем).

Закон Бойля — Мариотта, один из основных газовых законов, который описывает изотермические процессы в идеальных газах. Его установили учёные Р. Бойль в 1662 г. и Э. Мариотт в 1676 г. независимо друг от друга при экспериментальном изучении зависимости давления газа от его объема при постоянной температуре.

Во второй половине XVII в. в Европе началась промышленная революция, которая подстегнула новые научные открытия. Так, в связи с добычей полезных ископаемых требовались насосы для откачивания воды из шахт. Фабрики по производству тканей нуждались в паровых машинах, которые приводили бы в движение станки. Это побудило ученых приступить к тщательному изучению газа — в широком смысле слова.
А началось все с научного спора. Блез Паскаль и Отто фон Герике опытным путем пытались доказать, что воздух упругий.
Предметом этих дебатов заинтересовался англичанин Роберт Бойль (1627—1691). Поддерживая идеи Паскаля и Герике, он сам провел серию экспериментов с выкачиванием воздуха из сосуда (для чего предварительно усовершенствовал насос, изобретенный Р. Гуком) и сделал несколько чудесных открытий.
Бойль первым сказал, что нас окружает смесь разных газообразных веществ.

Два года спустя ученый и его помощник Ричард Таунли определили, что давление газа увеличивается ровно настолько, насколько уменьшается его объем, а значит, если измерить объем емкости с газом, то можно вычислить силу, с которой он давит на стенки сосуда.

Все свои опыты Бойль детально изложил в трудах, которые были изданы во всех странах Европы, а 15 лет спустя вышла книга «Речь о природе воздуха», написанная французским аббатом Эдмом Мариоттом (1620—1684).
Аббат рассказывал о якобы проведенных им экспериментах, точь-в-точь повторяющих исследования Бойля, однако имени английского ученого не называл, словно хотел присвоить его славу себе.
Между тем труд француза сильно проигрывал работе Бойля.
Тем не менее именно Мариотт указал на практическое применение данного закона — к примеру, предложил использовать показания барометра для определения высоты.

Формулировка закона Бойля-Мариотта
(изотермический процесс)
=
pV = const
T = const
Для газа данной массы произведение давления газа на его объем постоянно, если температура газа не меняется

Изотермический процесс

Доказательство

Изотерма на -диаграмме — это график обратно пропорциональной зависимости
Такой график является гиперболой (график функции ). Изотерма-гипербола изображена на рисунке.

Эксперимент

2. Закон Шарля
История открытия закона
Формулиро-вка закона
Биография Шарля
График изопроцесса
Эксперимент

Жак Александр Сезар Шарль родился в небольшом городке Божанси, расположенном в Луаре, Франция, 12 ноября 1746 года.
В юности он переехал в Париж, где одной из его первых должностей была небольшая должность в финансовом офисе городского министерства финансов, которую он занимал до тех пор, пока правительственный кризис не заставил его уволиться.
Продолжая свое направление исследований, основанное на поведении газов, Жак Шарль сформулировал закон, который в настоящее время известен как закон Чарльза или закон идеального газа.
Причины смерти этого известного ученого неизвестны, но известно, что Жак Шарль умер в Париже 7 апреля 1823 года.

Когда стали известны опыты Б. Франклина с молнией, Шарль повторил их с изменениями – настолько интересными, что сам Франклин приехал познакомится с ним и похвально отозваться о его способностях. Шарль построил воздушный шар из прорезиненной ткани и первым использовал для его наполнения водород. В 1783 году осуществил полет на этом шаре.

В 1787 французский учёный Жак Шарль измерил давление различных газов при нагревании при постоянном объёме и установил линейную зависимость давления от температуры, но не опубликовал исследования. Через 15 лет к таким же результатам пришел Гей-Люссак и, будучи на редкость благородным настоял, чтобы закон был назван в честь его первооткрывателя- Жака Шарля.

Формулировка закона Шарля
(изохорный процесс)
=
= const
V = const
Для газа данной массы при постоянном объеме отношение давления газа к его термодинамической температуре постоянно.

Изохорный процесс
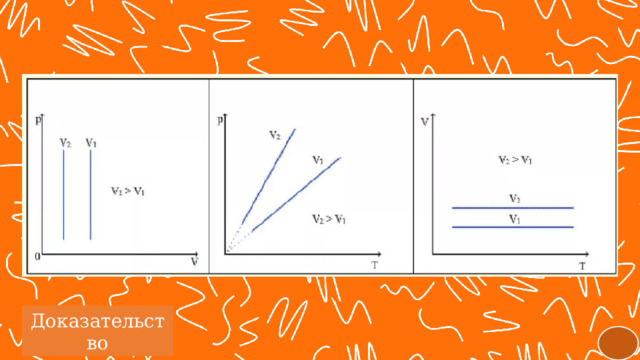
Доказательство

Фиксируем температуру и видим, что . Но при фиксированной температуре давление тем меньше, чем больше объём. Стало быть, .

Эксперимент

3. Закон Гей-Люссака
История открытия закона
Формулиро-вка закона
Биография Гей-Люссака
График изопроцесса
Эксперимент

Жозеф Луи Гей-Люссак (фр. Joseph Louis Gay-Lussac) родился 6 декабря 1778 года в Сен-Леонар-де-Нобла. В 15 лет он отправляется для обучения в Париж, в пансионат Сансье. В 19 лет начинает учиться в Политехнической школе в Париже.
После окончания Политехнической школы работает ассистентом Бертолле. В 1809 году получает звание профессора химии в Политехнической школе и одновременно профессора физики в Сорбонне.
В 1802 году Гей-Люссак открывает один из главных газовых законов — закон теплового расширения газов, позже названный в его честь.
Жозеф Луи Гей-Люссак скончался 9 мая 1850 года в Париже на 72-м году жизни.

В 1802 г. независимо от Джона Дальтона Гей-Люссак открыл один из газовых законов – закон теплового расширения газов, позже названный его именем. В 1804 г. он совершил два полёта на воздушном шаре (поднявшись на высоту 4 и 7 км), во время которых выполнил ряд научных исследований, в частности измерил температуру и влажность воздуха. В 1805 г. совместно с немецким естествоиспытателем Александром фон Гумбольдтом установил состав воды, показав, что соотношение водорода и кислорода в её молекуле равно 2:1.

В 1808 г. Гей-Люссак открыл закон объёмных отношений, который представил на заседании Философско-математического общества: «При взаимодействии газов их объёмы и объёмы газообразных продуктов соотносятся как простые числа». В 1809 г. он провел серию опытов с хлором, подтвердивших вывод Гэмпфри Дэви, что хлор – это элемент, а не кислородсодержащее соединение, а в 1810 г. установил элементарный характер калия и натрия, затем фосфора и серы. В 1811 г. Гей-Люссак совместно в французским химиком-аналитиком Луи Жаком Тенаром значительно усовершенствовал метод элементного анализа органических веществ. В 1811 г. Гей-Люссак начал обстоятельное исследование синильной кислоты, установил её состав и провёл аналогию между нею, галогеноводородными кислотами и сероводородом. В 1811-1813 гг. Гей-Люссак установил аналогию между хлором и иодом, получил иодистоводородную и иодную кислоты, монохлорид иода. В 1815 г. он получил и изучил «циан» (точнее говоря, дициан), что послужило одной из предпосылок формирования теории сложных радикалов.

Стеклянную трубку с резервуаром, в котором был исследуемый газ, он помещал в нагреватель. Газ «закупоривался» маленькой капелькой ртути в трубке, размещенной горизонтально. Таким образом, давление газа в резервуаре всегда равнялось атмосферному. Температура газа в резервуаре с помощью нагревателя изменялась от 0 до 100°С. Изменение объема газа от V 0 (при t 0 = 0) до V при неизменном давлении фиксировалось благодаря перемещению капельки ртути. Обобщив экспериментальные данные, Гей-Люссак установил, что с изменением температуры при постоянном давлении относительный объем данной массы газа изменяется линейно. На основании наблюдений он сформулировал утверждение, названное в его честь законом Гей-Люссака.

При постоянном давлении относительное изменение объема газа данной массы прямо пропорционально изменению температуры: = αΔt, где Δt — изменение температуры; V — объем газа при определенной температуре t. Коэффициент пропорциональности α называется температурным коэффициентом объемного расширения. Расчета показали, что все разреженные газы при нагревании на 1°C или 1 K изменяют свой объем приблизительно на частицу от начального объема: ≈

Закон Гей-Люссака приобретет более простую форму, если его выразить через абсолютную температуру. Поскольку 1 + αt = 1 + • (T — 273) = αТ, то V = V 0 αT. Таким образом, при постоянном давлении объем данной массы газа прямо пропорциональный абсолютной температуре. Закон Гей-Люссака утверждает, что в изобарном процессе отношение объемов данной массы газа в разных состояниях равно отношению абсолютных температур газа в этих состояниях:

Формулировка закона Гей-Люссака
(изобарный процесс)
=
= const
P = const
Для газа данной массы при постоянном давлении отношение объема газа к его температуре постоянно.

Изобарный процесс

Доказательство

Мы видим, что . Но при фиксированной температуре объём тем меньше, чем больше давление. Стало быть, .

Эксперимент

В заключении исследовательской работы, посвященной газовым законам, можно сказать, что это важная и интересная область физики, которая изучает свойства газов и их поведение при различных условиях в различных системах.
В результате проведенного исследования мы изучили три главных газовых закона: закон Бойля-Мариотта, закон Шарля и закон Гей-Люссака. Эти законы описывают зависимость объема, давления и температуры газа друг от друга, что позволяет сделать выводы о его поведении в различных условиях.
Также был проведен ряд экспериментов, которые подтвердили верность этих законов и позволили нам более глубоко понять, как газовые законы работают и как они могут быть применены на практике.
Знание газовых законов является необходимым для многих научных и технических областей, таких как аэродинамика, химическая промышленность и многие другие. Это позволяет создавать и проектировать новые процессы и технологии, которые могут улучшить жизнь людей.
Поставленная цель в начале работы была достигнута. Задачи выполнены.
Таким образом, исследование газовых законов имеет большое значение для научного и технического прогресса и представляет собой важную область изучения физики.





















































