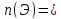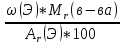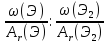| Основные величины для решения задач |
| Mr | относительная молекулярная масс вещества |
| 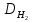
| относительная плотность паров вещества по водороду |
| 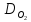
| относительная плотность паров вещества по кислороду |
| Dвозд | относительная плотность паров вещества по воздуху |
| 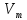
| молярный объем (постоянная величина 22,4 л/моль) |
| 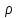
| плотность вещества |
| ω(Э) | массовая доля элемента |
| 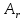
| относительная атомная масса элемента |
| 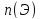
| количество атомов химического элемента в сложном веществе |
ЗАДАЧИ.
Выведите формулу вещества, содержащего 82,75% углерода и 17,25% водорода. Относительная плотность паров этого вещества по воздуху равна 2.
Выведите формулу вещества, содержащего 81,8% углерода и 18,2% водорода, если относительная плотность по водороду равна 22.
Выведите молекулярную формулу углеводорода, содержащего 85,71% углерода и 14,29% водорода. Относительная плотность паров этого вещества по водороду равна 21.
Определите молекулярную формулу углеводорода с массовой долей углерода 85,7%. Относительная плотность данного вещества по водороду равна 14.
Вычислите относительную молекулярную массу и его формулу, если массовая доля в нем углерода равна 92,3%, а водорода – 7,7%. Относительная плотность данного вещества по водороду равна 13.
Определите молекулярную формулу углеводорода, если массовая доля углерода равна 80%, а водорода – 20%. Относительная плотность данного вещества по водороду равна 15.
Определите молекулярную формулу органического соединения, если массовая доля в нем углерода равна 37,5%, кислорода – 50%. водорода – 12,5%. Относительная плотность данного соединения по водороду равна 16.
Выведите молекулярную формулу фторпроизводного предельного углеводорода с массовой долей фтора, равной 0,73, углерода – 0,23 и водорода – 0,04. Относительная молекулярная масса этого соединения равна 52.
Определите молекулярную формулу углеводорода, если массовая доля углерода в нем равна 82,8%, а плотность этого вещества составляет 2,59 г/л.
Какова молекулярная формулу вещества, в котором массовая доля углерода равна 0,52, кислорода – 0,35, водорода – 0,13? Относительная плотность вещества по водороду равна 23.
Органическое вещество, массовая доля углерода в котором равна 65,75%, водорода – 15,06%, азота – 19,18%, имеет относительную плотность паров этого вещества по воздуху 2,52. Выведите молекулярную формулу вещества.
Органическое вещество, в котором массовая доля углерода равна 53,3%, водорода – 15,6%, азота – 31,1%, имеет относительную плотность по воздуху 1,551. Выведите молекулярную формулу вещества.






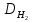
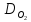
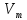
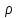
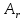
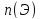
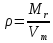 , где Vm = 22,4 л/моль
, где Vm = 22,4 л/моль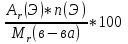 ; откуда
; откуда