
ТЕСТ
Ароматические углеводороды

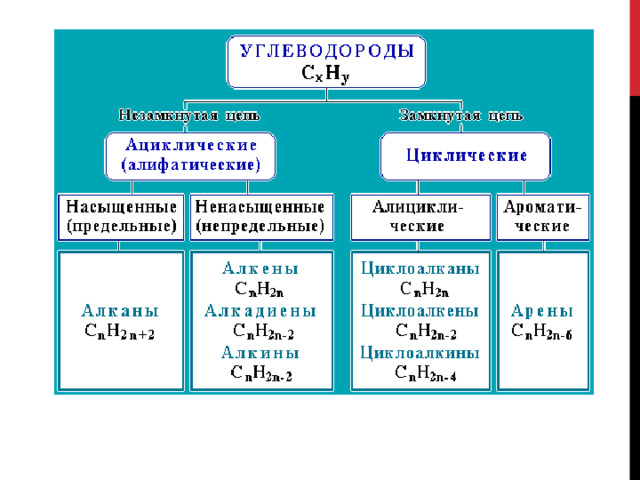
Аренами (ароматическими углеводородами) называют углеводороды, содержащие в молекуле циклогексатриеновый, бензольный цикл. Общая формула С n H 2n-6
План:
1. Актуализация знаний
2. Строение бензола. Ароматичность
3. Номенклатура и изомерия
4. Физические свойства
5. Способы получения
6. Химические свойства
7. Отдельные представители
8. Контрольные вопросы
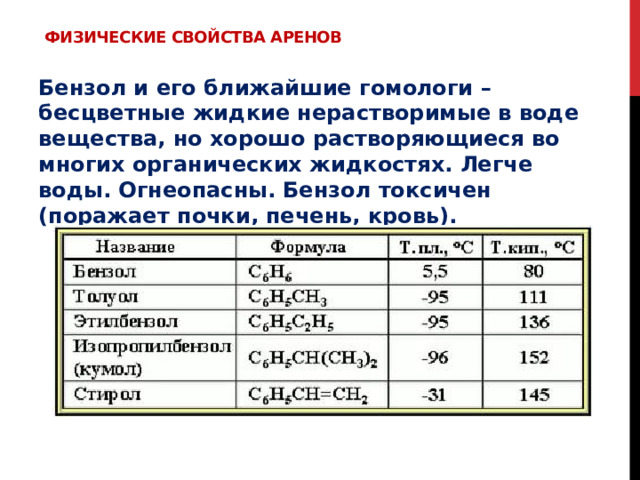
Физические свойства аренов
Бензол и его ближайшие гомологи – бесцветные жидкие нерастворимые в воде вещества, но хорошо растворяющиеся во многих органических жидкостях. Легче воды. Огнеопасны. Бензол токсичен (поражает почки, печень, кровь).

История открытия Аренов
Бензол был открыт еще в 1649 г.
немецким химиком, аптекарем
Иоганном Глаубером в результате перегонки каменноугольной смолы. Однако, тогда еще ничего не было известно о его составе.

История открытия Аренов
- Во второй раз бензол был "открыт" Майклом Фарадеем. Он выделил его из жидкого конденсата светильного газа в 1825 году, назвал «карбюрированным водородом» и тогда же был установлен его состав - С 6 Н 6.

История открытия Аренов
- В 1865 г. немецкий ученый Ф. А. Кекуле впервые высказал мысль о том, что атомы углерода в бензоле соединены не в виде открытой цепи, а замкнуты в цикл.
- Но эта формула не объясняет, почему бензол не обесцвечивает бромную воду и раствор перманганата калия.
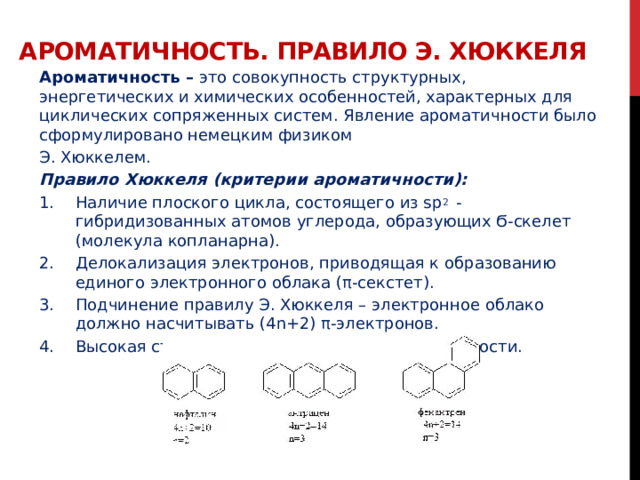
Ароматичность. Правило Э. Хюккеля
Ароматичность – это совокупность структурных, энергетических и химических особенностей, характерных для циклических сопряженных систем. Явление ароматичности было сформулировано немецким физиком
Э. Хюккелем.
Правило Хюккеля (критерии ароматичности):
- Наличие плоского цикла, состоящего из sp 2 - гибридизованных атомов углерода, образующих Ϭ-скелет (молекула копланарна).
- Делокализация электронов, приводящая к образованию единого электронного облака (π-секстет).
- Подчинение правилу Э. Хюккеля – электронное облако должно насчитывать (4n+2) π-электронов.
- Высокая степень термодинамической устойчивости.
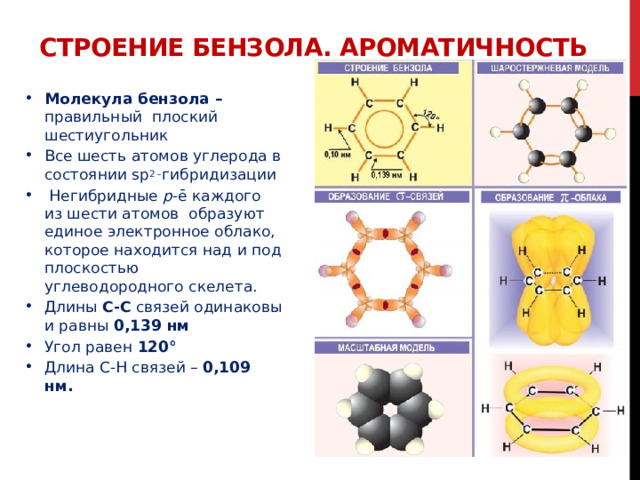
Строение бензола. Ароматичность
- Молекула бензола – правильный плоский шестиугольник
- Все шесть атомов углерода в состоянии sp 2 – гибридизации
- Негибридные р -ē каждого из шести атомов образуют единое электронное облако, которое находится над и под плоскостью углеводородного скелета.
- Длины С-С связей одинаковы и равны 0,139 нм
- Угол равен 120°
- Длина С-Н связей – 0,109 нм.
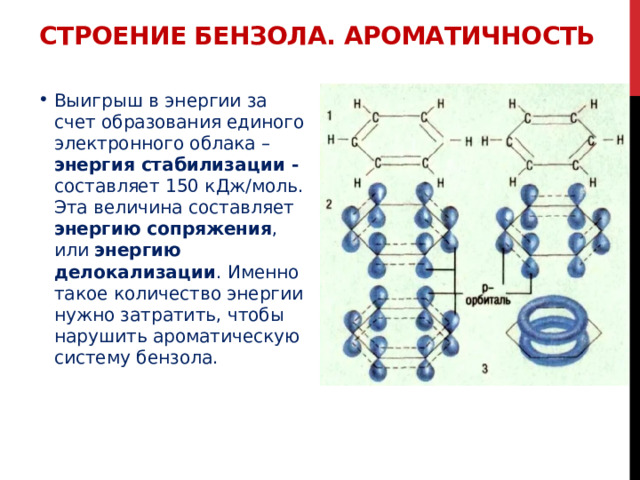
Строение бензола. Ароматичность
- Выигрыш в энергии за счет образования единого электронного облака – энергия стабилизации - составляет 150 кДж/моль. Эта величина составляет энергию сопряжения , или энергию делокализации . Именно такое количество энергии нужно затратить, чтобы нарушить ароматическую систему бензола.
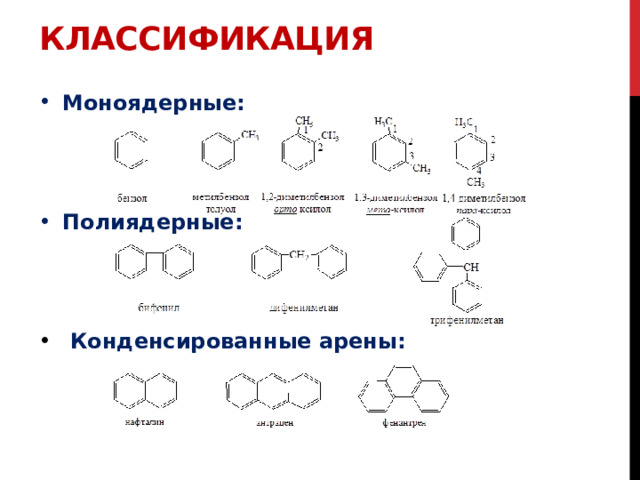
Классификация
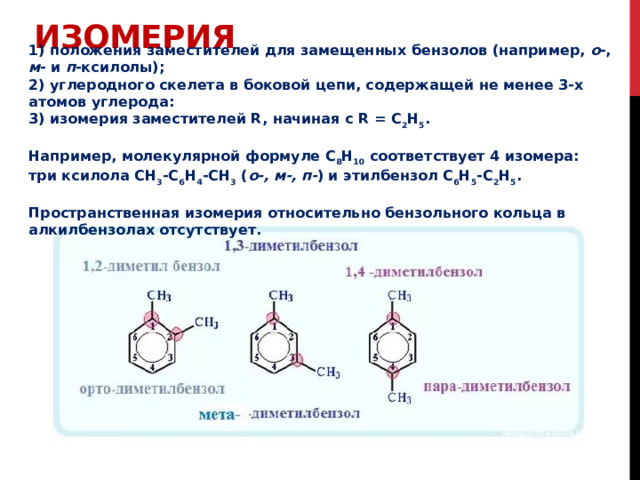
Изомерия
1) положения заместителей для замещенных бензолов (например, о -, м - и п -ксилолы); 2) углеродного скелета в боковой цепи, содержащей не менее 3-х атомов углерода:
3) изомерия заместителей R, начиная с R = С 2 Н 5 .
Например, молекулярной формуле С 8 Н 10 соответствует 4 изомера: три ксилола CH 3 -C 6 H 4 -CH 3 ( о-, м-, п- ) и этилбензол C 6 H 5 -C 2 H 5 .
Пространственная изомерия относительно бензольного кольца в алкилбензолах отсутствует.
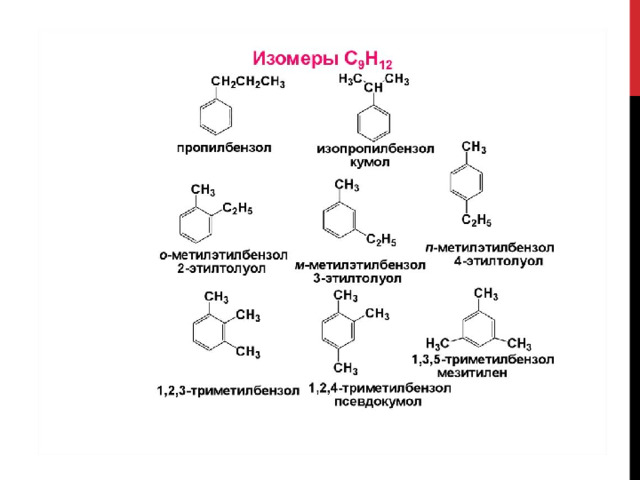

Изомерия
- Межклассовая изомерия, например:
НС≡С−СН 2 − СН2−С≡СН Гексадиин-1,5
- Валентные изомеры бензола, в которые бензол переходит УФ облучении:
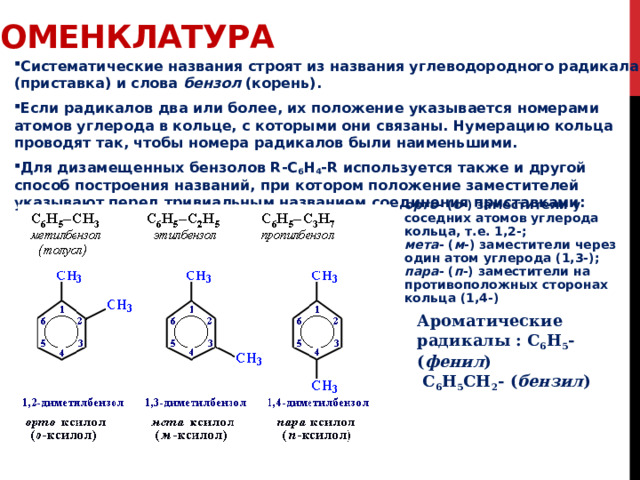
Номенклатура
- Систематические названия строят из названия углеводородного радикала (приставка) и слова бензол (корень).
- Если радикалов два или более, их положение указывается номерами атомов углерода в кольце, с которыми они связаны. Нумерацию кольца проводят так, чтобы номера радикалов были наименьшими.
- Для дизамещенных бензолов R-C 6 H 4 -R используется также и другой способ построения названий, при котором положение заместителей указывают перед тривиальным названием соединения приставками:
орто - ( о -) заместители у соседних атомов углерода кольца, т.е. 1,2-; мета - ( м -) заместители через один атом углерода (1,3-); пара - ( п -) заместители на противоположных сторонах кольца (1,4-)
Ароматические радикалы : C 6 H 5 - ( фенил )
C 6 H 5 CH 2 - ( бензил )
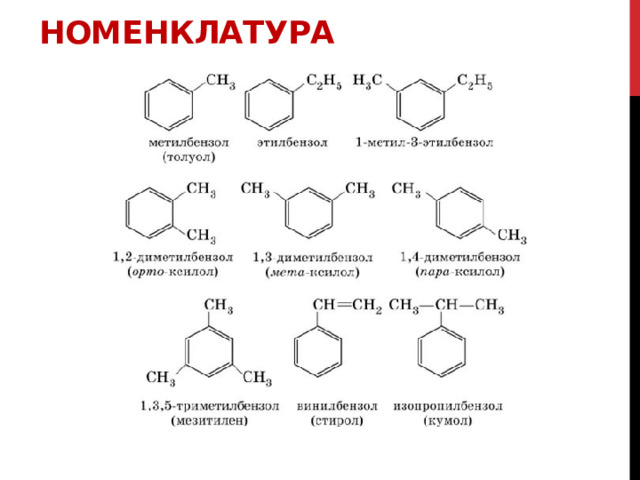
Номенклатура
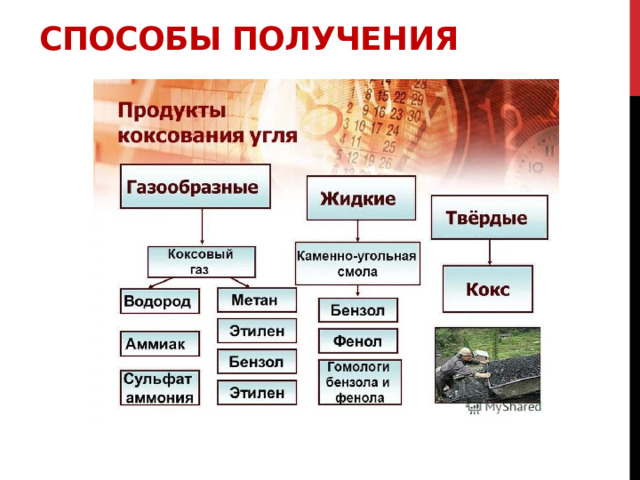
Способы получения

Способы получения
Приведите уравнения реакций:
1. дегидрирования циклогексана;
2. дегидроциклизации гексана и гептана;
3. тримеризации ацетилена и пропина-1;
4. декарбоксилирования натриевой соли бензоата натрия (натриевой соли бензойной кислоты.
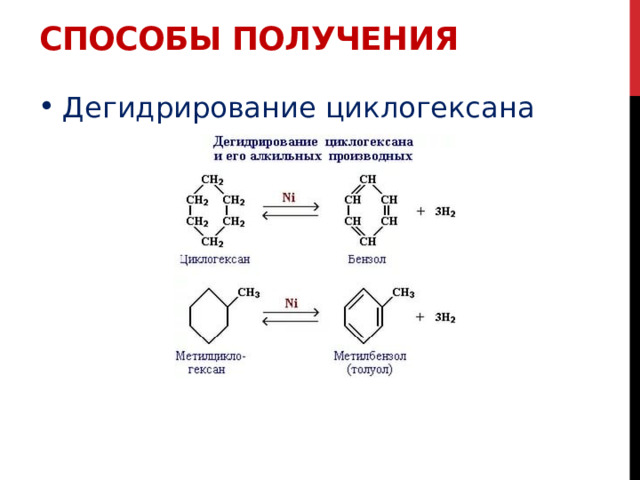
Способы получения
- Дегидрирование циклогексана
Способы получения
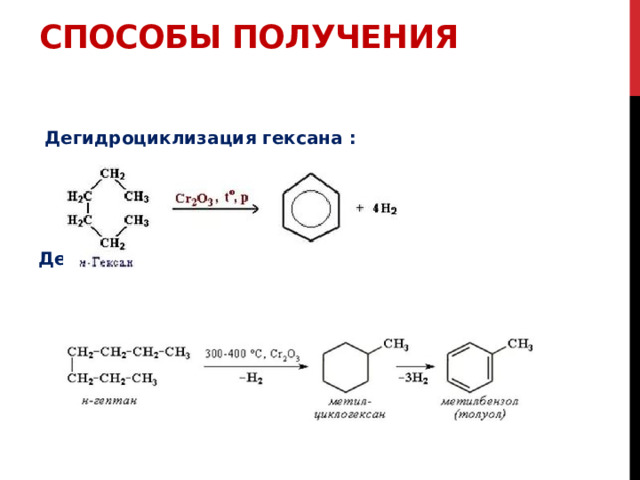
Дегидроциклизация гексана :
Дегидроциклизация гептана:
Способы получения
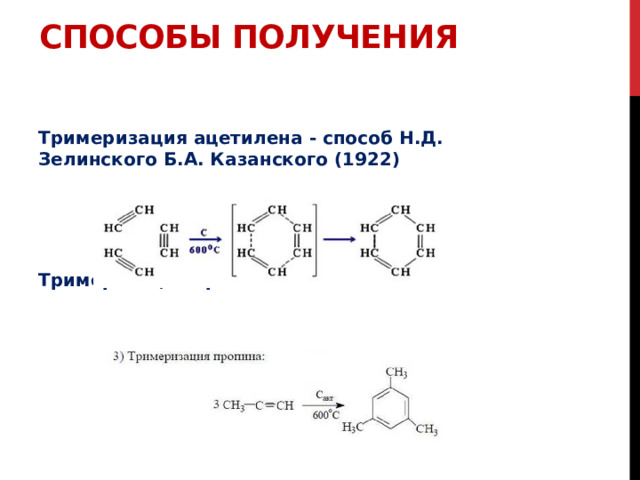
Тримеризация ацетилена - способ Н.Д. Зелинского Б.А. Казанского (1922)
Тримеризация пропина-1:
Способы получения
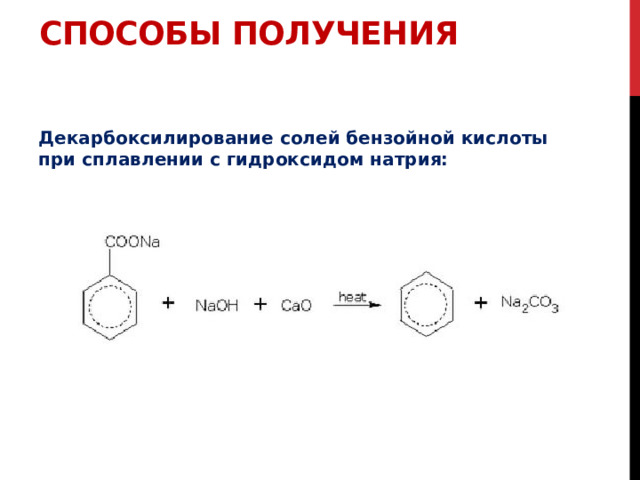
Декарбоксилирование солей бензойной кислоты при сплавлении с гидроксидом натрия:
Химические свойства аренов
По химическим свойствам арены отличаются от предельных и непредельных углеводородов. Это объясняется особенностями строения бензольного кольца. Делокализация шести пи-электронов в циклической системе понижает энергию молекулы, что обусловливает повышенную устойчивость (ароматичность) бензола и его гомологов.
Поэтому арены не склонны вступать в реакции присоединения или окисления, которые ведут к нарушению ароматичности.
Для них наиболее характерны реакции, идущие с сохранением ароматической системы, а именно , реакции замещения атомов водорода, связанных с циклом.
Наличие областей повышенной p-электронной плотности с двух сторон плоского ароматического цикла ведет к тому, что бензольное кольцо является нуклеофилом и в связи с этим склонно подвергаться атаке электрофильным реагентом. Таким образом, для ароматических соединений наиболее типичны реакции электрофильного замещения .
Механизм электрофильного замещения обозначается символом S Е (по первым буквам английских терминов: S – substitution [замещение], E – electrophil [электрофил]).
Другие реакции (присоединение, окисление) идут с трудом.
Химические свойства аренов
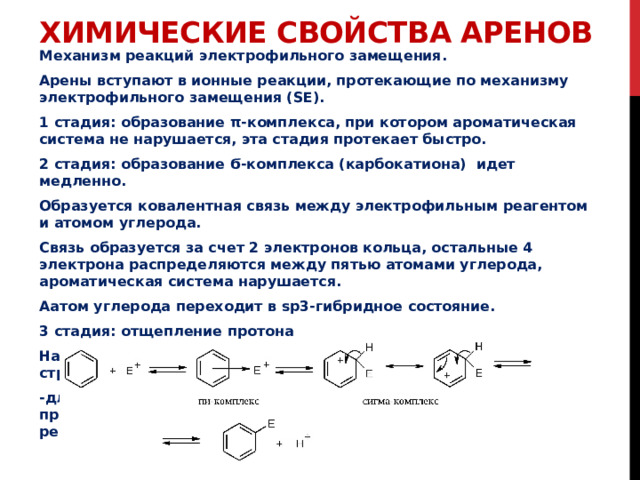
Механизм реакций электрофильного замещения.
Арены вступают в ионные реакции, протекающие по механизму электрофильного замещения (SE).
1 стадия: образование π-комплекса, при котором ароматическая система не нарушается, эта стадия протекает быстро.
2 стадия: образование Ϭ-комплекса (карбокатиона) идет медленно.
Образуется ковалентная связь между электрофильным реагентом и атомом углерода.
Связь образуется за счет 2 электронов кольца, остальные 4 электрона распределяются между пятью атомами углерода, ароматическая система нарушается.
Аатом углерода переходит в sp3-гибридное состояние.
3 стадия: отщепление протона
Нарушение ароматичности энергетически не выгодно, поэтому структура Ϭ-комплекса менее устойчива;
-для восстановления ароматичности происходит отщепление протона от атома углерода, связанного с электрофильным реагентом. 2 электрона возвращаются в π-систему.
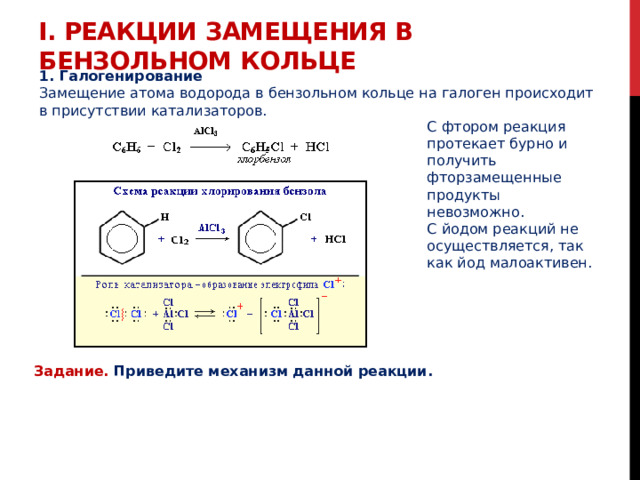
I. Реакции замещения в бензольном кольце
1. Галогенирование
Замещение атома водорода в бензольном кольце на галоген происходит в присутствии катализаторов.
С фтором реакция протекает бурно и получить фторзамещенные продукты невозможно.
С йодом реакций не осуществляется, так как йод малоактивен.
Задание. Приведите механизм данной реакции.
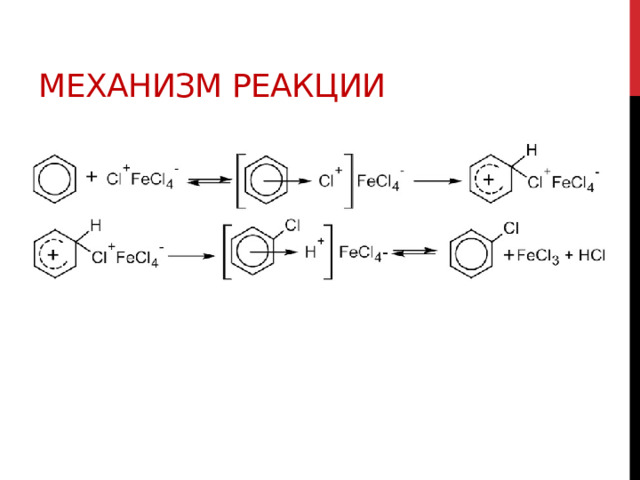
Механизм реакции
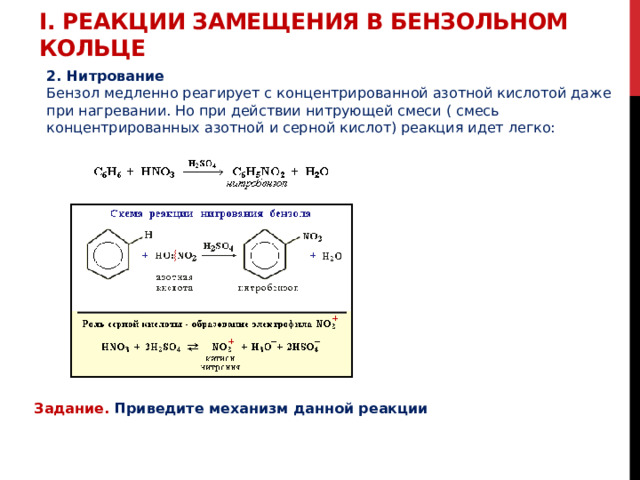
I. Реакции замещения в бензольном кольце
2. Нитрование
Бензол медленно реагирует с концентрированной азотной кислотой даже при нагревании. Но при действии нитрующей смеси ( смесь концентрированных азотной и серной кислот) реакция идет легко:
Задание. Приведите механизм данной реакции
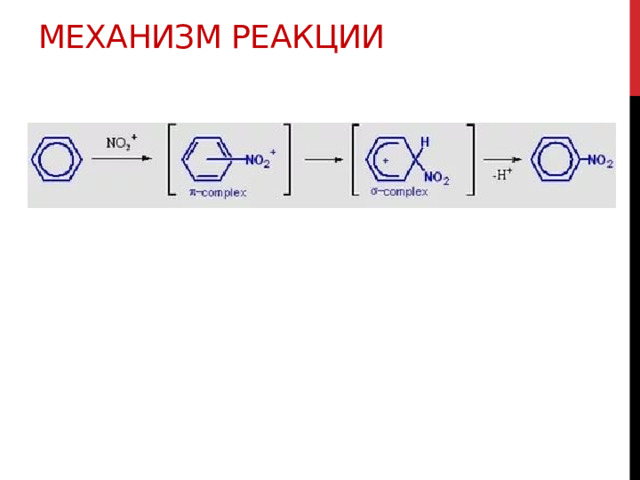
Механизм реакции
I. Реакции замещения в бензольном кольце
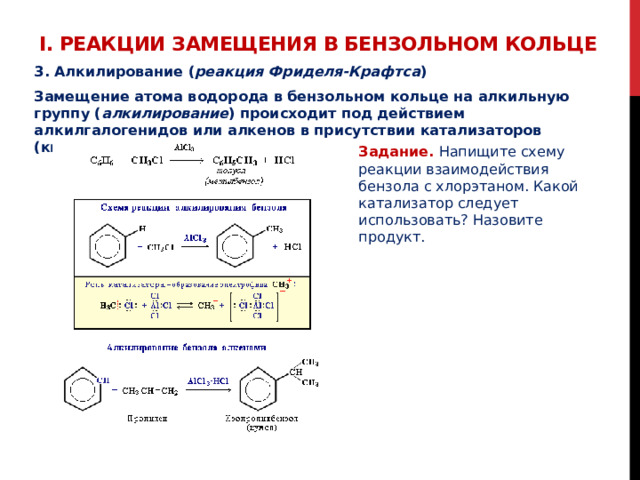
3. Алкилирование ( реакция Фриделя-Крафтса )
Замещение атома водорода в бензольном кольце на алкильную группу ( алкилирование ) происходит под действием алкилгалогенидов или алкенов в присутствии катализаторов (кислот Льюиса):
Задание. Напищите схему реакции взаимодействия бензола с хлорэтаном. Какой катализатор следует использовать? Назовите продукт.
Замещение в алкилбензолах
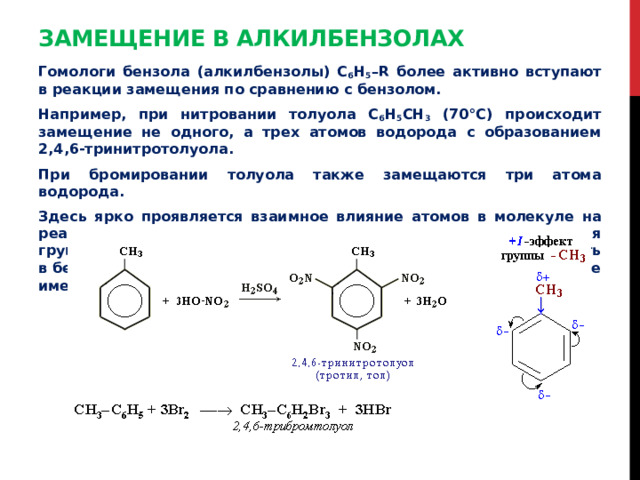
Гомологи бензола (алкилбензолы) С 6 Н 5 –R более активно вступают в реакции замещения по сравнению с бензолом.
Например, при нитровании толуола С 6 Н 5 CH 3 (70°С) происходит замещение не одного, а трех атомов водорода с образованием 2,4,6-тринитротолуола.
При бромировании толуола также замещаются три атома водорода.
Здесь ярко проявляется взаимное влияние атомов в молекуле на реакционную способность вещества. С одной стороны, метильная группа СH 3 (за счет + I -эффекта) повышает электронную плотность в бензольном кольце в положениях 2, 4 и 6 и облегчает замещение именно в этих положениях:
Химические свойства толуола
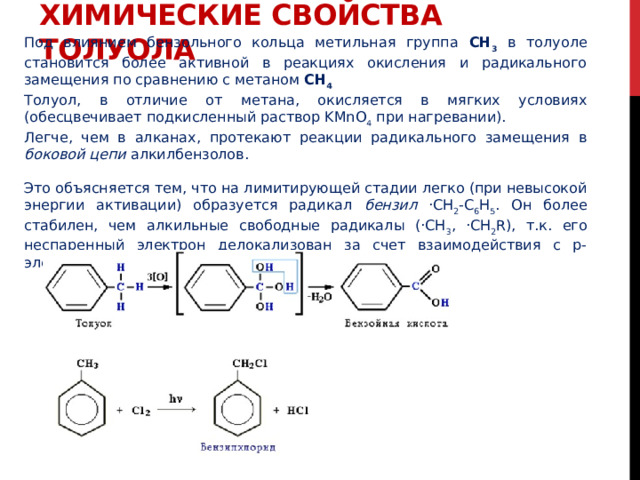
Под влиянием бензольного кольца метильная группа СH 3 в толуоле становится более активной в реакциях окисления и радикального замещения по сравнению с метаном СH 4
Толуол, в отличие от метана, окисляется в мягких условиях (обесцвечивает подкисленный раствор KMnO 4 при нагревании).
Легче, чем в алканах, протекают реакции радикального замещения в боковой цепи алкилбензолов.
Это объясняется тем, что на лимитирующей стадии легко (при невысокой энергии активации) образуется радикал бензил ·CH 2 -C 6 H 5 . Он более стабилен, чем алкильные свободные радикалы (·СН 3 , ·СH 2 R), т.к. его неспаренный электрон делокализован за счет взаимодействия с p-электронной системой бензольного кольца
II. Реакции присоединения к аренам
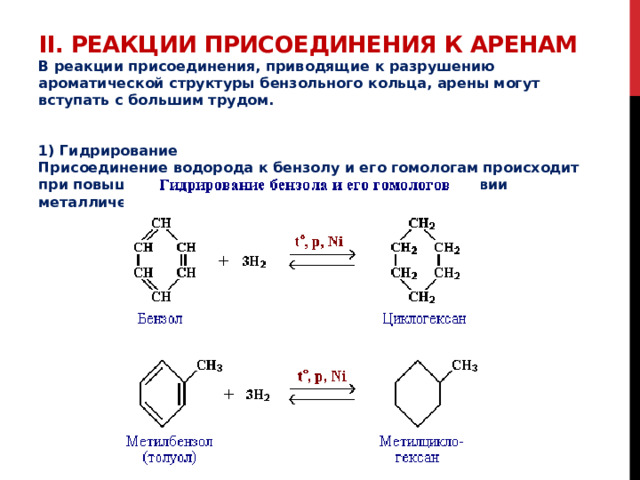
В реакции присоединения, приводящие к разрушению ароматической структуры бензольного кольца, арены могут вступать с большим трудом.
1) Гидрирование Присоединение водорода к бензолу и его гомологам происходит при повышенной температуре и давлении в присутствии металлических катализаторов.
II. Реакции присоединения к аренам
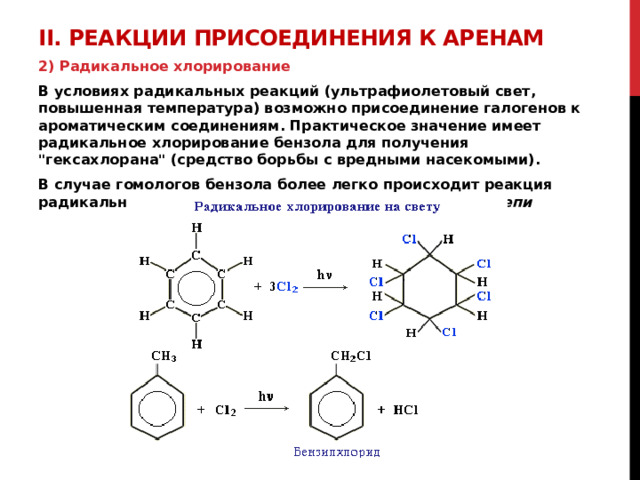
2) Радикальное хлорирование
В условиях радикальных реакций (ультрафиолетовый свет, повышенная температура) возможно присоединение галогенов к ароматическим соединениям. Практическое значение имеет радикальное хлорирование бензола для получения "гексахлорана" (средство борьбы с вредными насекомыми).
В случае гомологов бензола более легко происходит реакция радикального замещения атомов водорода в боковой цепи

III. Реакции окисления аренов
Бензол не окисляется даже под действием сильных окислителей (KMnO 4 , K 2 Cr 2 O 7 и т.п.). Поэтому он часто используется как инертный растворитель при проведении реакций окисления других органических соединений.
В отличие от бензола его гомологи окисляются довольно легко.
При действии раствора KMnO 4 и нагревании в гомологах бензола окислению подвергаются только боковые цепи
Бензол и его гомологи на воздухе горят коптящим пламенем, что обусловлено высоким содержанием углерода в их молекулах:
Бензол и его летучие гомологи образуют с воздухом и кислородом взрывоопасные смеси
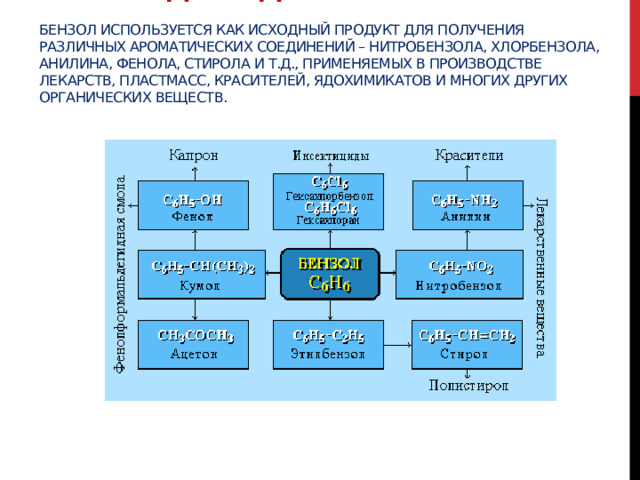
Применение ароматических углеводородов Бензол используется как исходный продукт для получения различных ароматических соединений – нитробензола, хлорбензола, анилина, фенола, стирола и т.д., применяемых в производстве лекарств, пластмасс, красителей, ядохимикатов и многих других органических веществ.
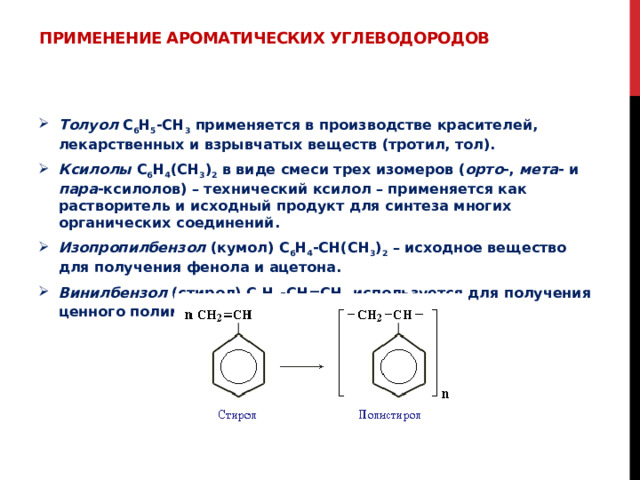
Применение ароматических углеводородов
- Толуол С 6 Н 5 -СН 3 применяется в производстве красителей, лекарственных и взрывчатых веществ (тротил, тол).
- Ксилолы С 6 Н 4 (СН 3 ) 2 в виде смеси трех изомеров ( орто -, мета - и пара -ксилолов) – технический ксилол – применяется как растворитель и исходный продукт для синтеза многих органических соединений.
- Изопропилбензол (кумол) С 6 Н 4 -СН(СН 3 ) 2 – исходное вещество для получения фенола и ацетона.
- Винилбензол (стирол) C 6 H 5 -CН=СН 2 используется для получения ценного полимерного материала полистирола
Правила ориентации
- Заместители, имеющиеся в бензольном ядре, направляют вновь вступающую группу в определенные положения, т.е. оказывают ориентирующее действие.
- По своему направляющему действию все заместители делятся на две группы: ориентанты первого рода и ориентанты второго рода . Ориентанты 1-го рода ( орто-пара -ориентанты) направляют последующее замещение преимущественно в орто - и пара -положения. К ним относятся электронодонорные группы (электронные эффекты групп указаны в скобках):
-R ( +I ); - OH ( +M,-I ); - OR ( +M,-I ); - NH 2 ( +M,-I ); - NR 2 ( +M,-I ) +M-эффект в этих группах сильнее, чем -I-эффект.
Ориентанты 1-го рода повышают электронную плотность в бензольном кольце, особенно на углеродных атомах в орто - и пара -положениях, что благоприятствует взаимодействию с электрофильными реагентами именно этих атомов.
Ориентанты 1-го рода, повышая электронную плотность в бензольном кольце, увеличивают его активность в реакциях электрофильного замещения по сравнению с незамещенным бензолом.
Особое место среди ориентантов 1-го рода занимают галогены, проявляющие электроноакцепторные свойства: - F ( +M ), - Cl ( +M ), - Br ( +M ). Являясь орто-пара -ориентантами, они замедляют электрофильное замещение. Причина - сильный –I -эффект электроотрицательных атомов галогенов, понижащий электронную плотность в кольце.
 бензол C 6 H 6 нитробензол C 6 H 5 NO 2 . " width="640"
бензол C 6 H 6 нитробензол C 6 H 5 NO 2 . " width="640"
Правила ориентации
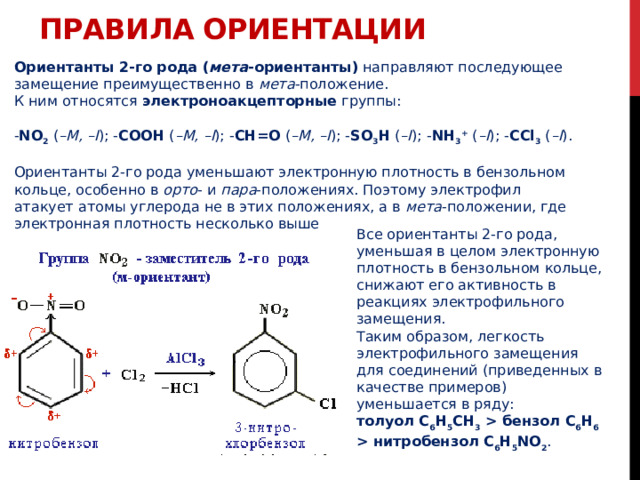
Ориентанты 2-го рода ( мета -ориентанты) направляют последующее замещение преимущественно в мета -положение. К ним относятся электроноакцепторные группы:
- NO 2 ( –M, –I ); - COOH ( –M, –I ); - CH=O ( –M, –I ); - SO 3 H ( –I ); - NH 3 + ( –I ); - CCl 3 ( –I ).
Ориентанты 2-го рода уменьшают электронную плотность в бензольном кольце, особенно в орто - и пара -положениях. Поэтому электрофил атакует атомы углерода не в этих положениях, а в мета -положении, где электронная плотность несколько выше
Все ориентанты 2-го рода, уменьшая в целом электронную плотность в бензольном кольце, снижают его активность в реакциях электрофильного замещения.
Таким образом, легкость электрофильного замещения для соединений (приведенных в качестве примеров) уменьшается в ряду:
толуол C 6 H 5 CH 3 бензол C 6 H 6 нитробензол C 6 H 5 NO 2 .

Отдельные представители
Бензол – бесцветная жидкость с характерным запахом, не растворяется в воде. Получают их каменноугольной смолы. Является сырьем для получения стирола, анилина. Применяется для синтеза красителей, ПАВ, фармацевтических препаратов.
Бензол сильный яд. При концентрации от 10 до 25 мг/л наступает острое отравление (голово- кружение, судороги, бессознательное состояние). При хроническом отравлении поражаются почки, печень, костный мозг.

Отдельные представители
Толуол – бесцветная жидкость, не растворяется в воде, проявляет слабое наркотическое действие. Служит растворителем, в качестве добавок к моторному топливу. Является сырьём для получения нитротолуолов, бензойной кислоты, сахарина.

Отдельные представители
Кумол (изопропил бензол) используется для получения фенола и ацетона.
N-Цимол (1-метил-4изопропилбензол) содержится в растениях и может быть выделен из эфирных масел (эвкалиптового и тминового). Его строение родственно терпенам.
Цимол представляет собой бесцветную подвижную жидкость с ароматическим запахом (чистый n-Цимол имеет слабый цитрусовый запах). Нерастворим в воде, растворим в этаноле и других органических растворителях.
Ограниченно применяется при составлении парфюмерных композиций и пищевых эссенций.

Отдельные представители
Нафталин – бесцветные пластинки (t пл. 80 градусов), легко возгоняется, не растворяется в воде, растворяется в органических растворителях. Легче бензола, вступает в реакции электрофильного замещения, широко используется в химии красителей.

Отдельные представители
Антрацен и фенантрен (t пл. 217 и 100), выделяют из каменноугольной смолы. Кристаллические вещества. Антрацен используется при производстве красителей
Фенантрен – основа стероидов, выполняющих роль гормонов в организме.
Многие применяются как лекарственные препараты: гидрокортизон, эстрадиол.
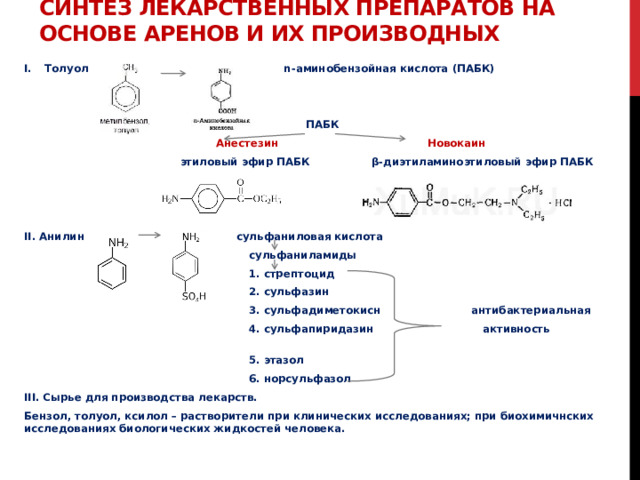
Синтез лекарственных препаратов на основе аренов и их производных
- Толуол n-аминобензойная кислота (ПАБК)
ПАБК
Анестезин Новокаин
этиловый эфир ПАБК β-диэтиламиноэтиловый эфир ПАБК
II. Анилин сульфаниловая кислота
сульфаниламиды
1. стрептоцид
2. сульфазин
3. сульфадиметокисн антибактериальная
4. сульфапиридазин активность
5. этазол
6. норсульфазол
III. Сырье для производства лекарств.
Бензол, толуол, ксилол – растворители при клинических исследованиях; при биохимичнских исследованиях биологических жидкостей человека.








































 бензол C 6 H 6 нитробензол C 6 H 5 NO 2 . " width="640"
бензол C 6 H 6 нитробензол C 6 H 5 NO 2 . " width="640"

























