
9 класс (обязательный минимум по химии) Азотная кислота. Получение, свойства. Нитраты, азотные удобрения.

Цели урока:
- Знать строение и свойства азотной кислоты и ее солей.
- Уметь составлять уравнения реакций, отражающие свойства этих веществ.
- Развивать наблюдательность, внимание, умение работать самостоятельно и в группе, умение анализировать.
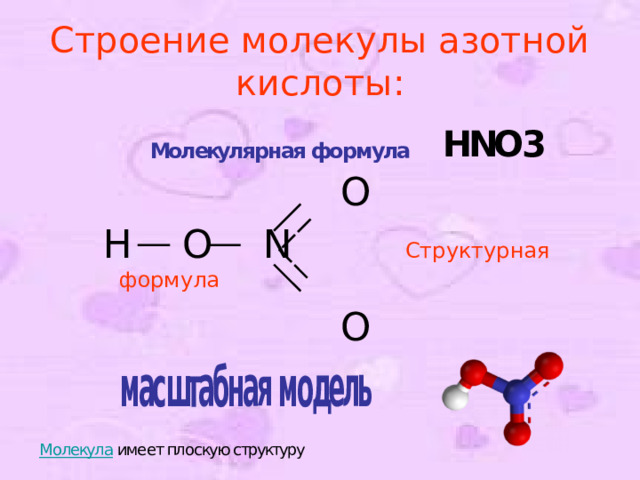
Строение молекулы азотной кислоты:
O
H O N Структурная формула
O
- O H O N Структурная формула O
- O H O N Структурная формула O

Физические свойства
Бесцветная, дымящаяся, неограниченно растворимая в воде жидкость, обладающая резким раздражающим запахом. t °пл.= -41° C ; t °кип.= 86°С. При долгом стоянии на свету желтеет из-за частичного разложения. Едкое вещество.

Получение.
Действие конц. серной кислоты на кристаллические нитраты.
KNO 3 + H 2 SO 4(конц) = KHSO 4 + HNO 3

Получение.
- Промышленный способ осуществляется в 3 этапа:
1) Окисление аммиака на платиновом катализаторе до NO
4NH 3 + 5O 2 = 4NO + 6H 2 O
2) Окисление кислородом воздуха NO до NO 2
2 NO + O 2 = 2 NO 2
3) Поглощение NO 2 водой в присутствии избытка кислорода
4NO 2 + О 2 + 2H 2 O = 4HNO 3

ХИМИЧЕСКИЕ СВОЙСТВА
- Общие с другими кислотами
- Специфические свойства
- - Общие с другими кислотами - Специфические свойства
- - Общие с другими кислотами - Специфические свойства
- - Общие с другими кислотами - Специфические свойства
- - Общие с другими кислотами - Специфические свойства

Общие химические свойства
HNO 3 :
- Очень сильная кислота.
- Диссоциирует в водном растворе практически нацело.
HNO 3 H + +NO 3 -

Разбавленная азотная кислота проявляет все свойства кислот :
- 1. взаимодействует с основными и амфотерными оксидами.
- 2. взаимодействует с основаниями.
- 3. реагирует с солями ( , )

HNO 3 :
- Реагирует с основными и амфотерными оксидами
CuO + 2 HNO 3 = Cu ( NO 3 ) 2 + H 2 O
CuO + 2H + + 2NO 3 - = Cu 2+ + 2NO 3 - + H 2 O
CuO + 2H + = Cu 2+ + H 2 O
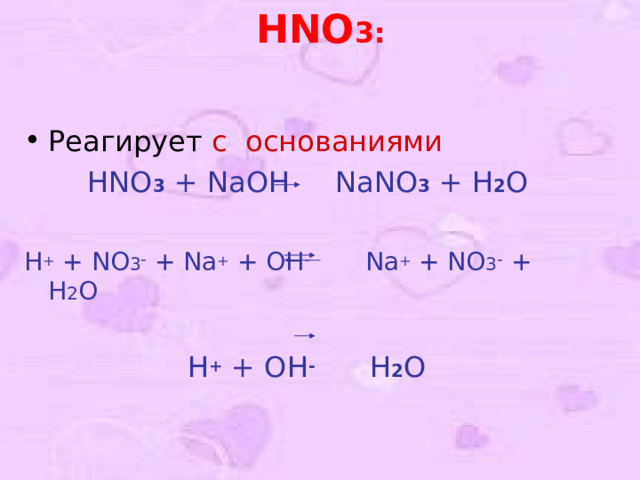
HNO 3 :
HNO 3 + NaOH NaNO 3 + H 2 O
H + + NO 3 - + Na + + OH - Na + + NO 3 - + H 2 O
H + + OH - H 2 O

HNO 3 :
- вытесняет слабые кислоты из их солей
- 2HNO 3 + Na 2 CO 3 2NaNO 3 + H 2 O + CO 2
2H + + 2NO 3 - + 2Na + + С O 3 2 - 2Na + + 2NO 3 - + H 2 O + CO 2
- 2H + + СO 3 2 - H 2 O + CO 2

Азотная кислота проявляет особые свойства:
- Взаимодействие с металлами
- Взаимодействие с неметаллами
- Взаимодействие с органическими соединениями
- Разложение при нагревании

Специфические свойства азотной кислоты
При взаимодействии с металлами никогда не выделяется водород !!
- При взаимодействии с металлами никогда не выделяется водород !!
- При взаимодействии с металлами никогда не выделяется водород !!
- При взаимодействии с металлами никогда не выделяется водород !!
металл + HNO 3 = соль азотной кислоты + вода + газ ( соединение азота, азот)
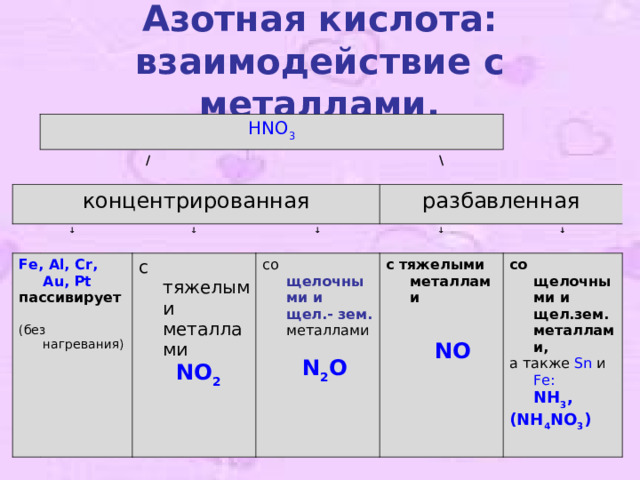
Азотная кислота: взаимодействие с металлами.
HNO 3
/
концентрированная
Fe, Al, Cr, Au, Pt
\
пассивирует
(без нагревания)
разбавленная
с тяжелыми металлами NO 2
со щелочными и щел.- зем. металлами
N 2 O
с тяжелыми металлами
NO
со щелочными и щел.зем. металлами,
а также Sn и Fe: NH 3 ,
(NH 4 NO 3 )

Реакция с металлами :
- Большинство металлов реагируют с азотной кислотой с выделением азота или его оксидов в различных степенях окисления, или с выделением аммиака. Продукты реакции зависят от условий ее проведения.
- Cu 0 + 4HN +5 O 3 → Cu +2 (NO3) 2 + 2N +4 O 2 + 2H 2 O
- 3Cu 0 + 8HN +5 O 3 → 3Cu +2 (NO 3 ) 2 + 2N +2 O + 4H 2 O
Fe, Al, Cr, Au, Pt с концентрированной кислотой не реагируют,
пассивируются (без нагревания) .

S + 6HNO 3 ( конц. ) = H 2 SO 4 + 6NO 2 + 2H 2 O
B + 3HNO 3 = H 3 BO 3 + 3NO 2
3P + 5HNO 3 + 2H 2 O = 5NO + 3H 3 PO 4
HNO 3 реагирует с неметаллами:
- Азотная кислота превращается в NO (или в NO 2 ); неметаллы окисляются до соответствующих кислот:

Азотная кислота
- 1. Разлагается на свету и при нагревании:
4HNO 3 = 2H 2 O + 4NO 2 + O 2

Реакции с органическими веществами:
Окрашивает белки в желтый цвет
("ксантопротеиновая реакция")

Качественная реакция на ион NO 3 -
Вещество + медные стружки + H 2 SO 4 (к.)+ t 0
NaNO 3 + H 2 SO 4 ( к . ) = NaHSO 4 + HNO 3
4 HNO 3 + Cu = Cu(NO 3 ) 2 + 2 NO 2 + 2H 2 O
бурый газ

Соли азотной кислоты
- называются нитратами (селитрами)
- NaNO 3 – нитрат натрия
- Cu(NO 3 ) 2 – нитрат меди( II)

РАЗЛОЖЕНИЕ НИТРАТОВ при нагревании:
1) Нитраты щелочных металлов разлагаются до нитритов :
2 NaNO 3 = 2 NaNO 2 + O 2
2) Нитраты менее активных металлов (от щелочноземельных до меди) разлагаются до оксидов:
2Mg(NO 3 ) 2 = 2MgO + 4NO 2 + O 2
2Cu(NO 3 ) 2 = 2CuO + 4NO 2 + O 2
3) Нитраты малоактивных металлов разлагаются до металлов :
2 AgNO 3 = 2 Ag + 2 NO 2 + O 2
4) Нитрат аммония разлагаются до N 2 O
NH 4 NO 3 = N 2 O + 2H 2 O
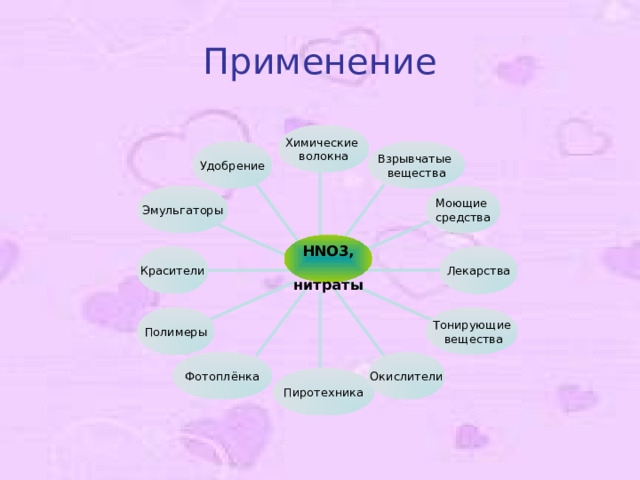
Применение
Химические
волокна
Взрывчатые
вещества
Удобрение
Эмульгаторы
Моющие
средства
HNO3 ,
нитраты
Красители
Лекарства
Полимеры
Тонирующие
вещества
Фотоплёнка
Окислители
Пиротехника







































