
5Н, 2Н 2 , 6Н, 3Н 2

Первый я на белом свете: Во Вселенной, на планете, Я из космоса пришёл, И в воде приют нашёл. Газ легчайший и бесцветный, Неядовитый и безвредный. Соединяясь с кислородом, Я для питья даю вам воду.

Тема урока:
«Водород, его общая характеристика и нахождение в природе. Получение водорода»

План
1.1 Водород – химический элемент
1.2 Водород – простое вещество
2. Открытие водорода
3.Распростроненность водорода в природе
4. Способы получения водорода

1.1 Водород- химический элемент
Химический знак –
Порядковый номер –
Относительная атомная масса
Ar (H)=
Химическая формула –
Относительная молекулярная
масса Mr (H 2 )=
Валентность –
Латинское название Hydrogenium (рождающий воду)

1.2 Водород – простое вещество



Лавуазье дал водороду название hydrogène (от др.-греч . «гидор» - вода и «гайноме» - "рождаю") — «рождающий воду».
Русское наименование «водород» предложил химик М. Ф. Соловьев в 1824 году — по аналогии с « кислородом » М. В. Ломоносова .
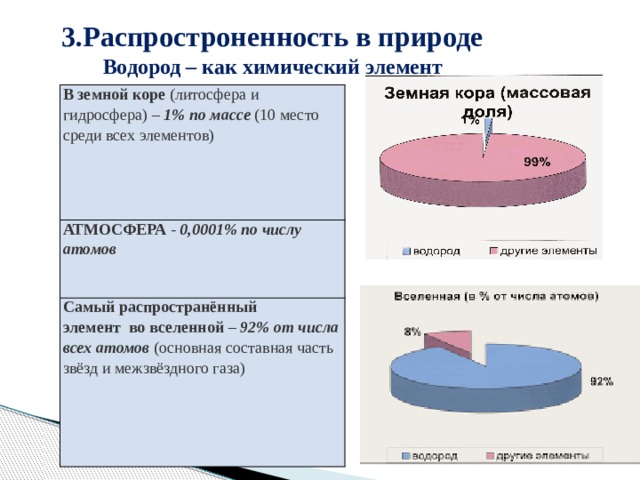
3.Распростроненность в природе
Водород – как химический элемент
В земной коре (литосфера и гидросфера) – 1% по массе (10 место среди всех элементов)
АТМОСФЕРА - 0,0001% по числу атомов
Самый распространённый элемент во вселенной – 92% от числа всех атомов (основная составная часть звёзд и межзвёздного газа)

Водород – как химический элемент
В соединениях
Н 2 О – вода (11% по массе)
СН 4 – газ метан (25% по массе)
Органические вещества (нефть, горючие природные газы и других)
В организмах животных и растений (то есть в составе белков, нуклеиновых кислот, жиров, углеводов и других)
В теле человека в среднем содержится около 7 килограммов водорода.
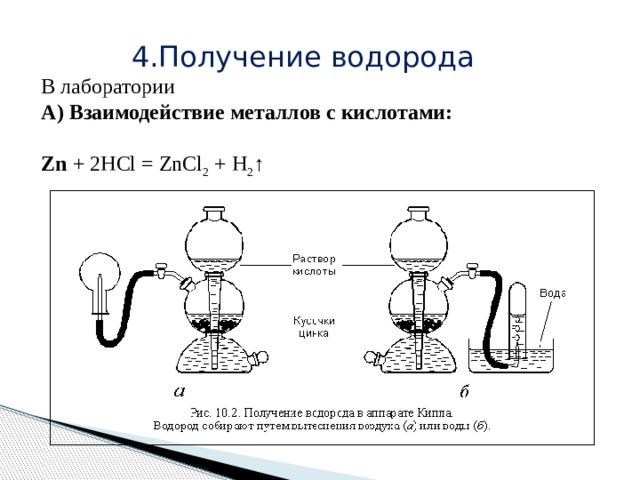
4.Получение водорода
В лаборатории
А) Взаимодействие металлов с кислотами:
Zn + 2HCl = ZnCl 2 + H 2 ↑



Схема составления уравнений реакции взаимодействия металла с кислотами.


Б)Взаимодействие активных металлов с водой
2Na + 2H 2 O = 2NaOH + H 2


Получение водорода в промышленности
Разложение воды под действием электрического тока
H 2 O H 2 + O 2
Получение из природного газа – метана
CH 4 C + H 2

Краткие выводы урока:
1.Водород — наиболее распространенный элемент во Вселенной.
2. Простое вещество водород Н 2 — самый легкий газ, у которого нет запаха, цвета, вкуса.
3.Водород мало растворяется в воде, его можно собирать методом вытеснения воды и воздуха.

Закрепление
Задание №1. Запишите 7 атомов водорода, семь молекул водорода, 7 катионов водорода, 7 анионов водорода, 7 молекул соляной кислоты.
Задание 2. Закончите уравнения химических реакций, используя алгоритм:
Подсказка! Zn - двухвалентен; K - одновалентен; Al - трёхвалентен.
В-1 В-2
Zn + H 2 SO 4 = Zn + HCl =
Zn + H 3 PO 4 = K + H 2 SO 4 =
K + HCl = K + H 3 PO 4 =
Al + H 2 SO 4 = Al + HCl =

Ответьте на вопросы:
- Почему водород не встречается в природе в свободном виде?
- Какими способами модно получить водород?
- Почему в лаборатории , где получают водород помещение проветривают?
- Как проверяют водород на чистоту и для чего это делают?

Домашнее задание
П. 28. с.96, вопросы 1-4, тесты.








































