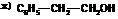Государственное бюджетное образовательное учреждение
среднего профессионального образования
Калининградской области
«Промышленно-строительный техникум»
| «Утверждаю» «___» _________ 20___г. Заместитель директора по УМР Л.Г.Алсынбаева _______ |
| Рассмотрено и согласовано на заседании ПЦК общеобразовательных дисциплин Протокол № _________ «___» ___________ 20__г. Председатель ПЦК М.Ю.Гайдай _________ |
Экзаменационные материалы
Дисциплина: химия
Специальность: садово-парковое и ландшафтное строительство
Разработано преподавателем биологии и химии Сафоновой Д.Н.
Калининград 2014
Экзамен по дисциплине химия состоит из двух частей теоретической и практической. Теоретическая часть выполняется в системе дистанционного обучения в электронном курсе химия. Банк вопросов включает сто заданий с выбором ответа. Компьютер автоматически формирует каждый раз новый вариант из 30 вопросов, каждый вопрос оценивается в 0,5 балла. Практическая часть состоит из 40 заданий, проверяющих знание законов химии и умение писать и уравнивать реакции, а так же различать классы неорганических и органических соединений и называть соединения по международной номенклатуре ИЮПАК. Каждому студенту предлагается выполнить 2 задания, каждое оценивается в 7,5 баллов. В итоге за весь экзамен студент может набрать 30 баллов.
Список вопросов из электронного банка:
Составьте формулы соединений с кислородом (II) для бария (Ba)
BaO
BaO2
Ba2O
На внешнем уровне атома химического элемента в основном состоянии находится 5 электронов. Какой это может быть элемент:
натрий
бор
азот
Общая формула высшего оксида элементов II A группы периодической системы Д.И.Менделеева:
R2O
RO
R2O3
Составьте формулы соединений с водородом (I) для хлора (Сl)
HCl
H2Cl
HCl2
К физическим свойствам металлов относится
легкоплавкость
теплопроводность
хрупкость
Химические элементы металлы обладают
окислительными свойствами
восстановительными свойствами
разрушительными свойствами
На внешнем энергетическом уровне у металлов в основном
1-3 электронна
4-5 электроннов
6-8 электроннов
при взаимодействии металлов с кислородом получаются
соли
кислоты
основные или амфотерные оксиды
Выберите способ защиты металлов от коррозии.
покрытие краской
обертывание бумагой
поливание соленым раствором
Продолжите уравнение реакции Al + Cl =
AlCl
AlCl2
AlCl3
Аллотропия - это
свойство неметаллов образовывать несколько простых веществ
свойство неметаллов переходить из твердого состояния в газообразное
свойство неметаллов вступать в реакции с хлором
Формула летучего водородного соединения для неметаллов 6 группы
RH4
RH3
H2R
Для простых веществ неметаллов характерен вид связи
ионная
металлическая
ковалентная
При взаимодействии основных оксидов с водой получается
соль
кислота
основание
К растворимым основаниям относится
NaOH
Al(OH)3
Fe(OH)2
Реакция взаимодействия основания и кислоты называется
дегенерацией
активацией
нейтрализацией
К бескислородным кислотам относится
HCl
H2CO3
HNO3
Назовите следующее соединение CaCl2
кальцид хлора
хлорокальций
хлорид кальция
класс химических соединений в состав которых входит протон водорода и анион кислотного остатка называется
оксиды
основания
кислоты
продолжите химическую реакцию Ca + H2O
Ca + H2
Ca (OH)2
HCa O
Продолжите уравнение реакции H2SO4 + MgCl2
MgSO4 +2HCl
MgH + ClS
H2S + Mg ClO
к двухосновным кислотам относится
HCl
HNO3
H2SO4
К физическим свойствам металлов относится
летучесть
ковкость
стойкость
Для простых веществ металлов характерна ...... решетка
ионная
атомная
металлическая
К щелочным металлам относится
бром
натрий
золото
Число электронов характерное для неметаллов
1
2-3
4-8
Для химических элементов неметаллов характерны
окислительные свойства
восстановительные свойства
разрушительные свойства
Электроотрицательность это
способность атома химического элемента притягивать общие электроны
способность неметаллов вступать в реакции с металлами
способность неметаллов блестеть
К аллотропным модификациям относится
кислород и озон
натрий и хлор
магний и сера
При взаимодействии кислотного оксида и воды образуется
соль
основание
кислота
Кислород в оксидах проявляет степень окисления
0
-1
-2
Растворимые основания по другому называют
гидроксиводороды
щелочи
мыла
К кислородсодержащим кислотам относится
HCl
HBr
HClO4
К трехосновным кислотам относится
HCl
H2S
H3PO4
Назовите следующее соединение NaBr
натрид брома
бромид натрия
бромонатрий
у кислоты плотность больше чем у воды, поэтому нужно
наливать кислоту в воду
наливать воду в кислоту
лучше вообще не смешивать
при взаимодействии Na +HCl выделится
натрий
водород
хлор
Класс соединений состоящий из катиона металла и гидроксид-аниона называется
соли
оксиды
гидроксиды
Продолжите реакцию NaOH + AlF3
Na Al +FOH
Na F +Al(OH)3
NaO +HFAl
Продолжите реакцию Al + S =
SAl
AlS
Al2S3
ядро атома это
совокупность электронов
совокупность радикалов
совокупность протонов и нейтронов
Простым и сложным веществом являются соответственно
фтор и вода
фтор и бром
фтор и натрий
Что такое моль
состав атомов вещества
масса вещества
мера количества вещества
Рассчитайте молярную массу воды ( H2O)
2 г/моль
18 г/моль
22 г/моль
определите вид химической связи в соединении NaCl
ковалентная
металлическая
ионная
Исключите лишнее понятие:
протон
электрон
ион
Химический элемент расположен во 2-м периоде, 1 а группе Назовите этот элемент
литий
радий
железо
К газообразным дисперсным системам относится атмосферный туман. Туман представляет из себя распределение мельчайших частиц:
газа в твердом веществе
жидкости в газе
жидкости в жидкости
Вещества с атомной кристаллической решеткой (алмаз)
очень твердые и тугоплавкие
проводят электрический ток
хрупкие и легкоплавкие
валентность это
способность атома присоединять определенное число других атомов
формальный заряд атома в молекуле, рассчитанный из предположения, что все связи в соединении ионные
количество протонов в ядре
Для веществ с металлической кристаллической решеткой характерным свойством является
хрупкость
электропроводность
летучесть
К химическим явлениям относятся
ржавление железа
таянье льда
измельчение соли
Четыре электрона на внешнем энергетическом уровне содержит атом
натрия
кремния
хлора
В молекуле СО2 имеется
ионная связь
металлическая связь
ковалентная связь
число протонов в атоме равно
количеству ионов
количеству электронов
количеству изотопов
период это
горизонтальный ряд
диагональный ряд
зигзаг
Валентность IV сера проявляет в соединении, формула которого:
Na2S
H2S
SO2
Ковалентная неполярная связь образуется
в неметаллах
в металлах
в ионах
Смесью веществ в отличии от чистого вещества является
воздух
алюминий
водород
в образовании химической связи принимают участие
все электроны атома
нейтроны
электроны внешних энергетических уровней
Молекулярная решетка воды
ионная
металлическая
молекулярная
Что такое молярная масса
это состав вещества
это масса одного моля вещества
это объем вещества
Рассчитайте молярную массу HCl
36,5 г/моль
12 г/моль
48 г/моль
Определите вид химической связи в соединении Li
ионная
ковалентная
металлическая
Сложным веществом называется
вещество состоящее из одного вида атомов
вещество состоящее из ионов
вещество состоящие из нескольких видов атомов
Правильным является утверждение
все атомы состоят из веществ
все молекулы состоят из атомов
все вещества состоят из ионов
При горении угля атомы углерода
распадаются
остаются неизменными
улетучиваются
Молекула вещества, формула которого HClO2, содержит
три атома двух элементов
четыре атома трёх элементов
три атома трёх элементов
Эмульсиями называются дисперсные системы, в которых
смешиваются две несмешиваемые жидкости
газ растворяют в жидкости
твердое вещество распыляют в газе
электроотрицательность влияет на
образование ковалентных связей
образование металлической связи
ни на что не влияет
Кристаллическая решетка графита состоит из атомов
азота
натрия
углерода
порядковый номер элемента соответствует
числу протонов в ядре атома
числу изотопов
числу ионов
число электронов в атоме
равно количеству нейтронов
каждый раз разное
равно количеству положительных протонов в ядре
Вещество это
то из чего состоят физические тела
то из чего состоят полимеры
то из чего состоят изомеры
Атом брома имеет следующую конфигурацию валентного слоя
2s22р5
5s25р2
4s24р5
Как фамилия ученого создавшего учение о строении органических веществ
Морковкин
Лувуазье
Бутлеров
К органическим кислотам относится
серная
щавелевая
азотная
каменный уголь образуется из
гранита
окаменелых деревьев
раковин моллюсков
Из чего состоят полимеры
из мономеров
из водомеров
из энантиомеров
А.М. Бутлеров создал учение
о строении органических веществ
о путешествии живого духа
о тории горения нефти
Синтетическими полимерами называются
вещества, созданные природой
вещества, синтезированные человекам и несуществующие в природе
природные вещества, созданные человеком
структурными изомерами называются
вещества, имеющие разный состав
вещества, имеющие одинаковый состав и разное строение
вещества, имеющие разное строение
как называются углеводороды, имеющие двойную связь между атомами углерода
спирты
алкены
кислоты
как называется самая легкая фракция получаемая при переработки нефти
мазут
гудрон
керосин
при сжигании натуральных волокон
образуется запах жженого пера
образуется запах горелого пластика
не образуется никакого запаха
Нефть когда-то образовалась из
гранита
при падении метеорита
из органических остатков животных и растений
Как называются ученые считавшие, что органические вещества можно получать только из животных и растений
виталисты
идеалисты
коммунисты
какой химический элемент входит в состав всех органических соединений
азот
натрий
углерод
как называется данное соединение CH4
метан
этан
нонан
Назовите фамилию советского ученого впервые синтезировавшего искусственный каучук
Бэр
Морковкин
Лебедев
Из чего состоят белки
сахара
аминокислоты
глицерин
К кислородсодержащим органическим соединениям относят
метан
пропан
этиловый спирт
как называются вещества, имеющие одинаковый состав, но разное строение
изомеры
электролиты
модификации
какую валентность имеет углерод в органических веществах
2
3
4
как называются углеводороды, имеющие все одинарные связи
спирты
алканы
кислоты
Из какого натурального вещества долгое время изготавливали резину
гудрон
каучук
смола
Как называется самая тяжелая фракция переработки нефти
бензин
керосин
мазут
при горении синтетических волокон
образуется запах горелого пера
образуется запах горелого пластика
нет никакого запаха
Назовите предельный углеводород имеющий пять атомов углерода
метан
этан
пентан
В молекуле I2 имеется
ионная связь
ковалентная неполярная связь
радикальная связь
Список практических заданий:
1.Пользуясь значениями атомных весов элементов из Периодической таблицы, рассчитайте молярную массу (г/моль) для следующих веществ: NaCl, F2, KOH, SO3.
2. Сколько молей азота содержится в 160 г азота?
3. В стакан налили 100 г хлорида натрия. Сколько это молей? Сколько молекул хлорида натрия в стакане?
4. Между собой прореагировали 1 моль калия и 1 моль хлора. Сколько молей KCl получилось? Какова масса получившегося хлорида калия KCl ?
5. В пассажирский самолет перед началом рейса погрузили 300 кг продуктов (масса без упаковки). Как изменилась масса авиалайнера после того, как в полете пассажирам предложили обед и все продукты были съедены?
6. Уравняйте следующие реакции Ca+ O2 = CaO, HF + KOH = KF+ H2O
7. Какой объем при нормальных условиях (н.у.) занимают 56 г газообразного аргона?
8. Какой объем при н.у. занимают 70 г газообразного хлора?
9. Составьте электронные формулы для следующих элементов: Ва, О, I, S
10. Охарактеризуйте по положению в ПСХЭ следующие элементы В, Р, О, К
11. Составьте схемы образования химической связи для соединений NaF, CaO, Cl2
12. Определите характер связи в приведенных ниже соединениях и разделите их на четыре группы: а) соединения с ковалентными связями, б) с полярными ковалентными связями, в) с ионными связями г) металлическими связями. Решение обоснуйте.
NH3, Na2O, Cl2, CaCl2, LiBr, C, AlF3, Fe, H2, CO, Na, Ni
13. Составьте формулы соединений с кислородом (II) для следующих хим элементов I, Na, B, P, Ba
14. Составьте схемы Льюиса для следующих соединений LiCl, SrO, NH3
15. Составьте формулы соединений с водородом (I) для следующих хим элементов Сl, Li, C, S, Ca
16. Напишите формулы оксидов для следующих элементов Ca, N, C, Fe (II)
17. Продолжите уравнения реакций и назовите полученные вещества Al + C = Na + N2 = Ca + F2 = Rb + S =
18. Рассчитайте массовые доли элементов в следующих соединениях Na2SO4, MgO, CsOH
19. В руде содержится 84 % железа, сколько нужно добыть руды, чтобы получить 761 кг железа
20. На фармацевтической фабрике производят глицин. В лабораторию принесли образец массой 3,493 г, анализ показал наличие чистого вещества в размере 3,399 г. Допустимая доля примесей 1%. Можно ли выпускать продукцию?
21. Составить формулы веществ : оксид натрия, оксид серы(IV), оксид алюминия , гидроксид цинка, гидроксид хрома(III), серная кислота, азотная кислота , соляная кислота.
22. Написать формулы оснований и кислот, которые соответствуют данным оксидам :
SО3, Na2О, Al2O3, СО2, ВаО
23. Напишите реакцию нейтрализации полное и сокращенное ионное уравнение:
H2SO4 + NaOH = HCl + Ca(OH)2 = H2SiO3 + LiOH =
24. Выпишите формулы бескислородных кислот HBr, H2SO4, HF, H2SiO3, H2MnO4, H2S, H2CO3
25. Выпишите в правый столбик формулы щелочей в левый столбик нерастворимые основания NaOH, KOH, Fe(OH)2, Fe(OH)3, LiOH, Ba(OH)2
26. Среди заданных вам веществ найдите оксиды, основания, кислоты и соли. Дайте им названия. ZnSO4, Na2O, NaOH, HCl, NaNO3, Cl2O5, Fe(OH)3, H2SO4, FeO, CuCl2.
27. К какому типу можно отнести каждую из приведенных реакций? (ОВР и не ОВР)
MgCO3 = MgO + CO2 HCl + NH3 = NH4Cl
FeSO4 + Cu = CuSO4 + Fe HCl + NaOH = NaCl + H2O
28. Уравняйте следующие реакции методом электронного баланса
Ca + O2 = CaO Na + Cl2 = NaCl
29. Составьте сжемы электролиза для следующих расплавов : Li J K2S MgSO4 AlCl3 32. 30. Составьте схемы электролиза расстворов: CaCl2 NaNO3 BaCO3
31. В 80 г воды растворили два кусочка сахара, каждый из которых весит по 4,5 г. Определить массовую долю сахара в полученном растворе.
32.Для приготовления коктейля к 500 мл воды добавили 32 г тростникового сахара, 20 г клубничного сиропа и лепестки мяты общей массой 20 г. Чему равна массовая доля клубничного сиропа в таком коктейле?
33.Смешали 150 г 60 %-го раствора и 110 г 40 %-го раствора. Определить массовую долю растворенного вещества в полученном растворе.
34.Сколько граммов NaNO3 необходимо взять для приготовления 1 л раствора с концентрацией 0,1 моль/л (0,1М)?
35.Какая молярная концентрация раствора поваренной соли объемом 700 мл содержащем 3 моль этого вещества.
36. Как приготовить 200 г 5% раствор спирта для компресса если вы имеете 40% раствор.
37. Хозяйке для маринада требуется 250г 9% уксуса, у нее есть уксусная эссенция 78%, как ей приготовить нужный раствор
38. Напишите структурные формулы всех изомеров гексана.
39. Составить 3 структурные формулы изомерных углеводородов состава С7Н16
40. Назовите по систематической номенклатуре вещества следующего состава