ФОРМИРУЮЩЕЕ ОЦЕНИВАНИЕ НА УРОКАХ ХИМИИ
В УСЛОВИЯХ РЕАЛИЗАЦИИ ФГОС.
При реализации Федерального государственного образовательного стандарта (ФГОС) большое внимание уделяется оцениванию результатов обучения. Оценивание выступает одновременно и как цель, и как средство обучения.
ФГОС предъявляют к процессу оценивания следующие требования:
оценивание достигаемых образовательных результатов (личностных, метапредметных, предметных);
оценивание процесса их формирования;
оценивание осознанности каждым обучающимся особенностей развития его собственного процесса обучения.
Формирующее (формативное) оценивание - это целенаправленный непрерывный процесс наблюдения за учением ученика. Оно основывается на оценивании в соответствии с критериями и предполагает обратную связь. Результаты ученика сравниваются с его предыдущими результатами. Происходит мотивирование обучающихся, постановка образовательных целей и определение путей их достижения.
Целью формирующего оценивания является корректировка деятельности учителя и обучающихся в процессе обучения на основе промежуточных результатов, полученных в процессе обучения.
Оценивать деятельность учеников необходимо строго по критериям. Формулировать конкретные критерии оценивания деятельности обучающихся на уроке, можно совместно с обучающимися. Ученики должны заранее знать критерии оценивания выполнения работы. При выборе критериев необходимо помнить, что они должны обладать следующими характеристиками:
- быть однозначными, т.е. результат оценивания не должен зависеть от личностей оценивающего и оцениваемого;
- быть понятными не только учителю, но и ученикам, чтобы они могли проводить самооценку и взаимооценку работ;
- быть конкретными, чтобы дать возможность однозначно оценить результат деятельности ученика.
Методы и приемы формирующего оценивания классифицируют по цели применения, по времени проведения, по возможности использования. Оценивание по итогам изучения темы: «индекс карточки», «одноминутное эссе», «цепочка заметок», «вопросы для тестов», «карты приложения», «недельный отчет», «две звезды и желание». Оценивание в ходе урока: «сигналы рукой», «речевые образцы», «поиск ошибки». Оценивание метапознавательных процессов: «Уточнение с помощью вопроса почему?», «рассуждение по алгоритму", «если бы я был учителем», «перевод информации».
Рассмотрим возможности применения приема «рассуждение по алгоритму». На уроке химии в 8 классе, по теме: «Окислительно-восстановительные реакции», на этапе первичного закрепления совместно с обучающимися составляется алгоритм записи окислительно-восстановительных реакций (ОВР).
Алгоритм записи окислительно-восстановительной реакции (ОВР)
| № | Действие | Пример |
| I | Определить степень окисления ХЭ. |
Zn0 + H+1 Cl-1 → Zn+2 Cl2-1 + H20↑ |
| II | Сравнить, как изменилась степень окисления химических элементов, сделать вывод – является ли данная химическая реакция ОВР. | Степень окисления цинка изменилась с 0 на +2, степень окисления водорода изменилась с +1 на 0 – данная реакция является ОВР. |
| III | Подчеркнуть знаки ХЭ, которые изменили свою степень окисления. |
Zn0 + H+1 Cl-1 → Zn+2 Cl2-1 + H20↑ |
| IV | Составить электронный баланс: |
|
| 1 | Выписать знаки ХЭ которые изменили свою степень окисления (если в балансе есть простые вещества (неметаллы), то перед ионом необходимо поставить соответствующий коэффициент). |
Zn0 ± ? ē → Zn+2 2H+1 ± ? ē → H20 |
| 2 | Определить и записать какое количество электронов отдает или присоединяет атом, ион или молекула. |
Zn0 - 2ē → Zn+2 2H+1 + 2ē → H20 |
| 3 | Определить и записать чем является атом, ион или молекула: восстановителем или окислителем. |
Zn0 - 2ē → Zn+2 в-ль 2H+1 + 2ē → H20 ок-ль |
| 4 | Определить и записать для каждого атома, иона или молекулы какой процесс протекает: окисление или восстановление. |
Zn0 - 2ē → Zn+2 в-ль/ок-ие 2H+1 + 2ē → H20 ок-ль/в-ие |
| 5 | В электронном балансе напротив восстановителя и окислителя подобрать и записать общий знаменатель и коэффициенты. |
  1 Zn0 - 2ē → Zn+2 в-ль/ок-ие 1 Zn0 - 2ē → Zn+2 в-ль/ок-ие
2 1 2H+1 + 2ē → H20 ок-ль/в-ие |
| V | Выписать из электронного баланса коэффициенты в уравнение химической реакции перед восстановителем и окислителем и подобрать недостающие коэффициенты. (Если водород и кислород не меняет своих степеней окисления, то их количество подсчитывают в последнюю очередь и добавляют нужное количество молекул воды в левую или правую часть уравнения) |
Zn0 + 2H+1 Cl-1 → Zn+2 Cl2-1 + H20↑
  1 Zn0 - 2ē → Zn+2 в-ль/ок-ие 1 Zn0 - 2ē → Zn+2 в-ль/ок-ие
2 1 2H+1 + 2ē → H20 ок-ль/в-ие
|
Составив алгоритм действий, обучающиеся приобретают инструмент составления ОВР и оценивания своей работы. В данном алгоритме получилось 9 действий, которые и выступают в роли критериев оценивания и определения зоны ближайшего развития обучающегося. Вместе с обучающимися 9 действий/критериев переводится в оценку:
| Количество баллов | % выполнения | Оценка |
| 9 баллов | 80-100 % | 5 |
| 8 баллов | 65-80 % | 4 |
| 6 - 7 баллов | 55 -65 % | 3 |
| 5 баллов | менее 55 % | 2 |
Во время последовательного выполнения алгоритма действий ученик определяет область «знаю-могу» и «не знаю-не могу». Для успешного выполнения области «не знаю-не могу», ученику необходимо предоставить справку, которая дает пояснения на каждый шаг алгоритма:
| № | Справка |
| I | Как определить степень окисления ХЭ в соединении? 
|
| II | К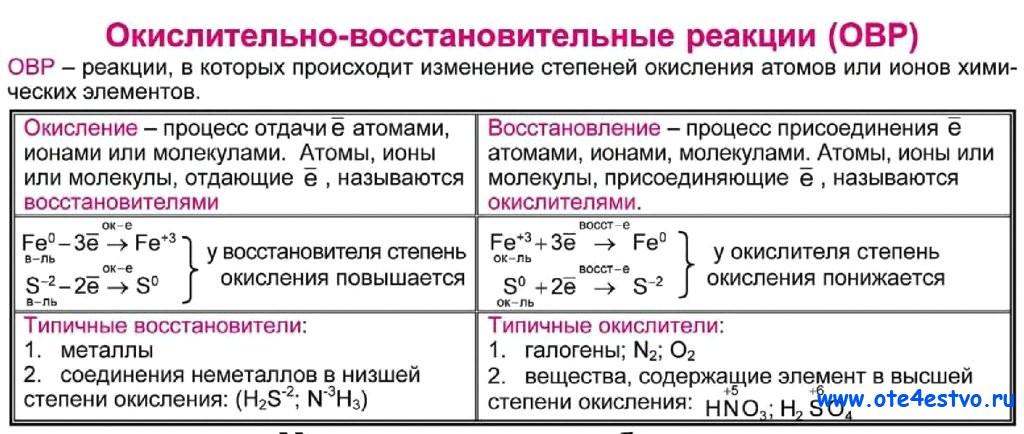 ак определить является ли химическая реакция ОВР? ак определить является ли химическая реакция ОВР? |
| IV | Как составить электронный баланс? |
| 2 | Как определить какое количество электронов отдает или присоединяет атом, ион или молекула? Al0 ± ? ē → Al+3 Степень ХЭ изменилась с 0 на +3, составляем выражение (по формуле: x – (± y) = ?) и раскрываем скобки: 0 – (+3) = - 3, из расчетов следует, что ХЭ отдал 3 электрона. Запись приобретает следующий вид: Al0 – 3 ē → Al+3 |
| 3 | Как определить чем является атом, ион или молекула: восстановителем или окислителем? |
| Восстановитель | Окислитель |
| А томы, ионы или молекулы, отдающие электроны томы, ионы или молекулы, отдающие электроны | Атомы, ионы или молекулы, п рисоединяющие электроны рисоединяющие электроны
|
| 4 | Как определить для каждого атома, иона или молекулы какой процесс протекает: окисление или восстановление? |
| Процесс окисления | Процесс восстановления |
| П роцесс отдачи электронов атомами, ионами или молекулами. роцесс отдачи электронов атомами, ионами или молекулами.
| П роцесс присоединения электронов атомами, ионами или молекулами. роцесс присоединения электронов атомами, ионами или молекулами. |
либо можно организовать самостоятельный поиск информации в учебнике. При данной работе осуществляется индивидуализация обучения.
Создавая алгоритм действий, выполняя задания по составлению ОВР, проводя самооценивание и взаимооценивание, у обучающихся формируются:
умение самостоятельно определять цели обучения, ставить и формулировать новые задачи в учебной и познавательной деятельности, развивать мотивы и интересы своей познавательной деятельности;
умение самостоятельно планировать пути достижения целей, в том числе альтернативные, осознано выбирать наиболее эффективные способы решения учебных и познавательных задач;
умение соотносить свои действия с планируемыми результатами, осуществлять контроль своей деятельности в процессе достижения результата, определять способы действий в рамках предложенных условий и требований, корректировать свои действия в соответствии с изменяющейся ситуацией;
умение оценивать правильность выполнения учебной задачи, собственные возможности ее решения.
Анализируя вместе с учениками выполненные письменные работы, гораздо лучше предложить ученикам отметить, что наиболее удачным, по их мнению, было в работе у одноклассника, а что необходимо улучшить, таким образом исключаются все негативные и критические высказывания, создается ситуация успеха. Чтобы ученики могли дать оценки работам одноклассников, учителю необходимо дать критерии оценивания, а если это старшеклассники, то результативнее разработать критерии совместно с учениками. И ещё, я считаю, что учитель, высказывая своё мнение должен отметить прогресс, достигнутый в данной работе по сравнению с предыдущими. Например, умение расставлять коэффициенты в уравнении химической реакции: ученик научился составлять формулы веществ, знает, что получится в ходе химической реакции, но неправильно расставляет коэффициенты. В таком случае, групповая или парная работа с более успевающим в этой теме учеником возможно позволит ему понять лучше правила расставления коэффициентов, контроль этого умения и совместный анализ результатов работы дадут возможность к постановке последующих задач.
Еще один интересный блиц - опрос, который я часто практикую на уроках. Отводя на него не более 5 мин., ученикам предлагается обсудить с соседом по парте то, что они поняли или не поняли из темы прошлого урока. Проговаривая, учащийся фиксирует свое внимание на непонятых моментах. Возникает парный процесс обсуждения, если для обоих в группе оказались одинаковые сложности, то прибегаем к помощи класса при коллективном обсуждении. Время на коллективное обсуждение зависит от сложности темы, количества обсуждаемых вопросов. Но в целом неясных моментов остаться не должно. Цель данного действа не контрольный опрос, а диагностика того, что дети понимают на данный момент и каковы их возможности продвижения. В целом урок можно завершить обсуждением всех учебных целей, показать, как учение будет развиваться, как сегодняшний этап учебы связан с тем, как они будут учиться в дальнейшем.
Карта самодиагностики по теме «Простые вещества. Решение расчетных задач»
| Насколько уверенно ты чувствуешь себя в следующих ситуациях. | Очень уверенно | Уверенно | Довольно уверенно | неуверенно |
| Я могу рассчитать массу вещества по известному количеству вещества. |
|
|
|
|
| Я могу рассчитать число частиц по известной массе или объему вещества |
|
|
|
|
| Я могу рассчитать объём вещества по известной массе вещества. |
|
|
|
|
Как вывод из всего сказанного: основная цель формирующего оценивания - максимальное увеличение включенности учеников в учебную активность, во все виды учебной работы, чтобы изменялась их роль в учебном процессе из пассивной в активную. Хотелось бы, чтобы возрастала ответственность учеников за то, как они учатся, к каким результатам приходят, чтобы у них появлялась уверенность в том, что добьются успешности, благодаря своим усилиям.
Таким образом, формирующее оценивание выступает как процесс формирования качества индивидуальных учебных достижений, направленный на своевременное обеспечение наглядной обратной связи в условиях комплексного подхода в обучении, а технология формирующего оценивания как описание средств и условий достижения планируемых результатов, позволяющего целенаправленно, планомерно, критериально-ориентированно обеспечивать гарантированное качество учебных достижений, регламентируя действия учителя и ученика. Что способствует успешной реализации ФГОС.
3








 ак определить является ли химическая реакция ОВР?
ак определить является ли химическая реакция ОВР?









