Практическая работа №1 «Правила ТБ при работе в химическом кабинете. Ознакомление с лабораторным оборудованием».
Цель работы: познакомится с устройством лабораторного штатива и спиртовки, научиться пользоваться и изучить строение пламени.
1. Приемы обращение с лабораторным штативом. Рассмотрите штатив.
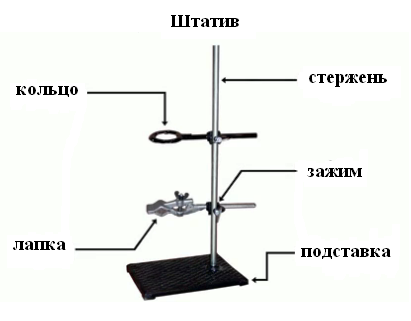
2. Приемы обращения со спиртовкой.

Снимите колпачок со спиртовки, проверьте, плотно ли диск прилегает к отверстию резервуара, иначе спирт в нём может загореться. Зажгите спиртовку спичкой. Погасите спиртовку, накрыв пламя колпачком.
3. Изучение строения пламени. Внимательно рассмотрите её пламя.

4. Сделайте выводы, оформите работу в тетради.
Практическая работа №2 «Очистка загрязнённой поваренной соли»
Цель работы: научиться очищать загрязненную поваренную соль, при помощи фильтрования и выпаривания.
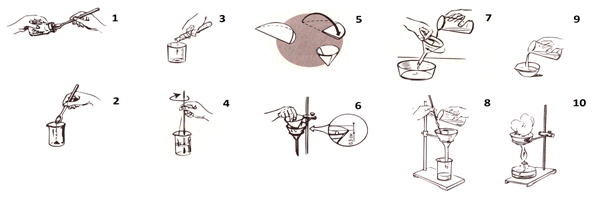
Опыт 1. Растворение загрязненной поваренной соли:
Возьмите из банки сухой чистой ложкой загрязнённую поваренную соль.
Насыпьте в стакан порцию соли.
Добавьте в стакан воды на 1/3 его высоты.
Осторожно размешайте содержимое стеклянной палочкой.
Опыт 2. Очистка полученного раствора при помощи фильтрования:
Приготовьте фильтр как показано на рисунке.
Вложите фильтр в воронку так, чтобы он: А) плотно прилегал к стенкам, Б) не доходил до края воронки на 0,5 см.
Слегка смочите фильтр водой.
Наливайте фильтруемую жидкость на фильтр по стеклянной палочке, направив её нижний конец к стенке воронки, а не в середину фильтра, чтобы не прорвать его.
Опыт 3. Выпаривание раствора:
Вылейте фильтрат (раствор соли) в фарфоровую выпаривательную чашку до ½ её объёма.
Поставьте чашку на кольцо штатива. Зажгите спиртовку. Нагревайте фильтрат до начала образования кристаллов соли.
Оформите в тетради отчёт о работе в виде таблицы:
| Что делали (название опытов, рисунки приборов с обозначениями) | Что наблюдали | Выводы |
| Растворение соли в воде. |
|
|
| Фильтрование. |
|
|
| Выпаривание фильтрата (раствора соли). |
|
|
Практическая работа №3 «Получение и свойства кислорода»
Цель работы: получить кислород и изучить его свойства.
Опыт 1. Получение и собирание кислорода:
1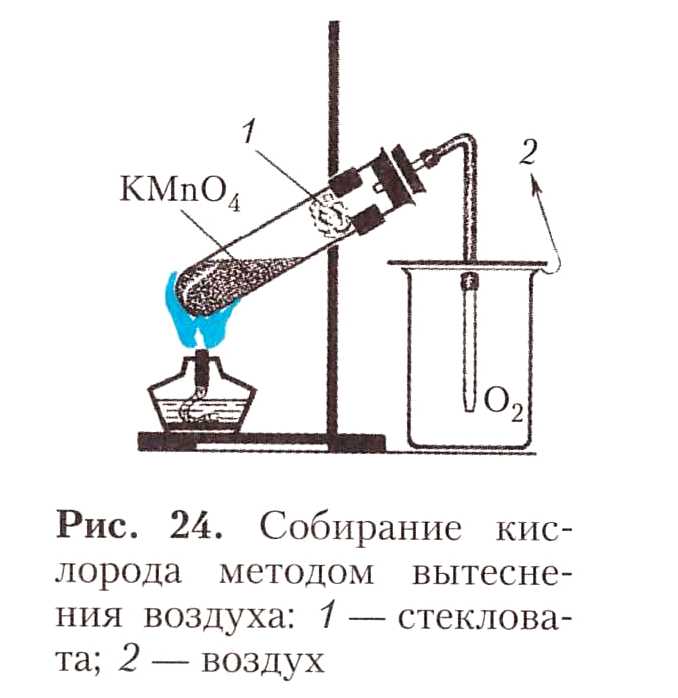 . Соберите прибор как показано на рисунке и проверьте его на герметичность. В пробирку насыпьте примерно ¼ её объёма перманганата калия и у отверстия пробирки положите рыхлый кусочек ваты. Закройте пробирку пробкой с газоотводной трубкой. Укрепите пробирку в лапке штатива так, чтобы конец газоотводной трубки почти доходил до дна стакана, в котором будет собираться кислород. Сначала обогрейте всю пробирку. Затем постепенно передвигайте пламя от её дна в сторону пробки. Полноту заполнения стакана кислородом проверяйте тлеющей лучинкой. Как только стакан наполнится кислородом, закройте его картоном. Запишите уравнение реакции получения кислорода.
. Соберите прибор как показано на рисунке и проверьте его на герметичность. В пробирку насыпьте примерно ¼ её объёма перманганата калия и у отверстия пробирки положите рыхлый кусочек ваты. Закройте пробирку пробкой с газоотводной трубкой. Укрепите пробирку в лапке штатива так, чтобы конец газоотводной трубки почти доходил до дна стакана, в котором будет собираться кислород. Сначала обогрейте всю пробирку. Затем постепенно передвигайте пламя от её дна в сторону пробки. Полноту заполнения стакана кислородом проверяйте тлеющей лучинкой. Как только стакан наполнится кислородом, закройте его картоном. Запишите уравнение реакции получения кислорода.
Опыт 2. Горение в кислороде угля:
Положите в железную ложечку кусочек древесного угля и раскалите его в пламени. Затем ложечку с тлеющим углём внесите в сосуд с кислородом и наблюдайте за происходящим. Запишите уравнение реакции горения угля (С).
Результаты работы оформите в виде таблицы:
| Что делали (название опытов, рисунки приборов с обозначениями) | Что наблюдали | Выводы |
|
|
|
|
Практическая работа №3 «Получение и свойства кислорода»
Цель работы: получить кислород и изучить его свойства.
Опыт 1. Получение и собирание кислорода:
1 . Соберите прибор как показано на рисунке и проверьте его на герметичность. В пробирку насыпьте примерно ¼ её объёма перманганата калия и у отверстия пробирки положите рыхлый кусочек ваты. Закройте пробирку пробкой с газоотводной трубкой. Укрепите пробирку в лапке штатива так, чтобы конец газоотводной трубки почти доходил до дна стакана, в котором будет собираться кислород. Сначала обогрейте всю пробирку. Затем постепенно передвигайте пламя от её дна в сторону пробки. Полноту заполнения стакана кислородом проверяйте тлеющей лучинкой. Как только стакан наполнится кислородом, закройте его картоном. Запишите уравнение реакции получения кислорода.
. Соберите прибор как показано на рисунке и проверьте его на герметичность. В пробирку насыпьте примерно ¼ её объёма перманганата калия и у отверстия пробирки положите рыхлый кусочек ваты. Закройте пробирку пробкой с газоотводной трубкой. Укрепите пробирку в лапке штатива так, чтобы конец газоотводной трубки почти доходил до дна стакана, в котором будет собираться кислород. Сначала обогрейте всю пробирку. Затем постепенно передвигайте пламя от её дна в сторону пробки. Полноту заполнения стакана кислородом проверяйте тлеющей лучинкой. Как только стакан наполнится кислородом, закройте его картоном. Запишите уравнение реакции получения кислорода.
Опыт 2. Горение в кислороде угля:
Положите в железную ложечку кусочек древесного угля и раскалите его в пламени. Затем ложечку с тлеющим углём внесите в сосуд с кислородом и наблюдайте за происходящим. Запишите уравнение реакции горения угля (С).
Результаты работы оформите в виде таблицы:
| Что делали (название опытов, рисунки приборов с обозначениями) | Что наблюдали | Выводы |
|
|
|
|
Практическая работа №4 «Получение водорода и изучение его свойств»
Цель работы: получить водород и изучить его свойства.
Опыт 1. Получение водорода:
Поместите в пробирку 2-3 гранулы цинка и прилейте 2 мл раствора соляной кислоты. Закройте пробирку пробкой с газоотводной трубкой. Накройте газоотводную трубку пробиркой (вверх дном) и выждите несколько секунд, пока из пробирки вытиснится воздух.
Опыт 2. Горение водорода:
Проверьте водород «на чистоту». Для этого пробирку, наполненную водородом, держа отверстием вниз, поднесите к пламени спиртовки. Если вы услышите легкий звук, напоминающий “п - пах”, вы собрали чистый водород. Если водород содержит примеси воздуха, слышен характерный свистящий хлопок.
Результаты работы оформите в виде таблицы:
| Что делали (название опытов, рисунки приборов с обозначениями) | Что наблюдали | Выводы |
|
|
|
|
|
|
|
|
Практическая работа №4 «Получение водорода и изучение его свойств»
Цель работы: получить водород и изучить его свойства.
Опыт 1. Получение водорода:
Поместите в пробирку 2-3 гранулы цинка и прилейте 2 мл раствора соляной кислоты. Закройте пробирку пробкой с газоотводной трубкой. Накройте газоотводную трубку пробиркой (вверх дном) и выждите несколько секунд, пока из пробирки вытиснится воздух.
Опыт 2. Горение водорода:
Проверьте водород «на чистоту». Для этого пробирку, наполненную водородом, держа отверстием вниз, поднесите к пламени спиртовки. Если вы услышите легкий звук, напоминающий “п - пах”, вы собрали чистый водород. Если водород содержит примеси воздуха, слышен характерный свистящий хлопок.
Результаты работы оформите в виде таблицы:
| Что делали (название опытов, рисунки приборов с обозначениями) | Что наблюдали | Выводы |
|
|
|
|
|
|
|
|
Практическая работа №5
«Приготовление растворов солей с определённой массовой долей растворённого вещества»
Цель работы: научиться готовить растворы с определенной массовой долей.
Задача. Приготовьте 50 граммов раствора поваренной соли в воде, с массовой долей соли 5%.
Инструкция:
1. Вычислите, сколько соли и сколько воды потребуется для приготовления данного раствора.
2. Отмерьте на весах необходимую массу соли и поместите её в стаканчик.
3. Отмерьте необходимый объём воды и влейте её в стакан с солью. Содержимое стакана тщательно перемешайте.
Сделайте выводы, оформите работу в тетради.
Практическая работа №5
«Приготовление растворов солей с определённой массовой долей растворённого вещества»
Цель работы: научиться готовить растворы с определенной массовой долей.
Задача. Приготовьте 50 граммов раствора поваренной соли в воде, с массовой долей соли 5%.
Инструкция:
1. Вычислите, сколько соли и сколько воды потребуется для приготовления данного раствора.
2. Отмерьте на весах необходимую массу соли и поместите её в стаканчик.
3. Отмерьте необходимый объём воды и влейте её в стакан с солью. Содержимое стакана тщательно перемешайте.
Сделайте выводы, оформите работу в тетради.
Практическая работа №5
«Приготовление растворов солей с определённой массовой долей растворённого вещества»
Цель работы: научиться готовить растворы с определенной массовой долей.
Задача. Приготовьте 50 граммов раствора поваренной соли в воде, с массовой долей соли 5%.
Инструкция:
1. Вычислите, сколько соли и сколько воды потребуется для приготовления данного раствора.
2. Отмерьте на весах необходимую массу соли и поместите её в стаканчик.
3. Отмерьте необходимый объём воды и влейте её в стакан с солью. Содержимое стакана тщательно перемешайте.
Сделайте выводы, оформите работу в тетради.
Практическая работа №6
Решение экспериментальных задач по теме
«Важнейшие классы неорганических соединений».
Цель работы: Закрепить знания по теме «Важнейшие классы неорганических соединений».
Задача 1. Даны два твердых вещества: оксид кальция и оксид меди (II).
Как различить эти вещества, не проводя химических опытов?
Как химическими опытами подтвердить наличие в склянках именно этих веществ?
Задача 2. В склянке находиться бесцветный раствор. Предполагают, что это раствор фенолфталеина. Проведите опыт, подтверждающий или опровергающий это предположение.
Задача 3. Из имеющихся на столе реактивов получите несколькими способами сульфат меди (II).
Сделайте выводы, оформите работу в тетради.
Практическая работа №6
Решение экспериментальных задач по теме
«Важнейшие классы неорганических соединений».
Цель работы: Закрепить знания по теме «Важнейшие классы неорганических соединений».
Задача 1. Даны два твердых вещества: оксид кальция и оксид меди (II).
Как различить эти вещества, не проводя химических опытов?
Как химическими опытами подтвердить наличие в склянках именно этих веществ?
Задача 2. В склянке находиться бесцветный раствор. Предполагают, что это раствор фенолфталеина. Проведите опыт, подтверждающий или опровергающий это предположение.
Задача 3. Из имеющихся на столе реактивов получите несколькими способами сульфат меди (II).
Сделайте выводы, оформите работу в тетради.
Практическая работа №6
Решение экспериментальных задач по теме
«Важнейшие классы неорганических соединений».
Цель работы: Закрепить знания по теме «Важнейшие классы неорганических соединений».
Задача 1. Даны два твердых вещества: оксид кальция и оксид меди (II).
Как различить эти вещества, не проводя химических опытов?
Как химическими опытами подтвердить наличие в склянках именно этих веществ?
Задача 2. В склянке находиться бесцветный раствор. Предполагают, что это раствор фенолфталеина. Проведите опыт, подтверждающий или опровергающий это предположение.
Задача 3. Из имеющихся на столе реактивов получите несколькими способами сульфат меди (II).
Сделайте выводы, оформите работу в тетради.










 . Соберите прибор как показано на рисунке и проверьте его на герметичность. В пробирку насыпьте примерно ¼ её объёма перманганата калия и у отверстия пробирки положите рыхлый кусочек ваты. Закройте пробирку пробкой с газоотводной трубкой. Укрепите пробирку в лапке штатива так, чтобы конец газоотводной трубки почти доходил до дна стакана, в котором будет собираться кислород. Сначала обогрейте всю пробирку. Затем постепенно передвигайте пламя от её дна в сторону пробки. Полноту заполнения стакана кислородом проверяйте тлеющей лучинкой. Как только стакан наполнится кислородом, закройте его картоном. Запишите уравнение реакции получения кислорода.
. Соберите прибор как показано на рисунке и проверьте его на герметичность. В пробирку насыпьте примерно ¼ её объёма перманганата калия и у отверстия пробирки положите рыхлый кусочек ваты. Закройте пробирку пробкой с газоотводной трубкой. Укрепите пробирку в лапке штатива так, чтобы конец газоотводной трубки почти доходил до дна стакана, в котором будет собираться кислород. Сначала обогрейте всю пробирку. Затем постепенно передвигайте пламя от её дна в сторону пробки. Полноту заполнения стакана кислородом проверяйте тлеющей лучинкой. Как только стакан наполнится кислородом, закройте его картоном. Запишите уравнение реакции получения кислорода. 









