Просмотр содержимого документа
«Ионные уравнения»

Самостоятельная работа.
Варианты I, II, III.
«А» - оценка 3;
«В» - оценка 4;
«С» - оценка 5.

Тема урока: ИОННЫЕ УРАВНЕНИЯ.
Задачи урока:
- закрепить знания об «ионах»;
- сформировать понятия: «ионные реакции», «ионные уравнения»;
- научить составлять полные и краткие ионные уравнения реакций, используя алгоритм.

Домашнее задание:
§ 37. упр. 1, 2, 5.

Ионные реакции – взаимодействие между ионами в растворах. Они протекают в направлении полного связывания ионов , то есть образования осадка , газа или малодиссоциирующего вещества , например воды H 2 O , а уравнения таких реакций – ионные уравнения.

Основные правила составления ионных уравнений реакций:
- Сильные электролиты записывают в виде образующих их ионов
(с учетом индексов и коэффициентов).
- Формулы слабых электролитов (в том числе H 2 O ), нерастворимых и газообразных веществ записываются в молекулярной форме.

- Если вещество выпадает в осадок, то рядом с его формулой ставят стрелку , направленную вниз ,а если в ходе реакции образуется газообразное вещество, то рядом с его формулой ставят стрелку , направленную вверх .
Ионные уравнения могут быть полными и сокращенными.

АЛГОРИТМ СОСТАВЛЕНИЯ ИОННЫХ УРАВНЕНИЙ РЕАКЦИЙ
- 1. Запишите схему реакции (письменно)
- 2. Проверьте растворимость в воде исходных веществ и продуктов реакции (см. таблица «Растворимость оснований, кислот и солей в воде» (форзац учебника)) (устно)
- 3. Отметьте формулу продукта реакции, уходящего из сферы реакции, соответствующим знаком (см.: Правило)
( устно )

- 4. Запишите молекулярные уравнения реакции, расставьте коэффициенты (письменно)
- 5. Составьте полное ионное уравнение реакции (сильные электролиты записывают в виде образующих их ионов (с учетом индексов и коэффициентов, и молекулярные формулы осадка, газа или воды)) (письменно)
- 6. Подчеркните формулы одинаковых ионов в левой и правой частях уравнения реакции
(письменно)

- 7. Составьте краткое ионное уравнение реакции из оставшихся неподчеркнутыми формул ионов и веществ (письменно)
- 8. Сделайте вывод (устно) .
Сущность ионной реакции – в связывании ионов.

Na 2 SO 4 + ВаС l 2 = 2 NaCl +BaSO 4
молекулярное уравнение

2Na + + SO 4 2- + Ва 2+ + 2 С l - = 2Na + + 2 С l - + BaSO 4
полное ионное уравнение
реакции

SO 4 2- + Ва 2+ = BaSO 4
сокращенное ионное уравнение реакции

NaOH + HNO 3 = NaNO 3 + H 2 O (реакция нейтрализации)
молекулярное уравнение
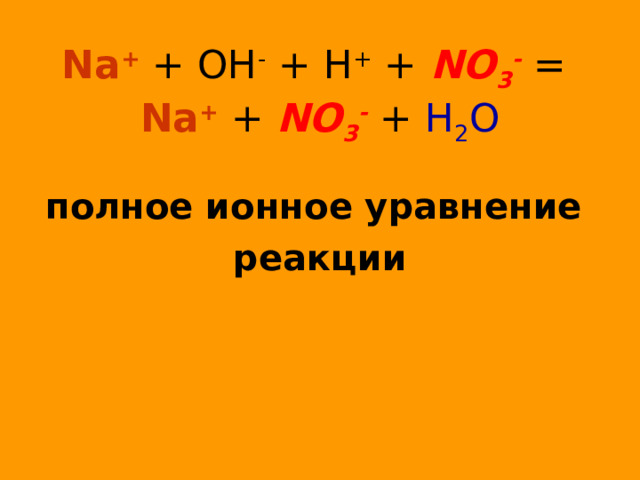
Na + + OH - + H + + NO 3 - = Na + + NO 3 - + H 2 O
полное ионное уравнение
реакции

H + + OH - = H 2 O
сокращенное ионное уравнение реакции

Na 2 CO 3 + 2Н Cl = 2 NaCl + Н 2 O + СО 2
молекулярное уравнение

2 Na + + СО 3 2- + 2Н + + 2 Cl - = 2 Na + + 2 Cl - + Н 2 О + СО 2
полное ионное уравнение
реакции

СО 3 2- + 2Н + = Н 2 О + СО 2
сокращенное ионное уравнение реакции

молекулярное уравнение
CuSO 4 + 2KOH = Cu(OH) 2 + K 2 SO 4
полное ионное уравнение реакции
Cu 2+ + SO 4 2- + 2K + + 2OH - =
Cu(OH) 2 + 2K + + SO 4 2-
сокращенное ионное уравнение реакции
Cu 2+ + 2 OH - = Cu ( OH ) 2



































