Урок на тему: ионные уравнения реакций
Учитель: Пугаченко Е.А.
Тип урока: урок открытия новых знаний
Цель: познакомить с понятием реакции ионного обмена, с условиями, при которых они протекают, формировать навыки составления полных и сокращенных ионных уравнений.
Задачи урока:
1. Образовательные:
-научить учащихся составлению реакций ионного обмена в молекулярном, полном ионном и сокращенных видах;
-выявить условия реакций ионного обмена, при которых они протекают до конца.
2. Развивающие:
-совершенствовать умения и навыки учащихся работы с лабораторным оборудованием и химическими реактивами;
-обеспечить развитие всех видов мышления;
-формировать культуру организации умственного труда;
-развивать у школьников умение оценивать свою работу
3. Воспитательные:
- формировать познавательный интерес к химии;
-способствовать формированию научного мировоззрения;
-выполнение лабораторных опытов с соблюдением правил техники безопасности;
-экономное расходование химических реактивов;
-аккуратное заполнение в рабочих тетрадях учащихся результатов опытов.
На уроке используются следующие методы:
-фронтальная беседа;
-исследовательский;
-объяснительно-иллюстративный;
-частично-поисковый.
Оборудование: химические реактивы: растворы HCl, H2SO4, KOH, BaCl2, Na2CO3, Na2SO4, KCl, фенолфталеин.
Ход урока
I. Организационный момент (3 МИН)
Добрый день! Я рада приветствовать вас сегодня на нашем уроке!
II. Актуализация опорных знаний. (3 МИН)
Прежде чем начать новую тему, проведем разминку
Задание № 1. «Закончите предложение одним словом».
(По цепочке на местах заканчивают предложение).
1. Положительно заряженные частицы -…(катионы).
2. Отрицательно заряженные частицы -…(анионы).
3. Вещества, водные растворы или расплавы которых проводят электрический ток -…(электролиты).
4. Вещества, водные растворы или расплавы которых не проводят электрический ток -…(неэлектролиты).
5. Процесс распада электролита на ионы при растворении или расплавлении вещества -…(диссоциация).
6. Реакции между двумя сложными веществами, при которых они обмениваются своими составными частями – ….(обмена)
7. Заряженные частицы, которые отличаются от атомов числом электронов ...(ионы)
8. На какие ионы распадаются при электролитической диссоциации кислоты… (ионы водорода и ионы кислотного остатка)
9. На какие ионы распадаются при электролитической диссоциации растворимые основания?... (ионы металла и ионы ОН-1 групп)
10. На какие ионы распадаются при электролитической диссоциации соли? …(ионы металла и ионы кислотного остатка)
Мотивация. Определение темы. Цели (5 МИН)
До изучения ТЭД, мы рассматривали эти реакции как взаимодействие молекул, теперь мы вами знаем, что в растворах этих веществ молекул практически нет, а есть ионы водорода, гидроксид-ионы, ионы металлов и кислотных остатков.
- Как будут называться реакции обмена между ионами?
- ионные реакции
- Химические реакции мы записываем при помощи химических уравнений, а ионные реакции мы запишем при помощи – чего?
- Ионных уравнений
- Сформулируйте тему урока?
- Ионные уравнения
Запишите тему урока в свои рабочие тетради «Ионные уравнения»
Попробуйте поставить цели сегодняшнего урока
Цель: На сегодняшнем уроке мы должны выяснить, какие реакции называются реакциями ионного обмена, каковы условия протекания реакций обмена до конца и научиться составлять ионные уравнения.
III. Изучение нового материала
Вы уже знакомы с реакциями обмена. Теперь вам известно, что в растворах кислот, оснований и солей молекул практически нет, а есть ионы водорода, гидроксид-ионы, ионы металлов и кислотных остатков. Отсюда следует вывод, что реакции между растворами этих веществ сводятся к взаимодействию ионов. А какие вещества пишут с помощью ионов, а какие- молекулами. Какие признаки реакций есть?
Постановка проблемного вопроса
Опыты 1)сульфат меди и гидроксид натрия
2) Хлорид натрия и гидроксид калия
Записываем 1 уравнение. Идет ли реакция? Почему? разбираем полное и сокращенное уравнения
А 2 реакция идет? Ответим в конце урока (РАЗОБРАТЬ НА ЛАБОРАТОРНОЙ)
Существуют обратимые реакции обмена, но они практического смысла не имеют, их не проводят и не используют. А вот важный смысл имеют реакции необратимые, это реакции про которые можно сказать, что они идут до конца. Тогда возникает вопрос «А можем ли мы предсказать, какая реакция обмена будет необратима. Что для этого нужно знать?» Обратимые и необратимые реакции. Что нужно для необратимых реакций
Попробуйте сформулировать понятие «ионные реакции».
Сейчас вы проведете лабораторные исследования и ответите на вопрос какая реакция обмена будет необратима и идет ли наша 2 реакция
Выполняют в парах лабораторную работу (Приложение)
ТБ вспомнить
Все ли реакции, протекающие в растворах между двумя сложными веществами, будут протекать до конца? Что на это ответит группа №4
Учащиеся отмечают, что в данном случае нет признаков реакции. Записывают уравнение реакции, работают с таблицей растворимости, делают вывод, что данная реакция не идет до конца, т.к. не происходит связывания ионов.
Учитель.
Сделайте вывод об условиях течения реакций ионного обмена до конца (учащиеся перечисляют признаки химических реакций)
Вывод: 1. Реакции в водных растворах электролитов являются реакциями между ионами, и поэтому их изображают в виде ионных уравнений.
2. Реакции ионного обмена в растворах электролитов практически необратимо протекают только в том случае, если в результате образуется осадок, газ или малодиссоциирующее вещество (вода).
IV. Закрепление изученного материала
Вот мы рассмотрели реакции ионного обмена и их условия. Теперь проверим, на сколько вы усвоили новую тему:
1.Могут ли одновременно находиться в одном и том же растворе ионы (Одновременно не могут находиться в растворе те ионы, которые образуют осадки).
А) Ag+ и CI-
В) Сu2+ и OH-
Г) Ba2+ и SO42-
Д) Ba2+ и NO3-
Е) K+ и CI-
2. упр. 5 стр.209
Приведите молекулярные уравнения реакций для следующих ионных:
А) 3Ca2+ + 2PO43- = Ca3(PO4)2↓
Б) Fe3+ + 3OH- = Fe(OH)3↓
В) 2H+ + S2- = H2S↑
Г) H2SiO3 + 2OH- = SiO32- + 2H2O
Д) Fe(OH)3 + 3H+ = Fe3+ + 3H2O
3.Колдунья с вороном отравили лечебный колодец, в котором был раствор хлористого кальция, который помогал целому городу. Он использовался горожанами при отравлениях, кровотечениях, аллергиях. Они превратили раствор СaCl2 в нерастворимый известняк CaCO3. Помогите жителям «расколдовать» колодец, если в вашем распоряжении есть растворы NaCl, Na2CO3, HCl, H2SO4, Zn(NO3)2.
СаСО3 + 2HCl 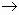 CaCl2 + H2O + CO2
CaCl2 + H2O + CO2 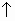
Предложите решение следующей задачи:
Задача 1.
В сточных водах гальванического цеха химического завода обнаружены катионы Fe3+, Fe2+, Ni2+ и анионы Cl-, SO42-. Как с помощью реакций ионного обмена можно очистить эти стоки?
- Поработайте в парах над решением подобных задач:
Задача 2.
Предложите ионные реакции для очистки сточных вод автотранспортного предприятия от катионов Pb2+ и Cu2+, оказывающих токсическое действие на живые организмы.
Задача 3.
В сточных водах животноводческих ферм отмечено повышенное содержание катионов Ca2+ и Zn2+. Предложите реактивы, с помощью которых можно очистить воду от этих ионов.
Обобщение
- Итак, мы рассмотрели реакции, протекающие в растворах электролитов с образованием осадка, газа или малодиссоциирующего вещества: растворы электролитов содержат ионы, следовательно, реакции в растворах электролитов сводятся к реакциям между ионами. Сформулируйте определение понятия «реакции ионного обмена» (реакции между ионами в растворах электролитов, протекающие с выделением осадка, газа или воды)
Значение реакций ионного обмена
- Реакции ионного обмена широко распространены в живой и неживой природе, например, образование осадочных пород (гипс, известняк, другие соли), появление камней в почках животных и человека.
РИО человек применяет в различных направлениях своей деятельности. Одним из таких направлений является живопись.
Живопись, как вид искусства существует с V века до нашей эры. Произведения живописи отражают и оценивают эпоху, когда они были созданы. Поэтому человечество бережно хранит произведения искусства.
Пожар во Всероссийском художественном научно-реставрационном центре имени академика Грабаря, уничтожил множество ценных икон, картин, скульптур. Оставшиеся картины нуждаются в большой реставрации. Для восстановления применяют Капельный метод. В основе которого лежат ионные реакции.
Широко используются реакции ионного обмена и в практических целях, например, для осаждения ионов, приносящих существенный вред людям и животным. К таким относят, в первую очередь, катионы тяжёлых металлов.
Тяжелые металлы - это элементы периодической системы с относительной молекулярной массой больше 40. Так сложилось, что термины "тяжелые металлы" и "токсичные металлы" стали синонимами.
На сегодняшний день безоговорочно к числу токсичных относят кадмий, ртуть, свинец, сурьму. Деятельность значительной части остальных в живых организмах можно оценить только на "отлично". Действительно, металлы в ионной форме входят в состав витаминов, гормонов, регулируют активность ферментов.
Установлено, что для белкового, углеводного и жирового обмена веществ необходимы Mo, Fe, V, Co, W, B, Mn, Zn; в синтезе белков участвуют Mg, Fe, Cu, Zn, Mn, Co; в кроветворении - Co, Cu, Mn, Ni, Zn; в дыхании - Mg, Fe, Cu, Zn, Mn, Co. Справедливо утверждение о том, что нет вредных веществ, есть вредные концентрации. Поэтому ионы меди, кобальта или даже хрома, если их содержание в живом организме не превышает естественного, можно именовать микроэлементами, если же они генеалогически связаны с заводской трубой, то это уже тяжелые металлы. Тяжелые металлы (ртуть, свинец, кадмий, цинк, медь, мышьяк,) относятся к числу распространенных и весьма токсичных загрязняющих веществ. Они широко применяются в различных промышленных производствах, поэтому, несмотря на очистные мероприятия, содержание соединения тяжелых металлов в промышленных сточных водах довольно высокое. Большие массы этих соединений поступают в океан через атмосферу. Для морских биоценозов наиболее опасны ртуть, свинец и кадмий. Ртуть переносится в океан с материковым стоком и через атмосферу.
V. Рефлексия
Учитель: А теперь, в конце урока хочется, чтобы вы выразили свое отношение к нашей сегодняшней работе и всему уроку в целом. Ответьте на вопросы в листах рефлексии и сдайте их мне. (Учащимся выдаются листки с рефлексивным заданием)
1. Я узнал(а) много нового.
2. Мне это пригодится в жизни.
3. На уроке было о чем подумать.
4. На все вопросы, возникающие на уроке, я получил(а) ответы.
Сегодня на уроке мы
1.Выяснили, что …
2.Узнали, что…
3.Научились…
4.Мне понравилось…
Д/З уже записано в маршрутных картах
(п.37, упр. 4 стр.209; Подготовить мультимедийную презентацию о практическом значении реакций ионного обмена (для желающих)).
Ребята, благодарю всех за работу и внимание. Удачи Вам, творчества и успехов!
- VII. Домашнее задание
(п.37, упр. 4 стр.209; Подготовить мультимедийную презентацию о практическом значении реакций ионного обмена (для желающих)).
Ребята, благодарю всех за работу и внимание. Удачи Вам, творчества и успехов!
С какими веществами может реагировать фосфорная кислота, образуя а) газ; б) воду; в) осадок?
Запишите уравнения реакций в молекулярном, полном и сокращённом ионном видах.
Приложение
Лабораторная работа «Реакции ионного обмена»
Цель работы: Изучить реакции ионного обмена и условия их протекания
ХОД РАБОТЫ
Опыт 1. В пробирку налейте 1–2 мл раствора карбоната натрия Na2СO3, добавьте 1 – 2 мл раствора соляной кислоты НCl. Что наблюдаете? Запишите уравнения реакций в молекулярной и сокращенной ионной формах.
Опыт 2. Налейте в пробирку 1мл сульфата меди CuSO4 и добавьте к нему гидроксид натрия NaOH. К полученному осадку добавьте 1–2 мл разбавленного раствора серной кислоты Н2SO4. Что наблюдаете? Запишите уравнения реакций в молекулярной и сокращенной ионной формах.
Опыт 3. В пробирку налейте 1 мл гидроксида натрия и добавьте 1-2 капли фенолфталеина. Какие изменения с раствором происходят? Добавьте к раствору раствор соляной кислоты. Что произошло с образовавшимся раствором?
Опыт 4. В пробирку налейте 0,5–1 мл раствора хлорида меди(II) CuCl2 , затем добавьте примерно такой же объем раствора серной кислоты Н2SO4. Что наблюдаете? Запишите уравнения реакций в молекулярной и сокращенной ионной формах.
Вывод:
















