
ИОННЫЕ УРАВНЕНИЯ РЕАКЦИЙ
9 класс

Запишите
NaCl + AgNO 3 = NaNO 3 + AgCl
1 . К какому типу относится данная реакция?
2. Назовите признаки химических реакций.

Вопросы ???
3. Что такое реакции обмена? (это реакции между двумя сложными веществами, при которых они обмениваются своими составными частями).
4. Что такое ионы? (это заряженные частицы, которые отличаются от атомов числом электронов)
5. На какие группы делятся ионы? (катионы – положительные ионы; анионы – отрицательные ионы)
6. Что такое электролитическая диссоциация? (процесс распада молекул электролитов на ионы при растворении в воде или расплавлении)

ОГЭ (13)
Повторение!
При полной диссоциации 1 моль каких двух из представленных веществ образуется 2 моль анионов?
1) нитрат магния
2) гидроксид бария
3) хлорид натрия
4) фосфат калия
5) сульфат натрия
Запишите номера выбранных ответов.

↓
NaCl + AgNO 3 = NaNO 3 + AgCl
Реакции обмена протекают между ионами, поэтому называются реакции ионного обмена.
Реакции ионного обмена идут до конца в трех случаях:
1. если образуется осадок – нерастворимое вещество после реакции)
2. если выделяется газ
3. если образуется вода (малодислоцированное вещество)
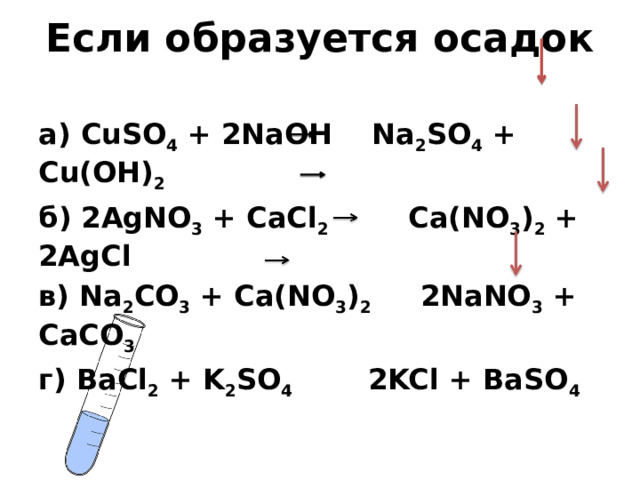
Если образуется осадок
а) CuSO 4 + 2NaOH Na 2 SO 4 + Cu(OH) 2
б) 2AgNO 3 + CaCl 2 Ca(NO 3 ) 2 + 2AgCl
в) Na 2 CO 3 + Ca(NO 3 ) 2 2NaNO 3 + CaCO 3
г) BaCl 2 + K 2 SO 4 2KCl + BaSO 4

Если образуется газ
а)CaCO 3 +2HNO 3 Ca(NO 3 ) 2 + H 2 O + CO 2 (H 2 CO 3 )
б) Na 2 SO 3 + 2HCl 2NaCl + H 2 O + SO 2 (H 2 SO 3 )
в) CuS + 2HCl CuCl 2 + H 2 S

Если образуется вода
а) CuO + H 2 SO 4 CuSO 4 + H 2 O
б) Fe(OH) 3 + 3HCl FeCl 3 + 3 H 2 O
в) NaOH + HNO 3 NaNO 3 + H 2 O

Если НЕ образуются осадок, газ и вода
Обратимые реакции – это реакции, которые при одних и тех же условиях протекают в двух противоположных направлениях
а) 2NaNO 3 + CaCl 2 Ca(NO 3 ) 2 + 2NaCl
б) K 3 PO 4 + 3NaCl Na 3 PO 4 + 3KCl
в) CuCl 2 + Na 2 SO 4 CuSO 4 + 2NaCl
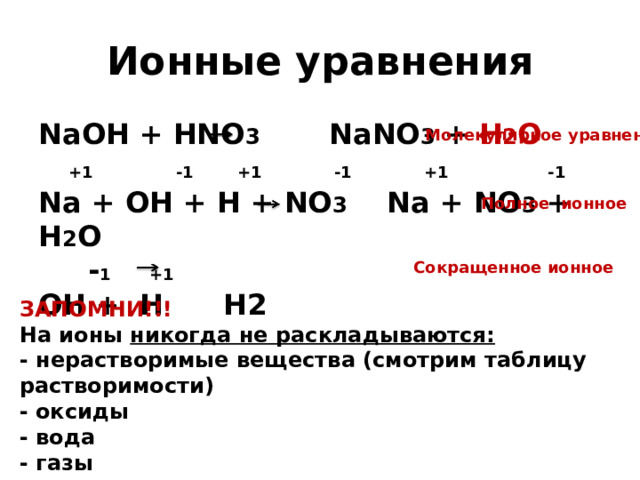
Ионные уравнения
NaOH + HNO 3 NaNO 3 + H 2 O
+1 -1 +1 -1 +1 -1
Na + OH + H + NO 3 Na + NO 3 + H 2 O
- 1 +1
OH + H H2
Молекулярное уравнение
Полное ионное
Сокращенное ионное
ЗАПОМНИ!!!
На ионы никогда не раскладываются:
- нерастворимые вещества (смотрим таблицу растворимости)
- оксиды
- вода
- газы

АЛГОРИТМ
1) Запишите молекулярное уравнение реакции.
2) Определите растворимость каждого вещества (таблица растворимости).
2KOH + H 2 SO 4 = K 2 SO 4 + 2H 2 O
2.А) Составьте полное ионное уравнение реакции (правила).
2.Б) Найдите одинаковые ионы и сократите их в правой и левой части уравнения.
+ - + 2- + 2-
2 K +2OH + 2H + SO 4 = 2K + SO 4 + 2H 2 O
3. Составить сокращенное ионное уравнение реакции
+ -
H + OH = H 2 O
ПРОВЕРЬ!!!
Сумма электрических зарядов ионов в левой части уравнения должна быть равна сумме электрических зарядов ионов в правой части.
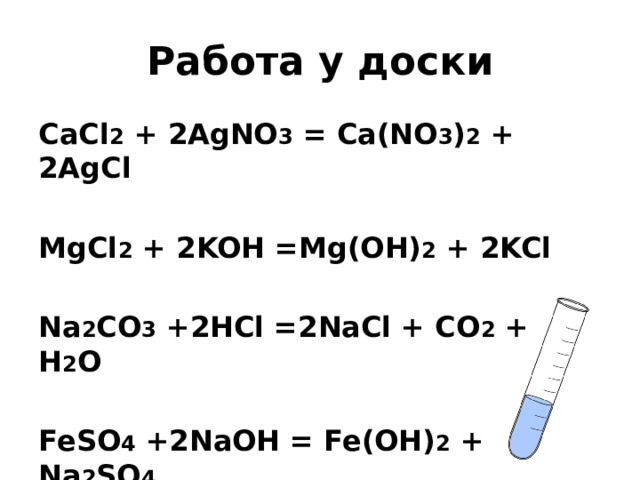
Работа у доски
CaCl 2 + 2AgNO 3 = Ca(NO 3 ) 2 + 2AgCl
MgCl 2 + 2KOH =Mg(OH) 2 + 2KCl
Na 2 CO 3 +2HCl =2NaCl + CO 2 + H 2 O
FeSO 4 +2NaOH = Fe(OH) 2 + Na 2 SO 4

Домашнее задание
1. Напишите уравнения реакций между растворами хлорида железа (III) и гидроксидом натрия в молекулярной и ионной формах. 2. Напишите уравнения реакций между растворами карбоната натрия и серной кислоты в молекулярной и ионной формах.

ИОНЫ,
ИОННЫЕ УРАВНЕНИЯ В ОГЭ

ОГЭ (12)
Установите соответствие
между реагирующими веществами и признаком протекающей между ними реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА ПРИЗНАК РЕАКЦИИ
А) 1)выпадение белого осадка
Б) 2) выпадение бурого осадка
В) 3)выпадение серо-зеленого осадка
4) выделение газа

ОГЭ (14)
Выберите два исходных вещества, взаимодействию которых соответствует сокращенное ионное уравнение реакции
1) СаО
2) Са
3) СаCl 2
4) K 2 SO 3
5) H 2 SO 3
6) SO 2
Запишите номера выбранных ответов.

ОГЭ (21)
Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для первого превращения составьте сокращенное ионное уравнение реакции.

































