Просмотр содержимого документа
«Кислоты (неорганическая химия)»
ТЕМА: Кислоты (§21)
Задание 1 Запишите в тетради определения:
Кислота-
Основность-
Нейтральная среда-
Кислотная среда-
Щелочная среда-
Задание 2 Перенесите схему в тетрадь и подпишите составные части кислоты, исходя из определения
Используя пример решения по расчёту степени оксиления химических элементов в кислоте (стр. 120), расчитайте степени окисления в следующих формулах кислот:
Вариант 1 1. H2СO3 Вариант 2 3. HNO2
2. H3РO4 4. H2SiO3
степень степень окисления окисления
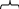
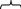

 H2 SO4
H2 SO4
часть часть
кислоты кислоты
Задание 3 Заполните схему в тетради, запишите название и химические формулы соответсвующих кислот.
Кислоты
Бескислородные


Кислородосодержащие



Одноосновные
Азотная -……
Азотистая- ….
Трёхосновные
Фосфорная-…
Двухосновные
Серная-….
Сернистая-….
Угольная-…..
Кремниевая-…
Одноосновные
Хлороводородная-…
Фтороводородная-…
Йодоводородная-…
Двухосновные
Сероводородная-…
Задание 4 Установите соответствие между названием кислоты и её свойствами
| 1 | H2SO4 | А | Кислота в свободном виде не существует, так как разлагается на оксид серы (IV) и воду. |
| 2 | H2СO3 | Б | Кислота очень быстро поглощает воду, обугливает части тел живой природы. |
| 3 | H2SO3 | В | Кислота в свободном виде не существует, так как разлагается на оксид углерода (IV) и воду. |
Задание 5 Дайте характеристику по плану
1)Химическая формула; 2) наличие кислорода; 3) основность; 4) растворимость в воде;
5) степени окисления элементов, образующих кислоту; 6) заряд иона, образуемый кислотным остатком;
7) соответствующий оксид.
Вариант 1 фосфорной кислоты Вариант 2 серной кислоты
Задание 6
Вариант 1
1) Даны формулы кислот: H2S, HCl, HNO3, H2SO4, H3РO4, H2СO3, H2SO3, H2СlO4. Распределите их по двум группам. Назовите по две кислоты в каждой группе.
2) Установите соответствие между кислотой и её оксидом
| 1 | H2SO4 | А | СO2 |
| 2 | H2СO3 | Б | Mn2O7 |
| 3 | H2SO3 | В | SO3 |
| 4 | HMnO4 | Г | SO2 |
Вариант 2
1) Даны формулы кислот: H2S, HCl, HNO3, H2SO4, H3РO4, H2СO3, H2SO3, H2СlO4. Распределите их по трём группам. Назовите по две кислоты в каждой группе.
2) Установите соответствие между кислотой и её оксидом
| 1 | HNO3 | А | SiO2 |
| 2 | H2SiO3 | Б | Р2O5 |
| 3 | HNO2 | В | N2O5 |
| 4 | H3РO4 | Г | N2O3 |
Задание 7 Решите задачу: Вычислите количество вещества в молях, соответствующее
Вариант 1 490 г серной кислоты
Вариант 2 9,8 г фосфорной кислоты.






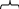
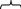

 H2 SO4
H2 SO4














