Тема «Вода. Растворы. Растворение»
Цель урока: Создать условия для высокого уровня воспроизведения системы знаний и умений студентов потеме «Вода. Растворы. Растворение».
Задачи:
Образовательные: ввести понятия растворов, гидратов, разобрать типы растворов, классификацию растворов, факторы, влияющие на растворение веществ; основные положения физической, химической и современной теории растворов.
Развивающие: развивать умения и навыки мыслительной деятельности (умения обобщать, сравнивать, анализировать), общеучебные умения и навыки (формирование самостоятельной и познавательной деятельности учащихся);
Воспитательные:воспитывать положительное отношение к учению, способствовать осознанию роли знаний в развитии личности, воспитании характера, преодолении трудностей.
Тип урока: учебное занятие по изучению нового материала.
Методы: частично-поисковые, практические, наглядные.
Форма проведения урока: коммуникативно-диалоговая.
Формы организации деятельности учащихся: индивидуальная, групповая, обще групповая.
Ход урока: урок начинается с демонстрации стакана с водой и показа лабораторного опыта- растворение поваренной соли в воде.
ТБ. Опыт 1: хлорид натрия, вода
Далее звучит вопрос группе: Как вы думаете, о чем сегодня пойдет речь на уроке?
(«Вода. Растворы. Растворение веществ в воде»). Слайд 2
Запись темы в тетради и демонстрация на слайдетемы «Вода. Растворы. Растворение».
Актуализация опорных ЗУН.
Вопрос группе: Какие сведения о воде и растворах были известны вам до сегодняшнего урока? (Слайд 3)
Знакомство студентов с задачами урока ( слайд 4)
На столах лежит раздаточный материал со словами Антуана де Сент-Экзюпери: (слайд 5)
Вода, у тебя нет ни вкуса, ни цвета, ни запаха,
Тебя невозможно описать, тобой наслаждаются не ведая, что ты такое.
Нельзя сказать, что ты необходима для жизни:
Ты – сама жизнь.
Вопрос группе: что означают эти слова?
«Значение воды для жизни человека» (сообщение студента)
Растворы играют важную роль в природе, науке и технике. Сложные физико-химические процессы, протекающие в организмах человека и животных, также протекают в растворах. Изучение свойств растворов занимает важное место в современной науке.
Давайте представим себя в роли сторонников этих теорий.
Работа по группам ( работа с текстом).
1 вариант – представители физической теории,
2 вариант – представители химической теории
Через 3 минутывы должны объяснить основную идею своей теории и назвать имена учёных, сторонников теории.
Обсуждение теорий сопровождается разбором схемы.(слайд 5)
Физическая теория: Химическая теория:
(Вант-Гофф, Оствальд, Аррениус). (Менделеев, Каблуков,
Кистяковский).
Растворение - это процесс диффузии, Растворение – это процесс
а растворы – это однородные смеси. химического взаимодействия
растворяемого вещества сводой-
процесс гидратации, а
растворы – это соединения –
гидраты.
Теперь вопрос- Как вы думаете, какая из этих теорий близка к современной теории о растворах?
Современная теория.
Растворение – это физико – химический процесс, а растворы – это однородная (гомогенная) система, состоящая из частиц растворённого вещества, растворителя и продуктов их взаимодействия – гидратов.
Гидраты – непрочные соединения веществ с водой, существующие в растворе. (слайд6 )
Студенты записывают определения в тетрадь со слайда
Растворимость веществ. Типы растворов.
От чего зависит растворение веществ?(слайд 8)
Вспоминаем со студентами инструктаж по ТБ. Далее идет демонстрация опытов: Опыт 2 -растворение разных веществ в воде.
1) от природы веществ. - хорошо растворимые;
- малорастворимые;
-практически нерастворимые (слайд9 )
Рассмотрите таблицу растворимости кислот, оснований и солей в воде, приведите примерырастворимых, малорастворимых и нерастворимых веществ (работа с таблицей растворимости).
Опыт 3: нагревание пробирки с раствором гидроксида кальция
2) от температуры
После демонстрации опытов студенты должны самостоятельно ответить на вопрос, поставленный ранее.
Классификация растворов:
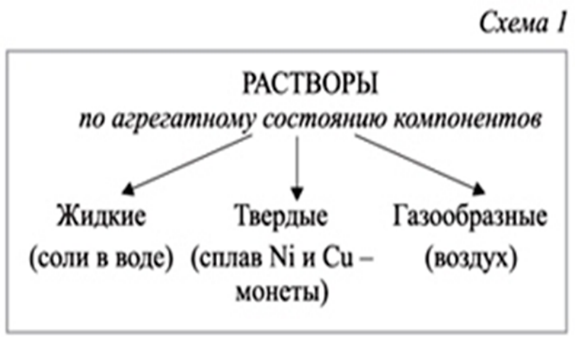
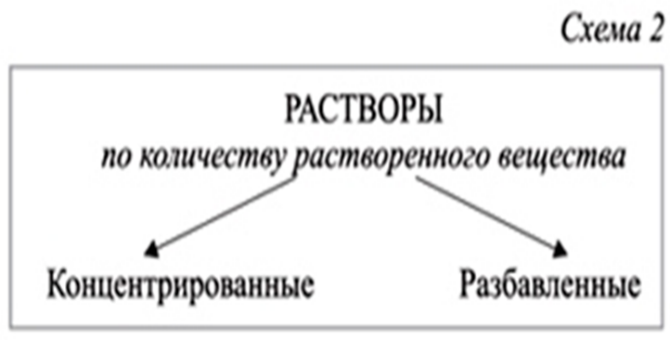
(Слайд 10)
На слайде показаны схемы классификации растворов. На примере опытов студентам ставится задача найти отличия между растворами.
Опыт 4: сульфат меди, химический стакан с водой.
Концентрированный раствор — раствор с высоким содержанием растворённого вещества.
Разбавленный раствор- раствор, содержащий малое количество растворённого вещества. (слайд 11). Работа с определениями.
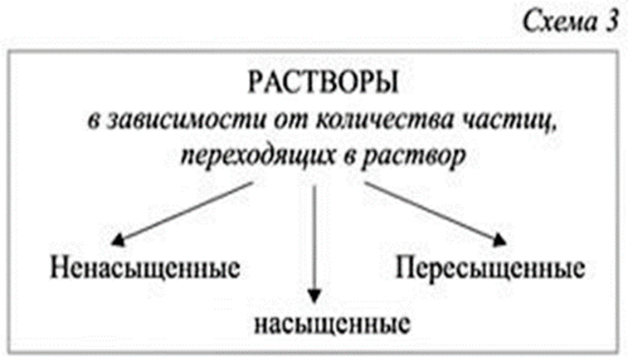 (слайд 10)
(слайд 10)
Студентам предлагается по изображению на презентации определить типы растворов.(слайд 12-13)
Демонстрация опыта 5 – растворение поваренной соли в воде, получение разных растворов по количеству частиц, переходящих в раствор. Студенты сами дают определения видам растворов.
Насыщенным называют такой раствор, в котором при данной температуре вещество больше не растворяется.
Ненасыщенным называют такой раствор, в котором при данной температуре находится меньше растворяемого вещества, чем в его насыщенном растворе.
Пересыщенным называют такой раствор, в котором при данной температуре находится в растворенном состоянии больше вещества, чем в его насыщенном растворе при тех же условиях. (слайд14)
Сегодняшний урок был посвящен теме «Вода.Растворы. Растворение», я предлагаю вам ответить на вопрос «Что нового вы узнали сегодня о воде, растворах?» (слайд 15)
(Закрепление изученного материала.)
Студентам предлагается ответить на вопросы:
1)Если вы были внимательны и уверены в себе, что все изученные вопросы усвоили, поставьте себе «5».
2) Если вы были внимательны, усвоили материал в целом, но на вопросы ответить можете, поставьте «4».
3) Кто сомневается, поставьте себе «3». (слайд 16)
Далее студенты выполняют упражнение «Данетка» по вариантам, затем студенты обмениваются листочками и оценивают своего соседа с помощью ответов продемонстрированных на слайде презентации.(слайд 17-18)
Рефлексия: (слайд 19)
Что вы считаете для себя главным на уроке?
Сегодня урок химии: легкий – трудный; интересный – скучный; полезный – ненужный?
Я ученик: старательный – ленивый; внимательный – невнимательный; урок усвоил – не усвоил.
Я запомнил....
узнал...
повторил...
удивился ...
Выводы по изученному материалу делают студенты в устной форме.
Домашнее задание п. 17 учебника, конспект по тетради. (слайд 20)









 (слайд 10)
(слайд 10)









