Просмотр содержимого документа
«Металлдардын касиети»

Металлдардын жалпы касиеттери.Коррозия.
Аткарган: Сүймөнкул Исматиллаев

Сабактын максаты:
- 1. Металлдардын физикалык жана химиялык касиеттерин үйрөнүү.

Металлдардын активдүүлүк катары

Физикалык касиеттери Кристаллдык торчо
Металлдык – бурчтарында оң заряддалган иондор, ал эми алардын арасында электрондор эркин кыймылдап жүрөт.
Эркин электрондордун көптүгү жогорку электр жана жылуулук өткөрүмдүүлүгүн, о.э. механикалык иштетүүгө жөндөмдүүлүгүн түшүндүрөт.

Агрегаттык абалы
- Баардык металлдар катуу абалда, бир өзгөчөлүк СЫМАП – жалгыз суюк абалдагы металл.

- Магниттешүү жөндөмдүүлүгү- темир, кобальт, никель. Магниттерди өндүрүүдө колдонулат
Ийкемдүүлүк
- Ар кандай буюмдарды жасоо.

Металлдык жаркыроо
- Жарык нурлары металлдын бетини тийип, металлдык жаркыроо эффектисин пайда кылуу менен, андан эркин электрондор менен түртүлөт. Күзгү түз беттүү айнектен жана ага капталган жука катмардуу металлдан турат. Көбүнчө күзгүлөрдү күмүш менен капташат, анткени ал жарыкты жакшы чагылдырат.

Электр өткөрүмдүүлүгү
- Жогорку электр өткөрүмдүүлүк металлдардын төмөну катары менен азайат:Аg Сu Аu Аl Мg Zn Fе РЬ Hg

Жылуулук өткөрүмдүүлүгү
- Жогорку жылуулук өткөрүмдүүлүк металлдардын төмөну катары менен азайат: Аg Сu Аu Аl Мg Zn Fе РЬ Hg

Баардык металлдар эки чоң топко бөлүнөт:
- Кара металлдар : кара-боз өңдүү, тыгыздыгы чоң, жогорку ээрүү температурасына жана катуулука ээ. Эң жөнөкөй өкүлү катары ТЕМИР каралат.

Түстүү металлдар:
- Мүнөздүү түскө ээ: кызыл, сары, ак; жогорку ийилчээктикти, төнмөнкү катуулукту көрсөтөт.
- Кадимки
түстүү металлдардын
өкүлү - ЖЕЗ

Тыгыздыгы
- Жеңил (тыгыздыгы 5 г/см 3 көп эмес) жеңил металлдарага: литий, натрий, калий, магний, кальций, цезий, алюминий, барий кирет. Эң жеңил металл — литий, тыгыздыгы 0.534 г/см 3 .

Тыгыздыгы
- Оор (тыгыздыгы 5 г/см 3 жогору).
Оор металлдарага: цинк , жез, темир, калай, коргошун, күмүш, алтын, сымап ж.б. Эң оор металл — осмий, тыгыздыгы 22,5 г/см 3 .

Ээрүү температурасы
- Жеңил ээрүүчү (ээрүү температурасы 1539°С-га чейин). Эң жеңил ээрүүчү металлдарга: сымап — ээрүү температурасы —37°С; галлий — ээрүү температурасы30°С;
- Оор ээрүүчү металдар (ээрүү температурасы 1539°С-дан жогору). Оор ээрүүчү металлдарга: хром — ээрүү температурасы 1890°С; молибден — ээрүү температурасы 2620°С; ванадий — ээрүү температурасы 1900°С; тантал — ээрүү температурасы 3015°С; ж.б. көптөгөн металлдар.
- Эң оор ээрүүчү металл вольфрам — ээрүү температурасы 3410°С.
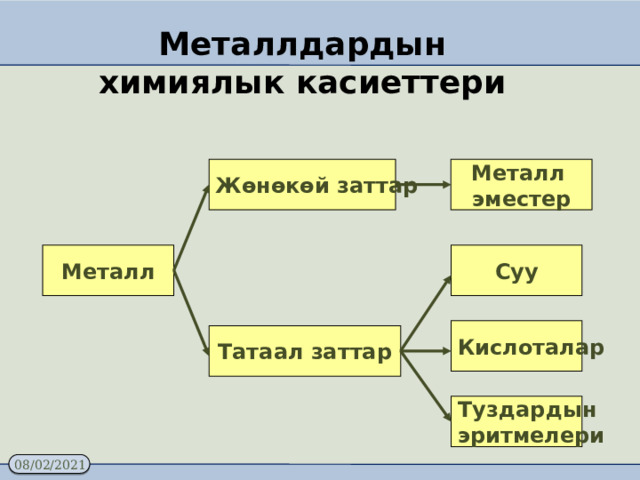
Металлдардын химиялык касиеттери
Жөнөкөй заттар
Металл
эместер
Металл
Суу
Кислоталар
Татаал заттар
Туздардын
эритмелери

Металл эместер менен реакциясы:
Cu + Cl 2 =CuCl 2
Fe + S =FeS
Кычкыл оксиддер менен реакциясы:
2Mg + CO 2 = 2MgO + C

Температуранын таасири менен жүргөн реакциялар:
4Na + O 2 = 2Na 2 O
2Mg + O 2 = 2MgO
Электр тогунун таасири менен жүргөн реакциялар:
4Ag + O 2 = 2Ag 2 O
4Au + O 2 =

Суу менен реакциясы:
2Na + 2H 2 O 2NaOH +H 2
2K + 2H 2 O = 2KOH + H 2
3Fe + 4H 2 O = Fe 3 O 4 + 4H 2
Cu + H 2 О = реакция жүрбөйт

Zn + 2HCl = ZnCl 2 + H 2
Fe + 2HCl = FeCl 2 + H 2
Cu + HCl = реакция жүрбөйт
Cu + 2H 2 SO 4конц. = CuSO 4 + SO 2 +2H 2 O
Cu + 4HNO 3 конц. = Cu(NO 3 ) 2 + 2NO 2 + 2H 2 O
Кислоталар менен реакциясы:

Сабактын жыйынтыгы(релаксация)
Фразаларды толуктагыла:





































