Анализ урока на тему: « Многоатомные спирты»
Поисковый подход в обучении – это обучение на основе исследовательской деятельности учащихся.
Использование исследовательского метода на данном уроке соответствует содержанию учебного материала.
Планируемые пути решения проблемной задачи соответствуют уровню развития учащихся и их индивидуальным возможностям.
Использование исследовательского метода на уроках требует определенного уровня исследовательских навыков, этого достигают учащиеся приученные самостоятельно добывать знания, когда это становится их потребностью.
Дидактическая цель урока:
1. познакомить учащихся с начальным этапом научного познания
2. повторение и закрепление ранее изученного материала
3. коррекция знаний
Педагогическая цель урока:
1. обучение исследовательской деятельности
Объем нашего исследования соответствует начальному этапу научного познания. В рамках методики научного исследования это урок - « Образец исследования»
На уроках исследования возможно использование разнообразных форм обучения учащихся: индивидуальная, парная, групповая, коллективная.
В структуре урока я выделила несколько этапов:
1. Актуализация знаний (в современном мире, где имеется огромное количество продуктов потребления, современный человек должен об этом знать)
2. Мотивация
3. Создание проблемной ситуации
4. Определение темы исследования
5.Выдвижение гипотезы (имеются ли многоатомные спирты в данных продуктах)
6. Проверка гипотезы (проведение эксперимента)
7. Интерпретация полученных данных (анализ данных исследования показывает, что во всех исследуемых продуктах присутствуют многоатомные спирты).
8. Выводы
9. Подведение итогов урока
10. Домашнее задание
Урок на тему: « Многоатомные спирты»
Цель урока – закрепить, обобщить понятие о многоатомных спиртах, развить понятия о взаимном влиянии атомов в молекулах, зависимости применения от свойств веществ; провести исследование- обнаружение многоатомных спиртов в жевательной резинке, Пепси-Коле, пчелином мёде.
Задачи:
обучающие – формирование представлений о многоатомных спиртах (отличие их от одноатомных), ознакомление с физическими и химическими свойствами многоатомных спиртов, их распознаванием и применением;
развивающие–способствовать формированию познавательной активности учащихся на уроке, с использованием мультимедийных презентаций, демонстрационных, исследовательских опытов;
воспитывающие – создать условия для развития способности использования знаний для принятия обоснованного решения.
Тип урока: урок- исследование, отработка учебных приемов, составляющих исследовательскую деятельность.
Методы обучения:
организация и осуществление учебно-познавательной деятельности:
перцептивныеметоды – словесные (лекция учителя), наглядные (презентация), практические (демонстрация опытов);
логические методы – аналитические;
гностические методы – исследовательские (исследование состава жевательных резинок, напитка Пепси-Колы, пчелиного мёда)
управление учением – работа под руководством учителя; самостоятельная работа обучающихся: с книгой, письменная работа в тетрадях;
стимулирование и мотивация учения:
стимулирование интереса к учению - учебная дискуссия, занимательность;
стимулирования долга и ответственности к учению - убеждение в значимости учения, поощрение в учении;
контроль и самоконтроль в обучении:
устный контроль – индивидуальный, групповой
письменный контроль - тестирование
экспериментальный - проведение опытов
Форма проведения урока: исследование в группе, мультимедиа - урок
Дидактические средства:
учебник под редакцией О.С.Габриеляна «Химия 10 класс»;
компьютер;
проектор;
презентация «Многоатомные спирты» (Приложение );
реактивы для демонстрации опытов учителю: глицерин, этиленгликоль, растворы гидроксида калия, сульфата меди (II), вода дистиллированная, химические стаканы, штатив, спиртовка;
реактивы для проведения исследования учащимися: жевательные резинки, напиток Пепси-Кола, раствор мёда, растворы гидроксида калия, сульфата меди (II), вода дистиллированная, химические стаканы;
демонстрационный материал:
образцы косметических средств: мыло, крем для рук, помада, гель для душа, крем для лица, краска для волос, зубные пасты;
образцы жевательных резинок (различные).
Различные газированные напитки
Мёд натуральный и искусственный
Методическая литература: Габриелян О.С. Химия.10 класс: Настольная книга учителя /О.С.Габриелян. И.Г.Остроумов/. - М.: Дрофа, 2004.-480с.
План урока:
1. Организационный момент.
На рабочих столах учащихся подготовлены:
Методички, с темами и планом исследования для трёх групп
Ящики с реактивами: жевательные резинки, раствор мёда, напитки Пепси, Фанта, Кола, растворы гидроксида калия, сульфата меди (II), вода дистиллированная, два химических стакана.
Образцы косметических средств в корзинке: мыло, крем для рук, зубная паста, гель для душа, помада
Раздаточный материал по строению и физическим свойствам многоатомных спиртов
Листы для итогового отчёта исследовательской группы, рефлексии, оценки качества знаний (приложение№1,2,3)
1.1 Вступительное слово учителя.
1.2 Подготовка к проведению химического исследования «Обнаружение многоатомных спиртов в продуктах питания»
1.3 Повторение классификации, изомерии, химических свойств одноатомных спиртов:
1. Тестовый контроль (три варианта заданий)– отметка «4» (Приложение 1);
2. Работа с дидактическими карточками - составление уравнений реакций одноатомных спиртов – отметка «5» (Приложение 2);
3. Составление самими учащимися заданий для контроля –«5» (Приложение 3).
2. Обобщение и систематизация знаний по теме: «Многоатомные спирты»
1. Строение, физические свойства и применение многоатомных спиртов.
2. Демонстрация растворимости глицерина.
3. Демонстрация качественной реакции многоатомных спиртов.
4. Исследование содержания многоатомных спиртов в жевательной резинке, Пепси – Коле и натуральном мёде.
3. Подведение итогов урока. Вывод.
4. Домашнее задание.
Ход урока
1. Организационный момент.
Мотивация к изучению темы урока.
Здравствуйте уважаемые коллеги и учащиеся. Я рада вас видеть на нашем уроке химии и хочу поделиться с вами своими наблюдениями. Недавно в аптеке я приобрела препарат для больного ребенка « Panadol Babu» не содержащий спирта (об этом свидетельствует надпись на упаковке), но с точки зрения химика кроме парацетамола и других компонентов в лекарстве присутствует органическое вещество глицерин.
Вопрос: К какому классу химических веществ относится это вещество?
Ответ: Кислородсодержащие органические соединения. Класс – многоатомные спирты.
Вопрос: Знаете ли вы какие продукты питания, лекарства где находятся вещества подобные глицерину и также относящиеся к данному классу веществ?
Ответ: Газированные напитки (Кола, Фанта, Пепси), кондитерские продукты для больных сахарным диабетом,
Давайте, почитаем, этикетки на упаковках изделий, которых я просила вас принести на этот урок: крема, мыла, кондитерские изделия, зубные пасты, жевательные резинки (Слайд №8,9 ). Очень часто встречаются названия:
Ответ: глицерин, пропиленгликоль, сорбит, ксилит, манит, глюкоза - это и есть многоатомные спирты.
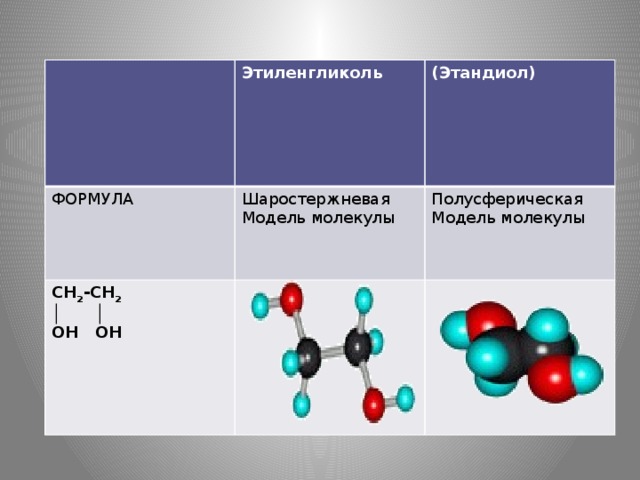
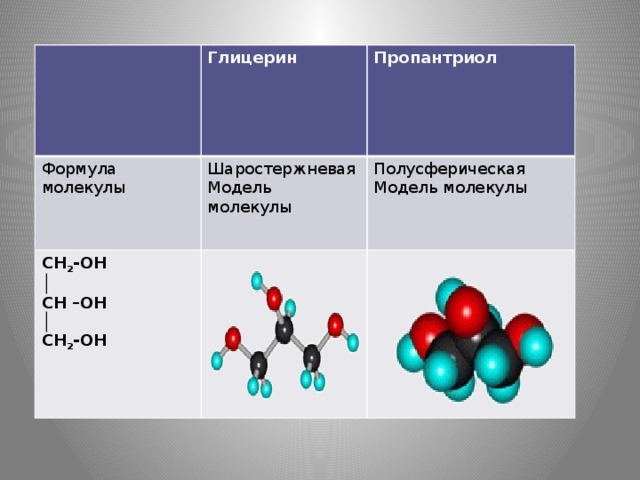
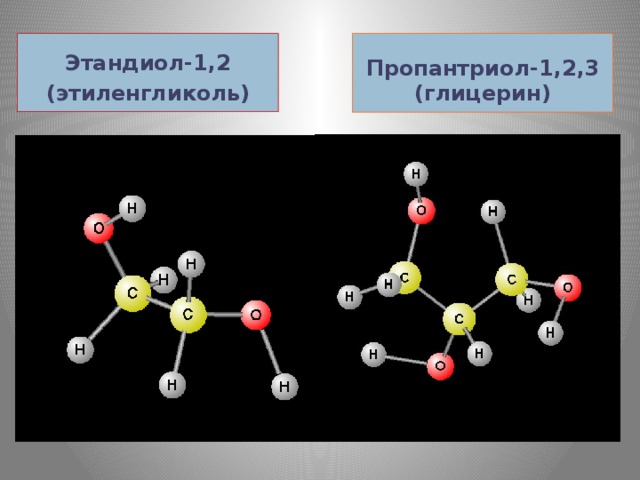
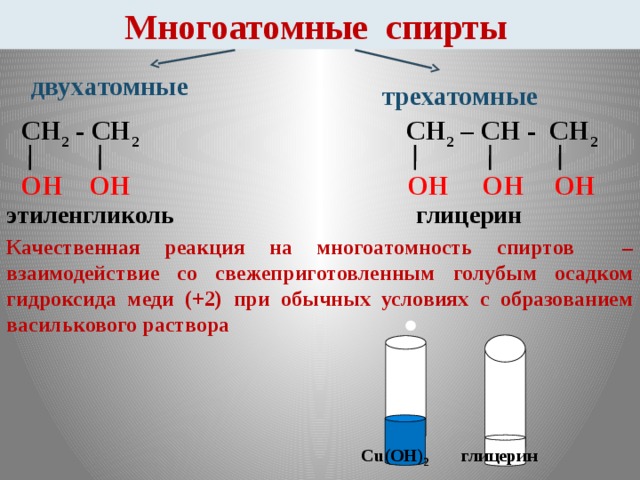
Вопрос: Вспомним, какое строение имеют многоатомные спирты, что у них общего в строении? (Слайд № 2,3,10) формулы веществ: глицерина, этиленгликоля.)
Ответ: Наличие гидроксильных групп
В Пепси содержится двухатомный спирт – бутандиол (двухатомный спирт)
Антифриз (незамерзающая жидкость) – этандиол или этиленгликоль (двухатомный спирт)
Конфеты, печенье для диабетиков - сорбит, ксилит (шестиатомный спирт)
Кондитерские изделия, мёд – глюкоза (пятиатомный спирт)
Мороженое – сахароза
Крем для смягчения кожи – глицерин (трёхатомный спирт)
Задача, которая сегодня стоит перед вами это- обнаружение многоатомных спиртов в составе трёх продуктов:
1. Газированный напиток Пепси-Кола
2. Жевательная резинка (конфета)
3. Натуральный пчелиный мёд
Также можно взять:
Лекарственный препарат - панадол, незамерзающую жидкость, продукты питания для больных сахарным диабетом.
Чтобы решить такую задачу вам нужно:
1. Вспомнить качественную реакцию на многоатомные спирты (Слайд №12 )
2. Почему глицерин, этиленгликоль, глюкоза хорошо растворяются в воде?
Класс делится на три исследовательских группы:
Группа№1 – Обнаружение многоатомных спиртов в натуральном мёде
Группа№2– Обнаружение многоатомных спиртов в газированном напитке «Пепси-Кола»
Группа№3 – Обнаружение многоатомных спиртов жевательной резинке « Орбит»
Проведём подготовительную часть эксперимента.
Группа№1 – в химический стакан положите чайную ложку мёда и прилейте небольшое количество дистиллированной воды.
Группа№2 – в химический стакан налейте газированный напиток и прилейте небольшое количество дистиллированной воды.
Группа№3 – в химический стакан положите измельченную жевательную резинку и прилейте небольшое количество дистиллированной воды. Настаивать 10-15 минут.
2. Обобщение и систематизация знаний по теме:
«Многоатомные спирты»
Повторение классификации, изомерии, химических свойств одноатомных спиртов.
проходит в группах по трём заданиям:
1. Тестовый контроль (три варианта заданий)– отметка «4» (Приложение №4);
2. Работа с дидактическими карточками - составление уравнений реакций одноатомных спиртов – отметка «5» (Приложение №5);
3. Составление самими учащимися заданий для контроля –«5» (Приложение №6).
Повторение строения и физических свойств многоатомных спиртов
повторение строения и свойств некоторых представителей многоатомных спиртов в целях экономии времени урока распечатывают каждому обучающемуся, и они их прикрепляют в свои тетради. (Слайд № 2,3,4) (распечатать каждому ученику класса)
Демонстрация растворимости глицерина.
Демонстрационный опыт: вода + глицерин → перемешать.
Вывод: хорошо растворим в воде.
Вопрос:
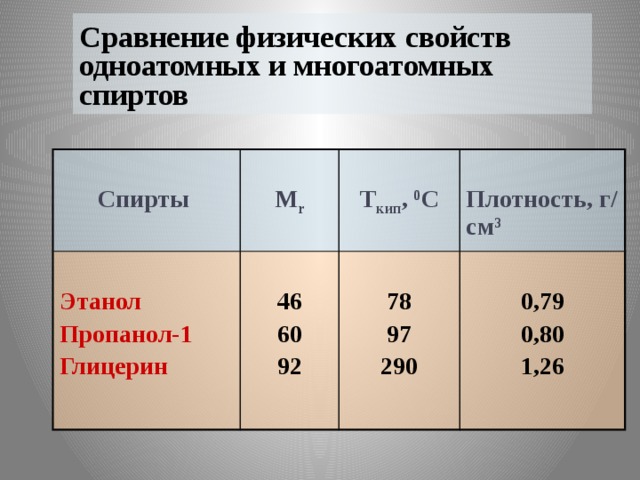
Сравните физические свойства одноатомных и многоатомных спиртов. Объясните причину такого различия (причина – число гидроксильных групп). (Слайд №5,6,7.)
Ответ:
В молекуле глицерина имеются 3 гидроксогруппы, значит число атомов водорода, способных к образованию водородной связи в 3 раза больше, чем в молекулах одноатомных спиртов. Поэтому, сила межмолекулярной связи в случае глицерина гораздо больше, чем в молекулах одноатомных спиртов. В случае глицерина необходимо более сильное нагревание, более высокая температура, для того чтобы ослабить связи между молекулами до такой степени, чтобы они перешли в газообразное состояние. По этой причине многоатомные спирты более вязкие и температуры кипения их выше, чем у соответствующих одноатомных спиртов.
Вывод: число гидроксогрупп обуславливает физические свойства (за счет водородных связей).
Демонстрация качественной реакции многоатомных спиртов.
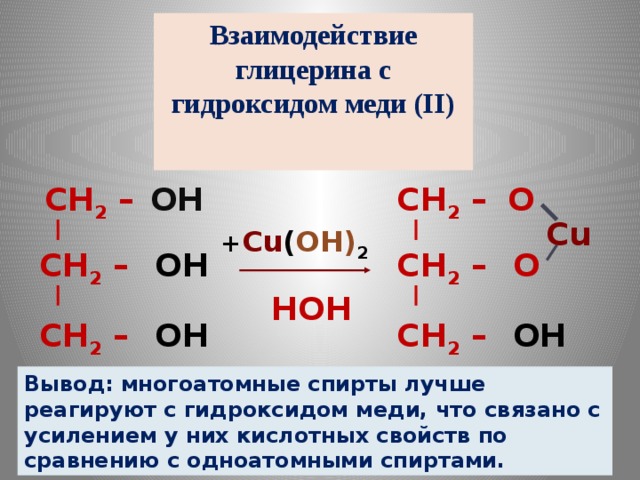
Ответ на него учащиеся получают при демонстрации опыта – действия глицерина на гидроксид меди (II). Отмечается, что многоатомные спирты в отличие от одноатомных спиртов реагируют с нерастворимым основанием и легче окисляются. Взаимодействие глицерина с основанием говорит о том, что многоатомные спирты обладают слабыми кислотными свойствами.
Записываем уравнение реакции глицерина с гидроксидом меди (II) (Слайд № 10,11,12).

Учитель:
Итак, мы рассмотрели отличительные свойства многоатомных спиртов. Вернёмся к вопросу исследования содержания многоатомных спиртов в жевательных резинках, мёде и газированных напитках.
Тема исследования, план исследования и вопросы для каждой группы находятся на столах. (Приложение №1,2,3) Вам нужно оформить итоговый отчёт и ответить на 5 вопросов. (Приложение №7) Не забудьте поставить своей группе оценку в бланке « рефлексия» (Приложение №8) Приступайте к работе. Удачи вам!
3. Подведение итогов урока. Вывод (Слайд№15 )
Во всех многоатомных спиртах гидроксильные группы находятся при разных атомах углерода;
Число гидроксогрупп влияют на физические свойства спирта (за счет водородных связей);
Общие свойства с одноатомными спиртами обусловлено наличием функциональной группой ОН;
На примере многоатомных спиртов ещё раз убеждаемся в том, что количественные изменения переходят в изменения качественные: накопление гидроксильных групп в молекуле обусловило в результате их взаимного влияния появление у спиртов новых свойств по сравнению с одноатомными спиртами – взаимодействие с нерастворимыми основаниями.
4. Домашнее задание:
§ 16, ученика «Химия 10 класс» под редакцией О.С.Габриеляна.
Творческое задание:
составить кроссворд;
написать реферат о применении сорбита и ксилита в пищевой прмышленности;
написать реферат об Альфреде Нобеле;
составить презентацию о применении нитроглицерина.
Приложение№1
Группа№1
Тема исследования:
«Обнаружение многоатомных спиртов в натуральном мёде»
Опыт№1. В химический стакан поместить 1 чайную ложку натурального мёда и прилить немного дистиллированной воды. Размешать стеклянной палочкой и дать настояться в течение 3-5 минут.
Опыт№2. В химический стакан налить 1 мл. раствора сульфата меди, к нему добавить 2 мл. раствора гидроксида калия.
Объясните, что вы наблюдаете?
Напишите уравнение реакции, которая протекает.
К полученному осадку прилейте раствор натурального мёда.
Объясните, что вы наблюдаете?
Напишите уравнение реакции, которая протекает.
Ответьте на вопросы:
1.Какое вещество входит в состав натурального мёда? Напишите его формулу.
2. Почему происходит растворение осадка?
3. Какое вещество образуется в результате реакции? Напишите его формулу и дайте название.
4.Какими свойствами обладает многоатомный спирт, входящий в состав мёда?
5. Сравните результаты своих анализов с результатами других групп учащихся.
6. Какое физиологическое действие оказывает этот многоатомный спирт на живой организм?
7. Сформулируйте выводы о строении и свойствах многоатомных спиртов.
Приложение№2
Группа№2
Тема исследования:
«Обнаружение многоатомных спиртов в газированном напитке Пепси»
Опыт№1. В химический стакан поместить 2 мл. газированного напитка «Пепси» и прилить немного раствора карбоната натрия. Объясните, что вы наблюдаете? Напишите уравнение реакции, которая протекает.
Опыт№2. В химический стакан налить 1 мл. раствора сульфата меди, к нему добавить 2 мл. раствора гидроксида калия.
Объясните, что вы наблюдаете?
Напишите уравнение реакции, которая протекает.
К полученному осадку прилейте раствор напитка «Пепси»
Объясните, что вы наблюдаете?
Напишите уравнение реакции, которая протекает.
Ответьте на вопросы:
1.Какое вещество входит в состав напитка «Пепси»? Напишите его формулу.
2. Почему происходит растворение осадка?
3. Какое вещество образуется в результате реакции? Напишите его формулу и дайте название.
4.Какими свойствами обладает многоатомный спирт, входящий в состав газированного напитка?
5. Сравните результаты своих анализов с результатами других групп учащихся.
6. Какое физиологическое действие оказывает этот многоатомный спирт на живой организм?
7. Сформулируйте выводы о строении и свойствах многоатомных спиртов.
Приложение№3
Группа№3
Тема исследования:
«Обнаружение многоатомных спиртов в жевательной резинке»
Опыт№1. В химический стакан поместить 1пластинку жевательной резинки и прилить немного дистиллированной воды. Размешать стеклянной палочкой и дать настояться в течение 15 минут.
Опыт№2. В химический стакан налить 1 мл. раствора сульфата меди, к нему добавить 2 мл. раствора гидроксида калия.
Объясните, что вы наблюдаете?
Напишите уравнение реакции, которая протекает.
К полученному осадку прилейте раствор где находится жевательная резинка, хорошо размешайте.
Объясните, что вы наблюдаете? В какой цвет окрашивается жидкость?
Напишите уравнение реакции, которая протекает.
Ответьте на вопросы:
1.Какое вещество входит в состав жевательной резинки? Напишите его формулу.
2. Почему происходит растворение осадка?
3. Какое вещество образуется в результате реакции? Напишите его формулу и дайте название.
4.Какими свойствами обладает многоатомный спирт, входящий в состав жевательной резинки?
5. Сравните результаты своих анализов с результатами других групп учащихся.
6. Какое физиологическое действие оказывает этот многоатомный спирт на живой организм?7. Сформулируйте выводы о строении и свойствах многоатомных спиртов.
Приложение№4
Оценка качества знаний
Выполнение тестового задания по группам:
1 группа – этиленгликоль;
2 группа – глицерин;
3 группа – глюкоза.
Тест по выбору ответов
1. Многоатомный спирт
2. Реакция этерификации
3. Одноатомный спирт
4. Реакция с солями тяжёлых металлов
5.Общая формула класса данного соединения
6.Входит в состав жиров
7.Сильнейший яд
8. Пятиатомный спирт
9. Антифриз
10. Находится в крови
11. Сладкое на вкус
12. Хорошо растворимо в воде
13.Исползуют как лекарство
14. Применяют в производстве и лекарства и взрывчатого вещества
15. Применяют в производстве синтетического волокна
Приложение №5
Дидактические карточки на тему:
«Химические свойства одноатомных спиртов»
Карточка для группы №1
1. Являются ли этиленгликоль и глицерин членами одного гомологического ряда? Почему? Напишите по два гомолога глицерину и этиленгликолю.
2. Назовите написанные спирты по заместительной номенклатуре. Как формируется их название?
3. Напишите уравнения реакций многоатомных спиртов с натрием и хлороводородом (общие свойства с одноатомными спиртами).
Карточка для группы №2
1. Составить реакции глицерина с азотной и уксусной кислотами, а также реакцию гидролиза сложного эфира уксусной кислоты.
2. Какие продукты получаются при внутримолекулярной дегидратации многоатомных спиртов?
3. Как отличить многоатомные спирты от одноатомных? Расскажите о качественной реакции на многоатомные спирты.
Карточка для группы №3
1. Составьте уравнения реакций получения этиленгликоля по схеме записанной ранее в тетради.
2. Из каких веществ можно получить глицерин? Составьте уравнение по схеме, представленной на диске.
3. Расскажите о применении многоатомных спиртов в промышленности, быту,медицине.
Приложение №6
Составление самими учащимися заданий для контроля
1.Дайте определение спиртам. Что такое функциональная группа?
2.Как классифицируют спирты по числу функциональных групп, по характеру углеводородного скелета, по характеру углерода, с которым связана гидроксильная группа?
3. Имеют ли спирты запах, цвет? Какое у них агрегатное состояние?
4. Почему первые представители спиртов - жидкости, а соответствующие им углеводороды - газы?
5. Какие виды изомерии характерны для спиртов?
6. Перечислите типы реакций, которые характерны для одноатомных спиртов.
7. Как можно получить спирты?
8. Какой спирт обладает большей растворимостью в воде: бутиловый или октиловый?
9.Дано вещество:
СН3
|
СН3— СН2 — С—СН2—ОН
|
СН3
Напишите формулы двух гомологов и двух изомеров, назовите их.
10. Дано вещество:
СН3— СН2 — СН— СН —СН3
| |
ОН СН3
Напишите формулы двух гомологов и двух изомеров, назовите их.
Приложение №7
Итоговый отчёт исследовательской группы
| Опыт № | Что делали? | Что наблюдали? | Уравнение химической реакции |
| №1 |
|
|
|
| №2 |
|
|
|
Вопросы группе:
1. Почему происходит растворение осадка гидроксида меди(11)
2. Какое вещество образуется в результате реакции в опыте №2?
3.Какими свойствами обладает вещество (глицерин, глюкоза, сорбит)?
4. Напишите структурную формулу глицерина, этиленгликоля, дайте им названия по Женевской систематической номенклатуре.
Приложение №8
Рефлексия
| №/п | Этапы исследования | Собственная оценка | Оценка учителя |
| 1. | Проведение эксперимента |
|
|
| 2. | Правильность написания уравнения химической реакции |
|
|
| 3. | Ответы на вопросы |
|
|
| 4. | Выводы |
|
|
Приложение №9
Выводы
Во всех многоатомных спиртах гидроксильные группы находятся при разных атомах углерода;
Число гидроксогрупп влияют на физические свойства спирта (за счет водородных связей);
Общие свойства с одноатомными спиртами обусловлено наличием функциональной группой ОН;
На примере многоатомных спиртов ещё раз убеждаемся в том, что количественные изменения переходят в изменения качественные: накопление гидроксильных групп в молекуле обусловило в результате их взаимного влияния появление у спиртов новых свойств по сравнению с одноатомными спиртами – взаимодействие с нерастворимыми основаниями.
Увеличение числа гидроксильных групп усиливает кислотные свойства многоатомных спиртов.