
Министерство здравоохранения Свердловской области
Краснотурьинский филиал
Государственного бюджетного профессионального образовательного учреждения
«Свердловский областной медицинский колледж»
ЛЕКЦИЯ 9. НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ. АЛКИНЫ
Жукова Алена Викторовна,
преподаватель высшей квалификационной категории
ОД.12 Химия
Краснотурьинск
2025
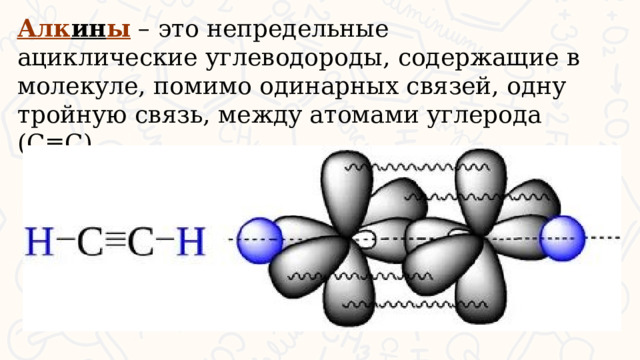
Алк ин ы – это непредельные ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, одну тройную связь, между атомами углерода (С≡С)
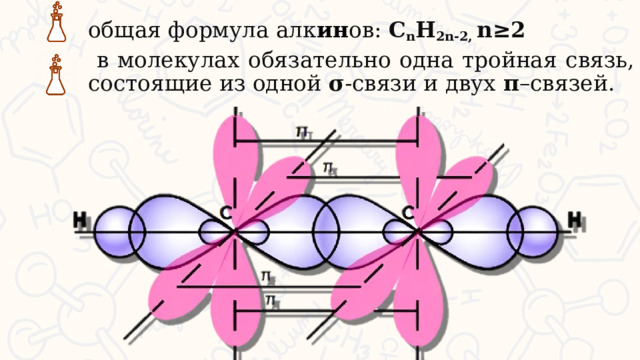
общая формула алк ин ов: C n H 2n-2, n≥2
в молекулах обязательно одна тройная связь, состоящие из одной σ -связи и двух π –связей.
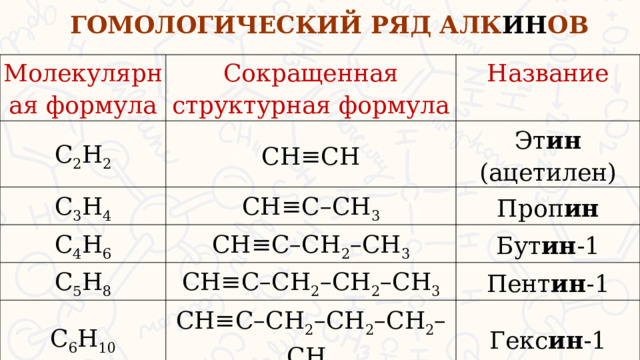
ГОМОЛОГИЧЕСКИЙ РЯД АЛК ИН ОВ
Молекулярная формула
Сокращенная структурная формула
C 2 H 2
C 3 H 4
Название
CH≡CH
C 4 H 6
CH≡C–CH 3
Эт ин (ацетилен)
Проп ин
CH≡C–CH 2 –CH 3
C 5 H 8
Бут ин -1
CH≡C–CH 2 –CH 2 –CH 3
C 6 H 10
Пент ин -1
CH≡C–CH 2 –CH 2 –CH 2 –CH 3
Гекс ин -1

НОМЕНКЛАТУРА АЛК ИН ОВ
Выбор главной цепи
Цепь должна содержать одну тройную связь (С ≡ С)
Нумерация главной цепи
Нумерация начинается с того конца, к которому ближе находится тройная связь
Формирование названия
С учетом всех заместителей и их местоположения
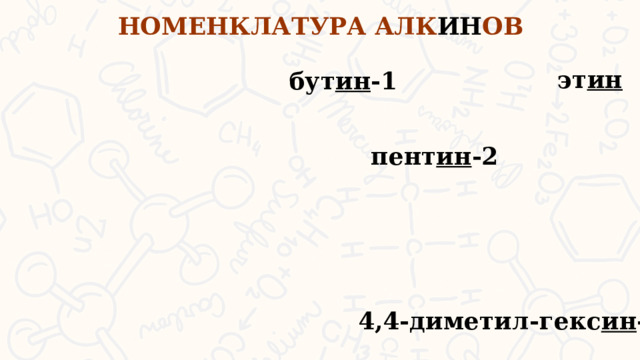
НОМЕНКЛАТУРА АЛК ИН ОВ
эт ин
бут ин -1
пент ин -2
4,4-диметил-гекс ин -2

ИЗОМЕРИЯ АЛКИНОВ
Изомерия углеродной цепи
гексин-1
3-метил-пентин-1
3,3-диметил-бутин-1

ИЗОМЕРИЯ АЛКИНОВ
Изомерия положения кратных связей
гексин-1
гексин-2
гексин-3

ИЗОМЕРИЯ АЛКИНОВ
Межклассовая изомерия с алкадиенами ( имеют одинаковую общую формулу C n H 2n-2 )
C 4 H 6
бутадиен-1,3
бутин-1
бутин-2

ФИЗИЧЕСКИЕ СВОЙСТВА АЛКИНОВ
С 2 – С 4 – газы
С 5 – С 16 – жидкости
С 17 – С … – твердые вещества
Растворимость в воде незначительна, немного выше, чем у алканов и алкенов
Хорошо растворимы в неполярных органических растворителях
t кип и t пл алкинов выше, чем у алканов

ХИМИЧЕСКИЕ СВОЙСТВА АЛКИНОВ
Реакции присоединения
Гидрирование
этен
этин
этен
этан
Рассмотрим 1 тип реакции присоединения к алкинам, это реакция гидрирования , т.е. присоединения молекулы водорода
На 1 ступени образуются алкены, на второй ступени - алканы
Суммарное уравнение
этин
этан

ХИМИЧЕСКИЕ СВОЙСТВА АЛКИНОВ
Реакции присоединения
Галогенирование
бутин-1
1,2-дибромбутен-1
Следующий тип реакции присоединения – реакция галогенирования, т.е. присоединения галогенов (хлор, фтор, бром, йод).
На 1 ступени реакции образуются дигалогеналкены, на 2 ступени – тетрагалогеналканы.
Алкинов с бромной водой качественной реакцией на алкины, бромная вода обесцвечивается.
1,2-дибромбутен-1
1,1,2,2-тетрабромбутан
ХИМИЧЕСКИЕ СВОЙСТВА АЛКИНОВ
Реакции присоединения
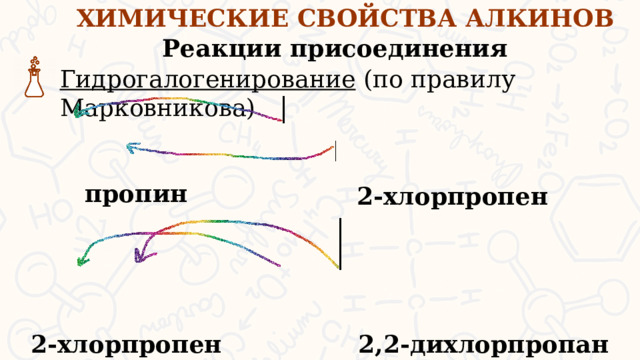
Гидрогалогенирование (по правилу Марковникова)
пропин
2-хлорпропен
Гидрогалогенирование – реакция присоединения галогенводородов. В данной реакция проходит по правилу Марковникова. На 1 ступени образуются моногалогеналкены на 2 ступени дигалогеналканы.
2-хлорпропен
2,2-дихлорпропан

ХИМИЧЕСКИЕ СВОЙСТВА АЛКИНОВ
Реакции присоединения
Гидратация (по правилу Марковникова)
Реакция гидратации или реакция присоединения воды происходит по правилу Марковникова. Ацетилен образует альдегид, а его гомологи образуют кетоны. Это так называемая реакция кучерова.
значит, берем ацетилен присоединяем к нему молекулу воды и получается виниловый спирт, но это неустойчивое соединение, и он быстро изомеризуется в этаналь или уксусный альдегид.
этаналь
(ацетальдегид,
уксусный альдегид )
этин
виниловый спирт
(неустойчивый )

ХИМИЧЕСКИЕ СВОЙСТВА АЛКИНОВ
Реакции окисления
Горение
Неполное окисление под действием KMnO 4 или K 2 Cr 2 O 7
Рассмотрим реакции окисления алкинов.
- Горение – т.е. полное окисление. В результате этой реакции образуются углекислый газ и вода
- Не полное окисление (под действием окислителей типа перманганата калия или дихромата калия)
при действии сильных окислителей алкины окисляются с разрывом тройной связи (кроме ацетилена). Конечным продуктом реакции являются карбоновые кислоты.
Например, при окислении бутина -2 образуется этановая или уксусная кислота.
Реакция с перманганатом калия является качественной реакцией на алкины. Раствор перманганата калия обесцвечивается
этановая (уксусная) кислота
бутин

ХИМИЧЕСКИЕ СВОЙСТВА АЛКИНОВ
Реакции полимеризации
Линейная полимеризация ацетилена
винилацетилен (димер)
Алкины могут образовывать линейные димеры, тримеры и полимеры, а также циклические тримеры.
Линейная полимеризация ацетилена происходит в присутствии солей меди.
дивинилацетилен (тример)

ХИМИЧЕСКИЕ СВОЙСТВА АЛКИНОВ
Реакции полимеризации
Циклотримеризация
бензол
Циклотримеризация алкинов приводит к образованию бензола и других ароматических углеводородов.
1,3,5-триметилбензол

ХИМИЧЕСКИЕ СВОЙСТВА АЛКИНОВ
Реакция с металлическим натрием
Ацетиленид натрия
Атомы водорода связаны со sp гибридизованными атомами углерода в молекулах алкинов обладают значительной подвижностью, что объясняется поляризацией связи ---С-Н. В связи с этим данные атомы водорода могут замещаться атомами металлов, в результате чего образуются ацетилениды. Способность к таким реакциям отличает алкины от других непредельных углеводородов.

ПОЛУЧЕНИЕ АЛК ИН ОВ
Дегидрирование УВ нефти
Гидролиз карбида кальция
Дегидрогалогенирование дигалогеналканов
CaC 2 + 2H 2 O Ca(OH) 2 + C 2 H 2
2,3-дибромпентан
пентин-2
ПРИМЕНЕНИЕ АЛК ИН ОВ
ацетилен
резка и сварка металлов
производство резины
органический синтез разнообразных веществ

ДОМАШНЕЕ ЗАДАНИЕ
- Учить конспект
- Ответить на следующие вопросы:
- назовите определение «Алкинов» и общую формулу для алкинов
- назовите физические свойства алкинов
- какие типы изомерии характерны для алкинов?
- как получают алкины?

Министерство здравоохранения Свердловской области
Краснотурьинский филиал
Государственного бюджетного профессионального образовательного учреждения
«Свердловский областной медицинский колледж»
ЛЕКЦИЯ 9. НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ. АЛКИНЫ
Жукова Алена Викторовна,
преподаватель высшей квалификационной категории
ОД.12 Химия
Краснотурьинск
2025







































