Просмотр содержимого документа
«Оксиды, классификация и химические свойства»

Барбашина Любовь Викторовна
Воронежский Государственный профессионально-педагогический колледж

ЦЕЛИ:
обобщить знания учащихся о составе оксидов, изучить их классификацию, свойства основных и кислотных оксидов.

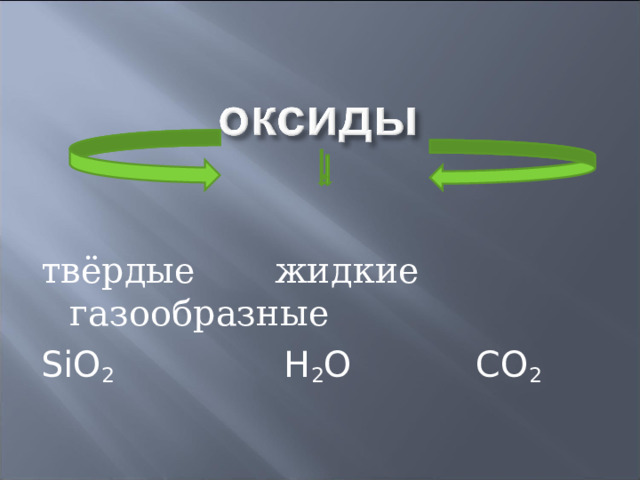
твёрдые жидкие газообразные
SiO 2 H 2 O CO 2



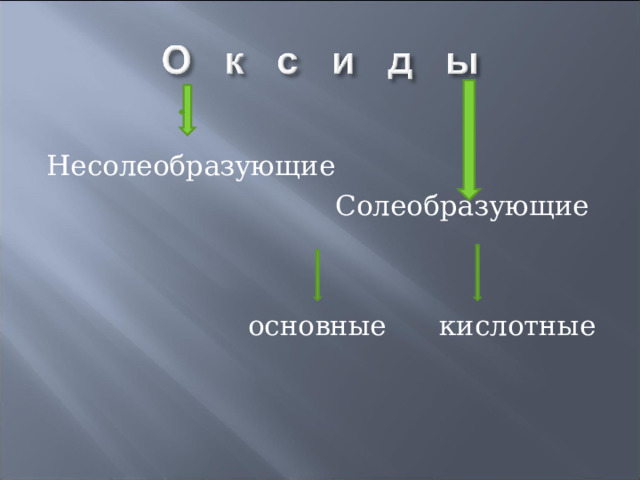
Несолеобразующие
Солеобразующие
основные кислотные



K 2 O – KOH
BaO- Ba(OH) 2
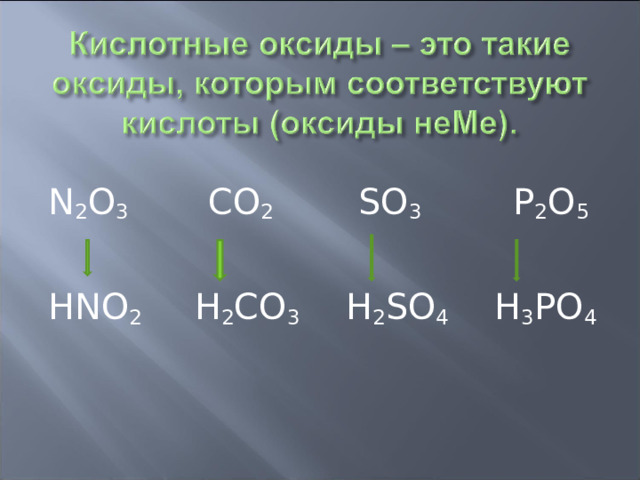
N 2 O 3 CO 2 SO 3 P 2 O 5
HNO 2 H 2 CO 3 H 2 SO 4 H 3 PO 4

Основный оксид + кислота→соль + вода
( реакция обмена)
CuO + H 2 SO 4 →CuSO 4 + H 2 O
K 2 O +2HCl→2KCl + H 2 O
Основный оксид + вода→щёлочь
(реакция соединения)
K 2 O + H 2 O→2KOH
Ca O + H 2 O→Ca(OH) 2

Кислотный оксид + щёлочь→соль + вода (реакция обмена).
SO 3 +2KOH→K 2 SO 4 +H 2 O
CO 2 +Ca(OH) 2 →CaCO 3 +H 2 O
Кислотный оксид + вода→кислота
(реакция соединения)
SO 3 +H 2 O→H 2 SO 4

Основный оксид + кислотный оксид→ соль
(реакция соединения)
K 2 O + CO 2 → K 2 CO 3
SO 2 + CaO → CaCO 3


*повторили определение «оксидов»,
*рассмотрели классификацию оксидов по агрегатному состоянию и способности образовывать соли,
*изучили свойства основных и кислотных оксидов, а также их общие свойства .

*обязательное:
параграф №40, упр.3
*дополнительное:
какие из данных в-в реагируют с оксидом натрия: соляная к-та, азотная к-та, сероводородная к-та, серная к-та. Напишите уравнения .

Как осуществить следующие превращения:
алюминий→оксид алюминия→гидроксид алюминия→хлорид алюминия→алюминий.
Напишите уравнения реакций.




































