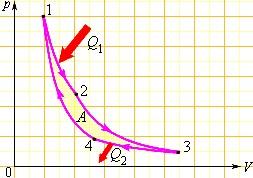
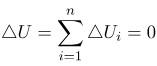| Процессы, нарушающие первый закон термодинамики, никогда не наблюдались. Первый закон термодинамики не устанавливает направления тепловых процессов. Однако многие тепловые процессы могут протекать только в одном направлении. Такие процессы называются необратимыми. Например, тепловой поток всегда направлен от более теплого тела к более холодному. Обратимыми процессами называют процессы перехода системы из одного равновесного состояния в другое, которые можно провести в обратном направлении через ту же последовательность промежуточных равновесных состояний. При этом сама система и окружающие тела возвращаются к исходному состоянию. Процессы, в ходе которых система все время остается в состоянии равновесия, называются квазистатическими. Все квазистатические процессы обратимы. Если рабочее тело тепловой машины приводится в контакт с тепловым резервуаром (его температура в процессе теплообмена постоянна), то единственным обратимым процессом будет изотермический, протекающий при бесконечно малой разнице температур рабочего тела и резервуара. При наличии двух тепловых резервуаров с разными температурами обратимым путем можно провести процессы на двух изотермических участках. Поскольку адиабатный процесс также можно проводить в обоих направлениях (сжатие и расширение), то круговой процесс, состоящий из двух изотерм и двух адиабат (цикл Карно) является единственным обратимым круговым процессом, при котором рабочее тело приводится в тепловой контакт только с двумя тепловыми резервуарами. Процессы превращения механической работы во внутреннюю энергию тела являются необратимыми из-за наличия трения, процессов диффузии, и т. д. Все реальные процессы необратимы, но они могут сколь угодно близко приближаться к обратимым процессам. Направление самопроизвольно протекающих процессов устанавливает второй закон термодинамики. Он может быть сформулирован в виде запрета на определенные виды термодинамических процессов. Английский физик В. Кельвин дал в 1851 году следующую формулировку второго закона: в циклически действующей тепловой машине невозможен процесс, единственным результатом которого было бы преобразование в механическую работу всего количества теплоты, полученного от единственного теплового резервуара. Гипотетическую тепловую машину, в которой мог бы происходить такой процесс, называют вечным двигателем второго рода. В земных условиях такая машина могла бы забирать тепловую энергию, например, у Мирового океана и полностью превращать ее в работу. Масса воды в Мировом океане составляет примерно 1021 кг, и при ее охлаждении на один градус выделилось бы огромное количество энергии (≈ 1024 Дж), эквивалентное полному сжиганию 1017 кг угля. Немецкий физик Р. Клаузиус дал другую формулировку закона: невозможен процесс, единственным результатом которого была бы передача энергии путем теплообмена от тела с низкой температурой к телу с более высокой температурой. Обе формулировки второго закона термодинамики эквивалентны. Если допустить, что тепло может самопроизвольно (без затраты внешней работы) переходить при теплообмене от холодного тела к горячему, то можно говорить о возможности создания вечного двигателя второго рода. Пусть реальная тепловая машина получает от нагревателя количество теплоты Q1 и отдает холодильнику количество теплоты Q2. При этом совершается работа A = Q1 – |Q2|. Если бы количество теплоты |Q2| самопроизвольно переходило от холодильника к нагревателю, то конечным результатом работы реальной тепловой машины и идеальной холодильной машины было бы превращение в работу количества теплоты Q1 – |Q2|, полученного от нагревателя без изменения в холодильнике. Таким образом, комбинация реальной тепловой машины и идеальной холодильной машины равноценна вечному двигателю второго рода. Точно также можно показать, что комбинация реальной холодильной машины и вечного двигателя второго рода равноценна идеальной холодильной машине. Энергия теплового движения молекул качественно отличается от всех других видов энергии – механической, электрической, химической и т. д. Энергия теплового движения молекул может испытать превращение в любой другой вид энергии лишь частично. Поэтому любой физический процесс, в котором происходит превращение какого-либо вида энергии в энергию теплового движения молекул, является необратимым процессом. Общим свойством всех необратимых процессов является то, что они протекают в термодинамически неравновесной системе и в результате этих процессов замкнутая система приближается к состоянию термодинамического равновесия. |