Открытый урок
по химии
в 10 классе
тема урока. Мыло
Выполнила
учитель химии и биологии
первой квалификационной категории
МБОУ СОШ №62 имени Е. И. Игнатенко
села Новый Егорлык
Павлова Н. Н.
2013 год
Тема урока. Мыло.
Цели урока.
Образовательные: изучение состава, строения мыла; прогнозирование моющих свойств мыла; экспериментальная проверка действия мыла на загрязнения. Рассмотреть состав мыла, понять механизм его моющей способности и выявить зависимость свойств мыла от строения и состава.
Развивающие: развитие ассоциативного и логического мышления, понятийного аппарата, экспериментальных умений и навыков, мотивирующего начала в процессе познания. Выявление причинно-следственных связей; формирование практико-ориентированного направления познавательной деятельности.
Воспитательные: воспитание научно-материалистического мировоззрения; культуры пользования химическими препаратами в быту.
Тип урока: урок усвоения новых знаний учащихся.
Форма проведения урока: урок-исследование.
Опережающее домашнее задание
Сообщение 1. «Из истории мыла».
Сообщение 2. « Производство мыла»
Сообщение 3. «Действие мыла на кожу»
Творческое задание . Изготовление мыла в домашних условиях
1. Организационный момент
Сегодня на уроке мы узнаем
О мыле все, чего пока не знаем.
Исследуем его со всех сторон:
Его состав, рН, найдем свой эталон.
Узнаем, почему им все белье стирают.
В какой воде на СМС меняют.
Ответим вместе и не на один вопрос
И почему на мыло в мире спрос?
Мотивация, введение в тему, постановка задачи на урок.
Эпиграф урока
Мыло бывает разное:
Желтое, белое, красное;
Хозяйственное и детское,
Туалетное, русское, шведское;
Жидкое, твердое мыло.
Главное, чтоб оно было.
2.Изучение нового материала
1. «Из истории мыла»
Как давно мыло стало пользоваться спросом ( Сообщение учащейся Овчаренко А. «Из истории мыла»)
2.Химические свойства мыла
Знакомясь со строением и свойствами жиров, мы узнали, что они служат основным продуктом для мыловарения. Какая реакция лежит в основе этого процесса? ( реакция омыления и учащиеся приводят пример реакции омыления) (предлагается посмотреть ролик).
Какой из полученных продуктов реакции представляет интерес для нашего сегодняшнего урока ( соли высших карбоновых кислот).
Действительно ли мыло так хорошо моет?
Опыт №1. Экспериментальная проверка моющего свойства мыла.
Чтобы проверить моющую способность мыла, два школьника согласились на небольшой эксперимент
Ход выполнения демонстрационного ученического эксперимента-исследования:
- испачкаем один палец руки сухой глиной, другой – сухой сажей, третий – растительным маслом, четвертый - сажей, смешанной с растительным маслом.
- сполоснем всю руку холодной водой, смывается глина, сажа – частично, масло – не смывается, сажа в масле – не смывается.
- сполоснем руку горячей водой, результат тот же.
- вымоем руки с мылом, рука - абсолютно частая.
Вывод: мыло обладает моющей способностью.
Объяснение эксперимента
Почему частицы глины смываются водой, а сажи – нет? В чем их разница? Конечно в строении. Частицы глины гидрофильны, т.е. они хорошо смачиваются водой, притягиваются ей и легко смываются с поверхности кожи. Частицы сажи, которая состоит из чистого углерода, гидрофобны, они не смачиваются водой, но они притягиваются к жировым выделениям на поверхности кожи и прочно ими удерживаются. В третьем и в четвертом случаях кожа покрыта масляной пленкой, она отталкивает воду, не дает частицам сбиваться в комки и смыть масло и сажу под ним невозможно простой водой. Приходим к выводу, что водой без мыла смываются только те загрязнения, частицы которых гидрофильны. Но ведь мыло смывает любые частицы. Значит, мыло переводит жировые гидрофобные вещества в раствор и смывает их с кожи, а при стирке – с тканей
А как мыло переводит жировые загрязнения в раствор? Вот мы и подошли к самой сути проблемы мытья и стирки
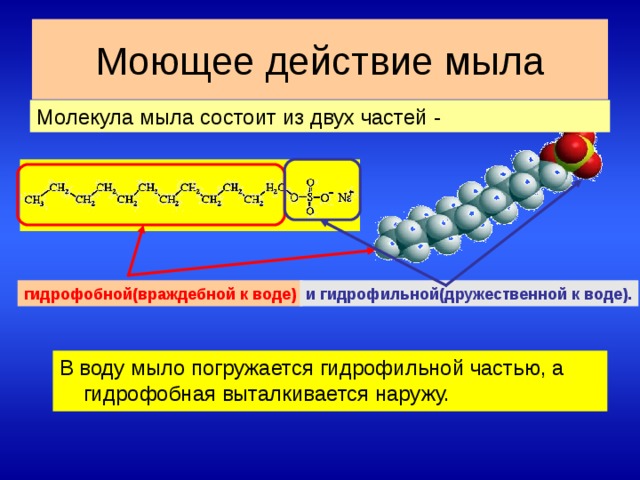
Как у всех солей, у мыла полярные молекулы, но за счет своей сложной органики они очень длинные. Как все соли, в водном растворе молекула мыла дает положительный ион того же натрия или калия, что для нас, в общем-то, неинтересно. Гораздо интереснее ее отрицательный ион: за счет большой длины молекулы один его конец, где “сидит” заряд, является гидрофильным, а другой конец – нейтральным и, соответственно, гидрофобным. Вот так! Что называется, сразу два в одном флаконе: один конец молекулы действует независимо от другого, один чувствует себя “как дома” в воде, другой – в масле. Такое строение, называемое дифильным, позволяет мылу быть в буквальном смысле связующим звеном между несовместимыми субстанциями – водой и жиром.
Гидрофобная часть молекулы мыла проникает в гидрофобное загрязняющее вещество (жир), в результате чего поверхность каждой частицы или капельки загрязнения оказывается как бы окруженной оболочкой из гидрофильных групп. Гидрофильные группы взаимодействуют с полярными молекулами воды. Благодаря этому молекулы моющего средства вместе с загрязнением отрываются от поверхности ткани и уходят в водную среду. Моющая способность мыла усиливается благодаря тому, что при гидролизе мыла образуется щелочь, которая обладает эмульгирующим свойством (учащиеся составляют уравнение реакции). R–СОО–Nа + Н-ОН — R–СООН+ NаОН
Если в воду поместить небольшое количество мыла, оно образует на ее поверхности тонкую пленку толщиной всего в одну молекулу, причем в этой пленке полярные (гидрофильные) концы молекул обращены к воде, а нейтральные (гиброфобные) направлены вверх, в воздух. Такой “нейтралитет” поверхности жидкости существенно сказывается на ее свойствах: снижается так называемый коэффициент поверхностного натяжения. Сила поверхностного натяжения чистой воды заставляет ее собираться в капельки, особенно на жирной, гидрофобной поверхности. Вода же с добавкой мыла растекается по поверхности, смачивает ее. В этом состоит важнейший вклад мыла в процесс стирки.
Получается, что вода с добавкой мыла – более мокрая, чем обычная вода: она хорошо смачивает волокна ткани, проникает в них, что способствует удалению загрязнений.
Опыт №2 Моющие свойства мыла в жесткой воде
К раствору мыла приливаем раствор хлорида кальция. (учащиеся дают объяснение происходящему явлению)
???Две хозяйки готовились к стирке. Первая подогрела воду до 60 С и замочила в ней белье, вторая нагрела воду до кипения, прокипятила ее 5 мин, а затем охладила до 60 С и только после этого начала стирку. У кого белье лучше отстирается?
Опыт №3 Определение среды растворов мыла.
Из приготовленных растворов разных сортов мыла, с помощью универсальной индикаторной бумаги исследуют реакцию раствора мыла.
Определяем реакцию раствора мыла с помощью цветовой эталонной шкалы на упаковке индикаторной бумаги и цифровой шкалы.
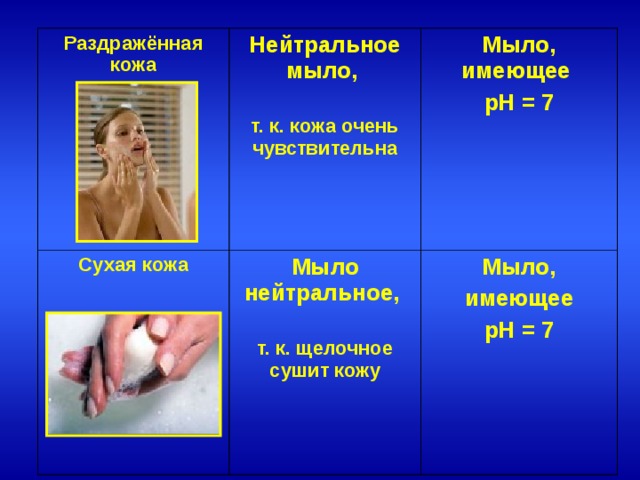
Сравните значение pH приготовленных растворов мыла со значением pH рогового слоя кожи, которое, по данным физиологов, составляет 5,5.
(Сообщение учащегося о типах кожи, и какие из исследованных вами сортов мыла наиболее подходят для ухода за кожей. РадченкоФ.)
3. Получение мыла в промышленности
Сообщение учащегося о промышленном производстве мыла . (Камчантный А)
4. Мыловарение в домашних условиях
Учащиеся представляют свои работы и рассказывают о технологии мыловарения в домашних условиях (Полтинникова И., Зимовец Т)
3. Закрепление материала.
1.Тест “Незаконченные предложения”
- объяснил суть процесса получения мыла …………………
- в состав мыла входят соли …………………
- радикал молекулы мыла …………, а функциональная группа – …………
- задача мыла – переводить в раствор ………………….
- вещество С17Н33СООNa – это – …………………
2.Задача. Сколько кальцинированной соды (в г) потребуется для реакции со стеариновой кислотой массой 28,4 г и сколько (в г) образуется стеарата натрия при 90%-м выходе?
а) 5,3 и 17,2; б) 7,2 и 27,54;
в) 10,6 и 17,2; г) 5,3 и 27,54
4. Подведение итогов урока
5. Рефлексивно-оценочный этап
- на уроке было над ,чем подумать.
- на все возникшие у меня в ходе урока вопросы я получил(а) ответы.
- на уроке я поработал(а) добросовестно и цели урока достиг(ла).
- я узнал(а) много нового.
- мне это пригодится в жизни.
Источники информации:
Интерактивный курс “Открытая химия 2.6.”, 2006.
Мультимедиа учебный курс “1С: Образовательная коллекция. Органическая химия”, 2003.
... Мыловар. www.milo.orion-granit.ru. Статья: Химия мыла и моющих...
О мыле и о том, что происходит, когда оно встречается с водой