Просмотр содержимого документа
«Презентация к уроку по теме: "Водород".»

«Знание только тогда знание, когда оно приобретено усилиями своей мысли».
Л.Н. Толстой

«Покопаемся в памяти».
- Этот элемент- самый распространенный во Вселенной.
2. Этот элемент составляет около 70% массы Солнца и звезд.
3. В гидросфере этот элемент входит в состав воды.
4. Это- самый легкий газ.
5. Этот первый элемент, который использовали для заполнения Дирижаблей.

6. В средние века химики называли это вещество «горючим газом».
7. Это экологически чистое топливо, т.к. при горении образует воду.
8. В 1784 году французский химик А. Лавуазье дал этому элементу название «Гидрогениум», что означает «Рождающий воду».
9. Это самый первый элемент периодической системы.

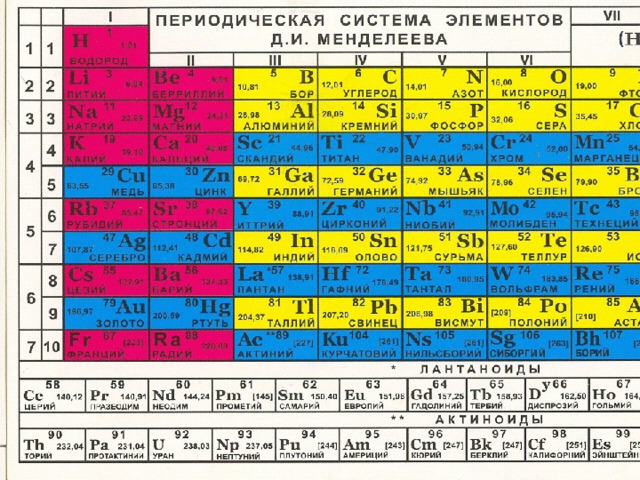

Химический элемент
- Порядковый номер 1
- Группа – I
- Период – 1
- Электронная формула 1s 1
- Степени окисления:
-1, 0, +1

Химические свойства
H 2 + F 2 = 2HF
H 2 + Cl 2 = 2HCl ↑
2. С кислородом (в соотношении 2:1 гремучая смесь)
2H 2 + O 2 = 2H 2 O
3. С серой
H 2 + S = H 2 S ↑
4. С азотом (при давлении и с катализатором)
3 H 2 + N 2 = 2NH 3
5 . С активными металлами
H 2 + 2Na = 2NaH – гидрид натрия
6 . Восстанавливает металлы из их оксидов
MoO 3 + 3H 2 = Mo + 3H 2 O
03.08.23
Микурова О.А. МБУ СОШ № 93 Тольятти
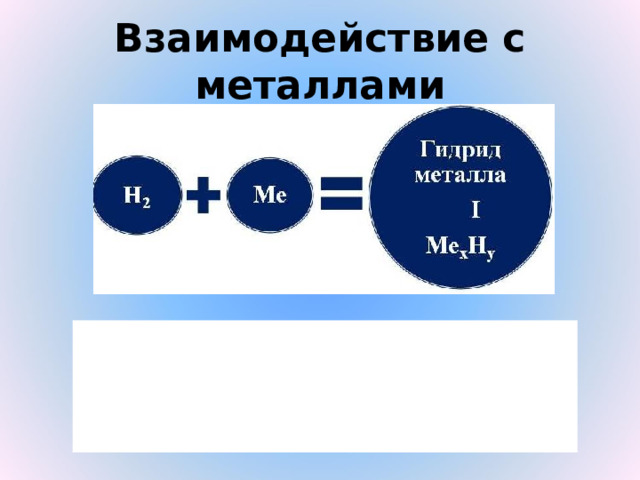
Взаимодействие с металлами
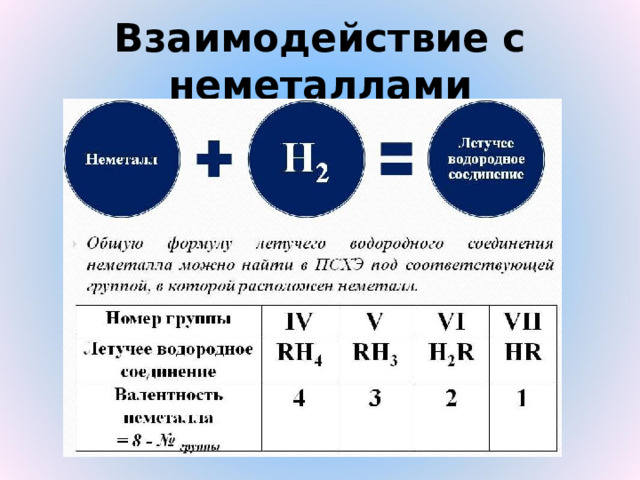
Взаимодействие с неметаллами

Физические свойства
- Водород – газ, без цвета, вкуса и запаха.
- Намного легче воздуха.
- В виду малой молекулярной массы это самый подвижный и самый легкоподвижный из газов.
- Плохо растворим в воде.
- t 0 кипения = -253 0 C
- t 0 плавления = -259 0 C
03.08.23
Микурова О.А. МБУ СОШ № 93 Тольятти


Водород в космосе

Ближайшая к нам звезда Галактики, которую мы знаем под именем «Солнце», на 70 % своей массы состоит из водорода.

Водород на Земле
Вода
Природный
газ
Нефть

История открытия и названия
Водород был обнаружен немецким ученым Т.Парацельсом в XVI веке, когда он погружал железо в серную кислоту.
Название «водород» означает – «рождающий воду».
03.08.23
Микурова О.А. МБУ СОШ № 93 Тольятти

Физические свойства

Получение водорода
- Взаимодействие кальция с водой:
- Гидролиз гидридов:
- Действие разбавленных кислот на металлы:
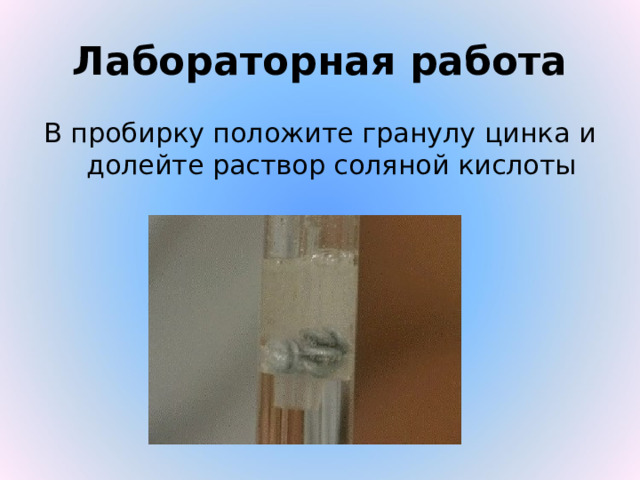
Лабораторная работа
В пробирку положите гранулу цинка и долейте раствор соляной кислоты

Получение в промышленности
В технике водород чаще всего получают
1. Из природного газа:
CH 4 = C + 2H 2 ↑
CH 4 + H 2 O = CO + 3 H 2 ↑ - синтез газ
2. Из воды пропуская через нее постоянный электрический ток
2 H 2 O = 2 H 2 ↑ + O 2 ↑
03.08.23
Микурова О.А. МБУ СОШ № 93 Тольятти

Применение
- Синтез хлороводорода.
- Восстановление металлов.
- Топливо в двигателях.
- Синтез аммиака. (минеральные удобрения)
- Получение маргарина.
- Водородная сварка и резка металлов.
- Синтез метанола.
- Наполнение воздушных шаров, дирижаблей.
9. Дейтерид лития – основной компонент заряда водородной бомбы.
03.08.23
Микурова О.А. МБУ СОШ № 93 Тольятти

В продажу водород поступает в баллонах под давлением свыше 150 атм. Они окрашены в тёмно-зелёный цвет и снабжаются красной надписью "Водород".

Домашнее задание.
- Параграф -19
- Творческое задание: Сочинение «В некотором царстве Химоза правил Гидрогениум ибн Водород…» (по желанию).
- Задача: Вычислите объем водорода, который выделится при взаимодействии цинка с 60 г раствора соляной кислоты, в которой массовая доля кислоты составляет 20%.







































