
Химия алканов
Подготовила :
Трубникова Елена Евгеньевна
учитель химии и биологии
МБОУ «Клюквинская средняя
общеобразовательная школа»
Курского района Курской области

Общая формула
Строение молекулы
Гомологический ряд
Номенклатура
Изомерия
Способы получения
Физические свойства
Химические свойства
Применение

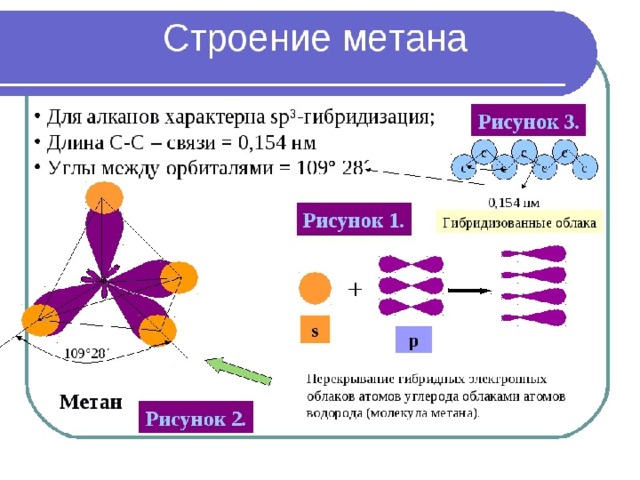
Алканы – это предельные алифатический углеводороды, в их молекулах все атомы углерода соединены между собой одинарными σ- связями.
Общая формула:
С n H 2n+2
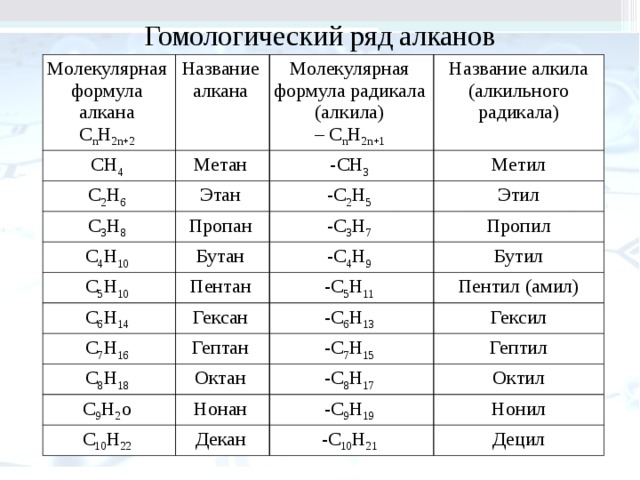
Гомологический ряд алканов
Молекулярная
формула алкана
Название алкана
СН 4
Метан
C 2 H 6
Молекулярная формула радикала (алкила)
С n Н 2n+2
Название алкила
С 3 Н 8
Этан
-CH 3
– C n H 2n+1
-С 2 Н 5
(алкильного
Метил
С 4 Н 10
Пропан
C 5 H 10
Бутан
Этил
радикала)
-C 3 H 7
Пропил
-С 4 Н 9
Пентан
С 6 Н 14
Бутил
-С 5 Н 11
C 7 H 16
Гексан
Пентил (амил)
С 8 H 18
Гептан
-С 6 Н 13
Гексил
-С 7 Н 15
Октан
С 9 Н 2 о
Гептил
-C 8 H 17
Нонан
С 10 Н 22
Октил
-С 9 Н 19
Декан
Нонил
-С 10 Н 21
Децил

Номенклатура алканов ИЮПАК
Выбор главной цепи .
Формирование названия углеводорода начинается с определения главной цепи — самой длинной цепочки атомов углерода в молекуле, которая является как бы ее основой.
Нумерация атомов главной цепи .
Атомам главной цепи присваивают номера. Нумерация атомов главной цепи начинается с того конца, к которому ближе стоит заместитель (структуры А, Б). Если заместители находятся на равном удалении от конца цепи, то нумерация начинается от того конца, при котором их больше (структура В). Если различные заместители находятся на равном удалении от концов цепи, то нумерация начинается с того конца, к которому ближе старший (структура Г). Старшинство углеводородных заместителей определяется по тому, в каком порядке следует в алфавите буква, с которой начинается их название: метил (—СН 3 ), затем пропил (-СН 2 -СН 2 -СН 3 ), этил (—СН 2 —СН 3 ) и т. д.
Обратите внимание на то, что название заместителя формируется заменой суффикса -ан на суффикс -ил в названии соответствующего алкана.

Формирование названия .
В начале названия указывают цифры — номера атомов углерода, при которых находятся заместители.
Если при данном атоме находятся несколько заместителей, то соответствующий номер в названии повторяется дважды через запятую (2,2-).
После номера через дефис указывают количество заместителей (ди — два, три — три, тетра — четыре, пента — пять) и название заместителя (метил, этил, пропил).
Затем без пробелов и дефисов — название главной цепи.
Главная цепь называется как углеводород — член гомологического ряда метана (метан, этан, пропан и т. д.).
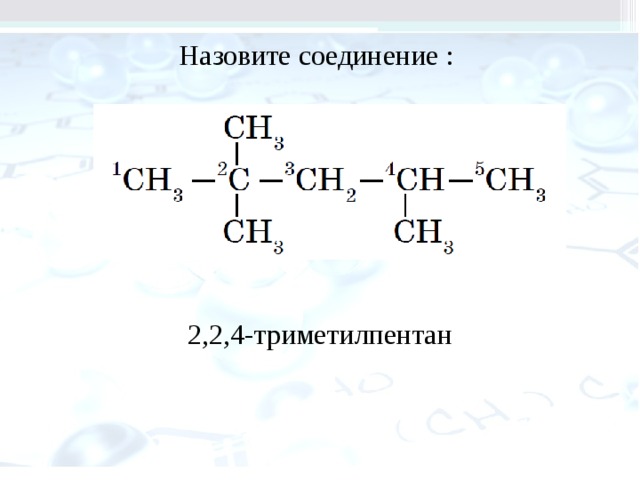
Назовите соединение :
2,2,4-триметилпентан

Изомерия алканов
Для алканов характерна так называемая
структурная изомерия . Структурные изомеры отличаются друг от друга строением углеродного скелета. Простейший алкан, для которого характерны структурные изомеры, — это бутан.

Способы получения алканов (метана)
1. В промышленности:
- из природного газа;
- синтез из оксида углерода (II) и водорода (оксосинтез):
nCO + (2n+1) H 2 → C n H 2n+2 + nH 2 O

2. В лаборатории:
- гидролиз карбида алюминия:
А1 4 С 3 + 12Н 2 О → 3СН 4 ↑ + 4А1(ОН) 3 ;
- сплавление солей уксусной кислоты со щелочами (реакция Дюма) t
СН 3 СООNa + NaОН → СН 4 + Nа 2 СО 3


Получение гомологов метана.
1. В промышленности:
- из природного сырья (нефть, газ, горный воск);
- синтез из оксида углерода (II) и водорода
2. В лаборатории:
- каталитическое гидрирование (+Н 2 ) непредельных УВ
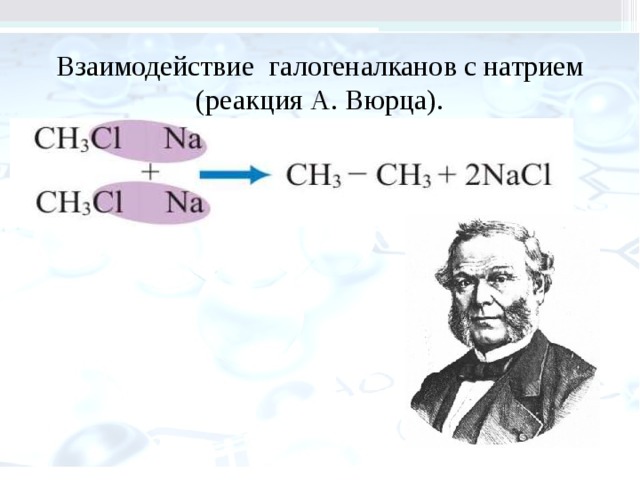
Взаимодействие галогеналканов с натрием (реакция А. Вюрца).

Электролиз растворов
солей карбоновых кислот
(синтез Кольбе)

Синтез Гриньяра

Физические свойства
Первые четыре представителя гомологического ряда метана — газы. Простейший из них — метан — газ без цвета, вкуса и запаха (запах «газа», почувствовав который, надо звонить 04, определяется запахом меркаптанов — серосодержащих соединений, специально добавляемых к метану, используемому в бытовых и промышленных газовых приборах для того, чтобы люди, находящиеся рядом с ними, могли по запаху определить утечку).
Углеводороды состава от С 5 Н 12 до С 15 Н 32 — жидкости; более тяжелые углеводороды — твердые вещества. Температуры кипения и плавления алканов постепенно увеличиваются с возрастанием длины углеродной цепи. Все углеводороды плохо растворяются в воде, жидкие углеводороды являются распространенными органическими растворителями.

Химические свойства алканов

Химические свойства алканов

Химические свойства алканов

Применение алканов
(на примере метана)
Использованные источники
http://ruscopybook.com/chemistry/10_class /
http://school-books.download/novoshinskij-novoshinskaya-organicheskaya-ximiya-posobie-dlya-starsheklassnikov-i-abiturientov/
https ://yandex.ru/images/search?text= строение%20молекулы%20предельных%20углеводородов& noreask =1&img_url=https%3A%2F%2Fds02.infourok.ru%2Fuploads%2Fex%2F064a%2F00012b41-31612ebe%2Fimg8.jpg&pos=12&rpt= simage&lr =8
http://www.chem-mind.com/2017/03/27/тема-№15-алканы/
https://yandex.ru/images/search?text= Шарль%20Адольф%20Вюрц& noreask =1&img_url=http%3A%2F%2Fegorov-sn.ru%2F_bl%2F0%2F20292717.jpg&pos=13&rpt= simage
https://yandex.ru/images/search?text=гриньяр&noreask=1&img_url=https%3A%2F%2Fupload.wikimedia.org%2Fwikipedia%2Fcommons%2F3%2F31%2FVictor_Grignard.jpg&pos=1&rpt=simage&lr=8






































