Презентация к уроку химии 9 класса по теме Металлы. железо. В презентации представлены сведения о строении атома, возможных валентностях, свойствах простого вещества, биологического и промышленного значения.
Просмотр содержимого документа
«Презентация к уроку Металлы. Железо.»

Тема урока: «Железо»

Положение железа в периодической системе: электронная формула
4,VIII, побочная
4s 2
2
3s 2 3p 6
3d 6
14
2s 2 2p 6
8
1s 2
2

Нахождение железа в природе
2-ой по распространенности металл после Al (5,1%)
FeS 2
Пирит
Fe 3 O 4
Магнетит
Fe 2 O 3
Гематит

Химические свойства железа:
1.Взаимодействие с простыми веществами(при t ° ):
а) с галогенами: 2Fe + 3Cl 2 →2FeCl 3
б) с кислородом: 3Fe + 3O 2 →Fe 3 O 4
окалина
в) с серой: Fe + S → FeS

Химические свойства железа:
2. Взаимодействие со сложными веществами:
а) с кислотами (HCl ,разб.H 2 SO 4 )
Fe +2 HCl → FeCl 2 + H 2
б) с солями
Fe + CuSO 4 → Cu + FeSO 4

Химические свойства железа:
При восстановлении железом еще менее активных металлов, например, серебра из соли серебра, железо переходит в соединение, в котором оно проявляет степень окисления +3.
0
+1
0
+3
3AgNO 3 + Fe = Fe(NO 3 ) 3 + 3Ag
в) с водой (при t 0 )
3Fe +4H 2 O→ Fe 3 O 4 +4 H 2
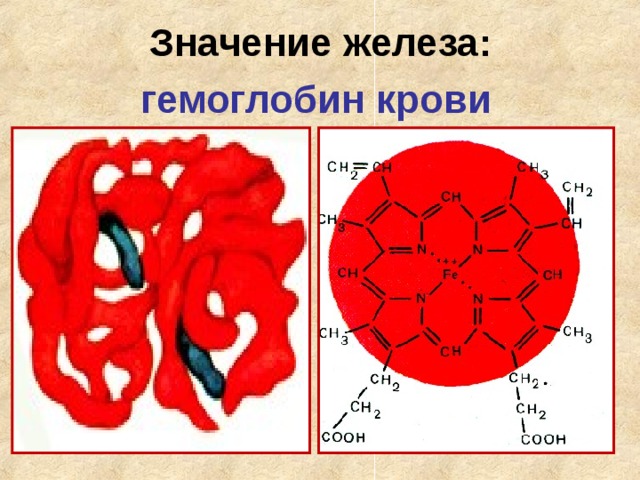
Значение железа:
гемоглобин крови

Значение железа:
шпинат
капуста
яблоки
мясо

Значение железа:
сердечники для трансформаторов
мембрана для микрофонов


























