

СДЕЛАЙТЕ СВОИ УРОКИ ЕЩЁ ЭФФЕКТИВНЕЕ, А ЖИЗНЬ СВОБОДНЕЕ
Благодаря готовым учебным материалам для работы в классе и дистанционно
Скидки до 50 % на комплекты
только до
Готовые ключевые этапы урока всегда будут у вас под рукой
Организационный момент
Проверка знаний
Объяснение материала
Закрепление изученного
Итоги урока







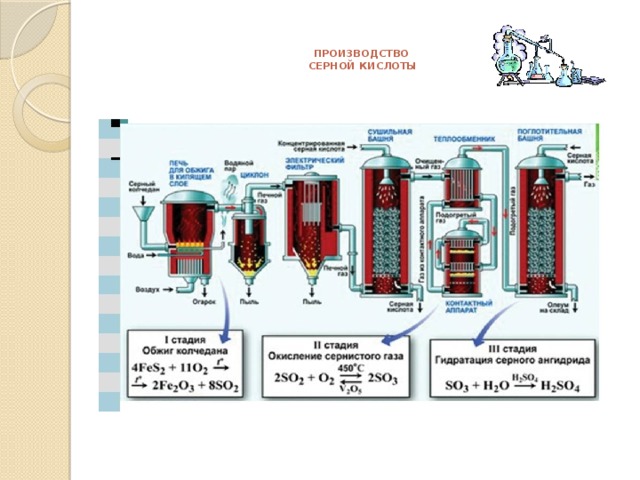



 SO 2 — SO 3 — H 2 SO 4 — SO 2 — Na 2 SO 3 — SO 2 Определить количество 10%-ного и 30%-ного растворов, необходимых для приготовления 300г 15%-ного раствора серной кислоты. " width="640"
SO 2 — SO 3 — H 2 SO 4 — SO 2 — Na 2 SO 3 — SO 2 Определить количество 10%-ного и 30%-ного растворов, необходимых для приготовления 300г 15%-ного раствора серной кислоты. " width="640"











