Просмотр содержимого документа
«Производство серной кислоты»

Производство
серной кислоты
Производство
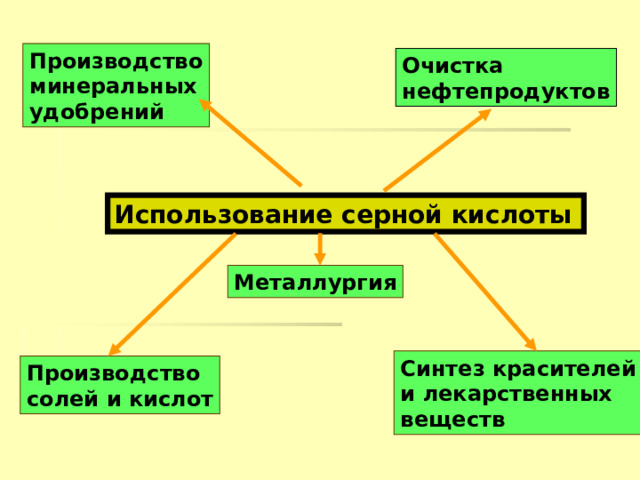
минеральных
удобрений
Очистка
нефтепродуктов
Использование серной кислоты
Металлургия
Синтез красителей
и лекарственных
веществ
Производство
солей и кислот

Применение серной кислоты
хлопок, лен
- в производстве минеральных удобрений
овощи и зерновые культуры
- для качественного, стойкого окрашивания
шерстяных и хлопчатобумажных тканей
применяют соли серной кислоты
- сами красители изготавливают с применением
серной кислоты



Применение серной кислоты
- для обработки кожи, применяемой на обувных
фабриках
- в производстве мыла
- для отбеливания бумаги
для изготовления чернил
- в производстве смазочных масел и керосина



Применение серной кислоты
- в фармацевтической промышленности
- для производства искусственного волокна
- в производстве взрывчатых веществ

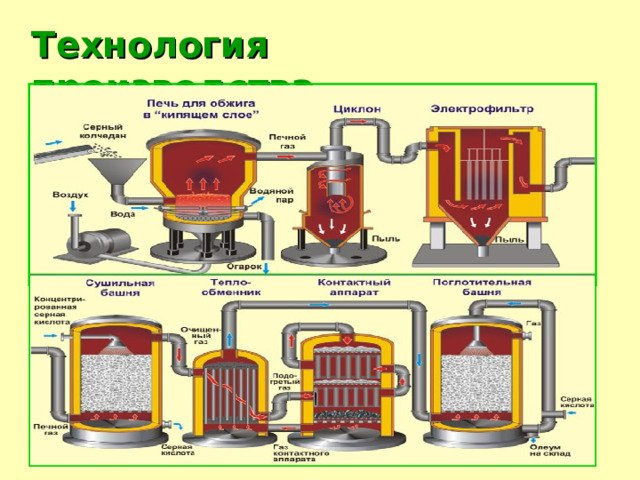
Технология производства

Сырьё
- FeS 2 - пирит, серный колчедан, железный колчедан
- S 8 самородная ромбическая сера
- H 2 S – сероводород
- С u 2 S ; ZnS ; PbS – сульфиды цветных металлов
- CaSO 4 *2H 2 O – гипс
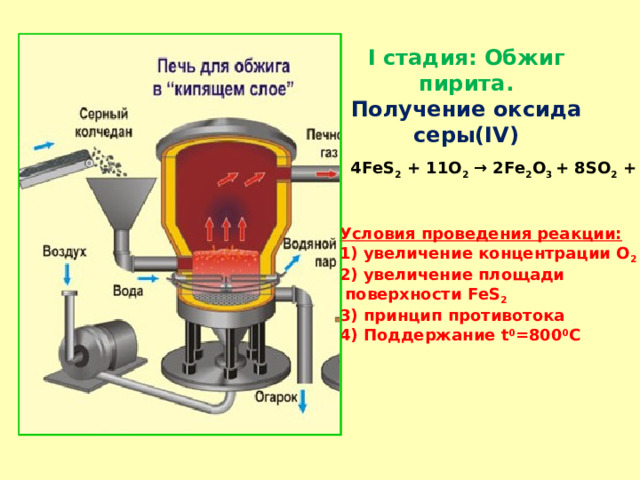
I стадия: Обжиг пирита.
Получение оксида серы( IV )
4 FeS 2 + 11O 2 → 2Fe 2 O 3 + 8SO 2 + Q
Условия проведения реакции:
- увеличение концентрации О 2
- увеличение площади
поверхности FeS 2
3) принцип противотока
4) Поддержание t 0 =800 0 C
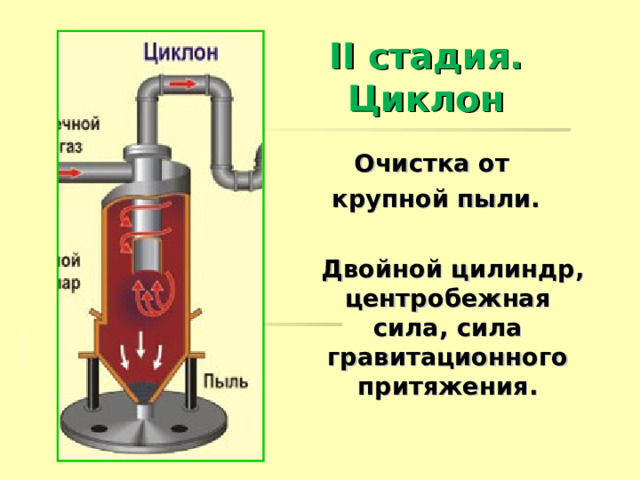
II стадия. Циклон
Очистка от
крупной пыли.
Двойной цилиндр, центробежная сила, сила гравитационного притяжения.
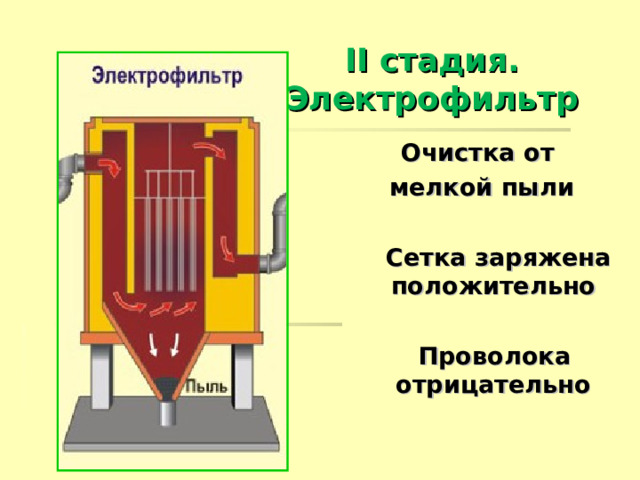
II стадия. Электрофильтр
Очистка от
мелкой пыли
Сетка заряжена положительно
Проволока отрицательно
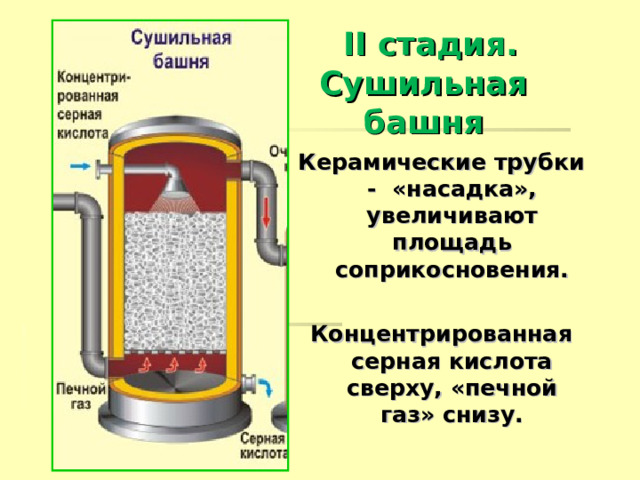
II стадия. Сушильная башня
Керамические трубки - «насадка», увеличивают площадь соприкосновения.
Концентрированная серная кислота сверху, «печной газ» снизу.
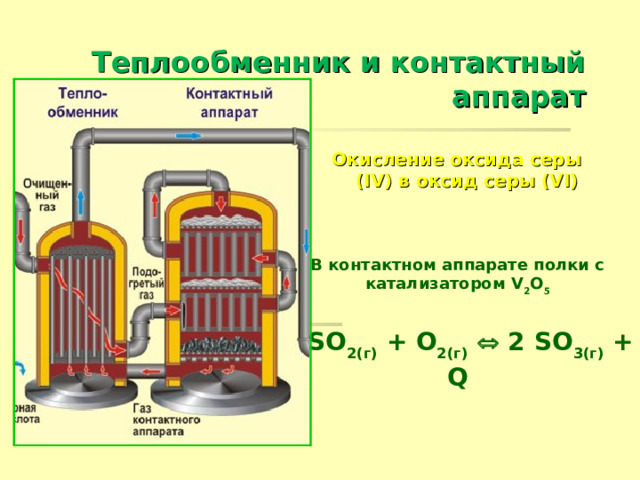
Теплообменник и контактный аппарат
Окисление оксида серы (IV) в оксид серы (VI)
В контактном аппарате полки с катализатором V 2 O 5
2 SO 2(г) + O 2(г) 2 SO 3(г) + Q
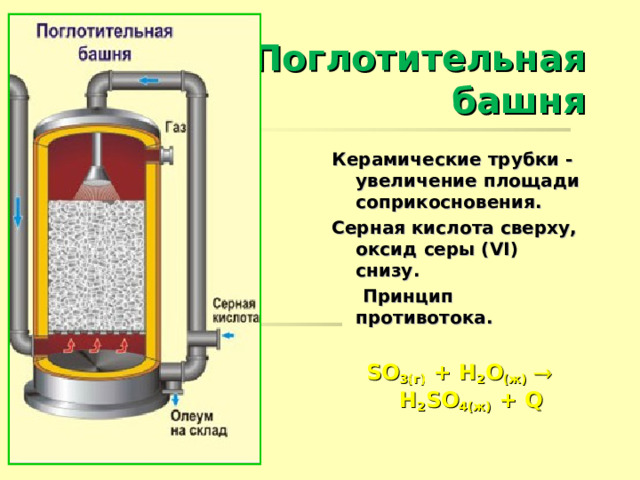
Поглотительная башня
Керамические трубки - увеличение площади соприкосновения.
Серная кислота сверху, оксид серы ( VI) снизу.
Принцип противотока.
SO 3(г) + Н 2 О (ж) Н 2 SO 4(ж) + Q
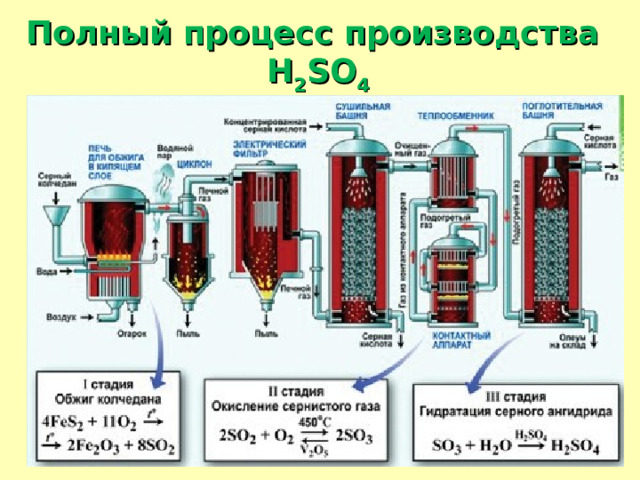
Полный процесс производства H 2 SO 4

Принципы производства
- Механизация процесса;
- Автоматизация процесса;
- Оптимальные условия реакций ( 800 0 C , давление, «кипящий слой», катализатор);
- Использование теплоты;
- Противоток;
- Обогащение кислородом воздуха;
- Герметизация аппаратуры.

Профессии работников сернокислотного производства:
- Инженер – технолог.
- Аппаратчик.
- Лаборант – аналитик .

Транспортировка и хранение серной кислоты
- Транспортируют в железнодорожных и автоцистернах из кислотостойкой стали
- Хранят в герметически закрытых емкостях из полимера или нержавеющей стали, покрытой кислотоупорной плёнкой
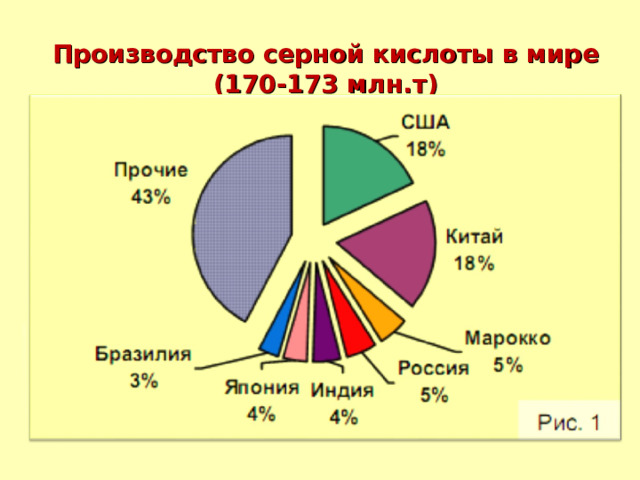
Производство серной кислоты в мире (170-173 млн.т)
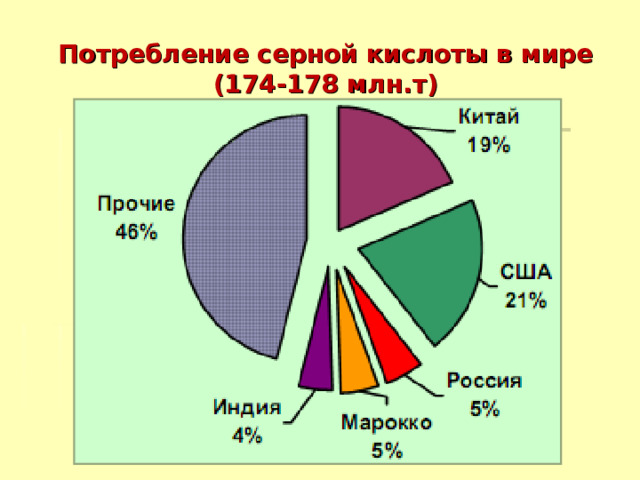
Потребление серной кислоты в мире (174-178 млн.т)

Потребление серной кислоты
- 1. Производство минеральных удобрений.
- 2. Производство сульфатов (солей серной кислоты).
- 3. Производство синтетических волокон.
- 4. Черная и цветная металлургия.
- 5. Производство органических красителей.
- 6. Спирты, кислоты, эфиры(орг. вещества).
- 7. Пищевая промышленность(патока, глюкоза), эмульгатор (загуститель) Е513.
- 8. Нефтехимия(минеральные масла).
- 9. Производство взрывчатых веществ.

Экологический ущерб производства
При аварийных выбросах в атмосферу попадают соединения серы:
SO 2 ;SO 3 ; H 2 S; H 2 SO 4 ; Fe 2 O 3 (пыль)
Последствия: «закисление» почв и водоёмов, «металлизация» атмосферы
РЕШЕНИЕ ЭКОЛОГИЧЕСКИХ ПРОБЛЕМ:
- Непрерывность технологического процесса;
- Комплексное использование сырья;
- Совершенствование технологического оборудования.











































