Кристаллические решетки
Цель: познакомить учащихся с типами кристаллических решеток, раскрыть взаимосвязь свойств веществ с типом кристаллических решеток, воспитать интерес к изучению химической науки.
Оборудование: презентация, карточки с заданием, фильмы (анимации)
Ход урока
Организация класса
Основная часть
Изучение нового материала
Слайд 1 – 3 Сообщение темы, целей и плана урока
Просмотр фильма Агрегатное состояние воды
Слайд 4 Учащиеся агрегатное состояние веществ
Слайд 5 Твердые вещества делятся в свою очередь на кристаллические и аморфные
Учащиеся Валя особенности аморфных веществ и примеры
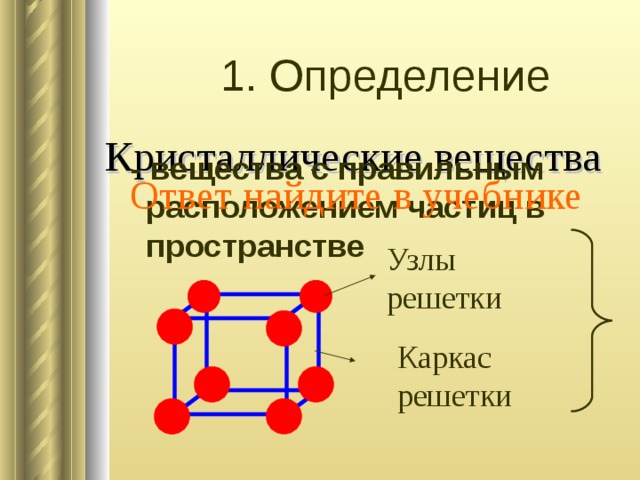
Учитель найдите определение кристаллические вещества в учебнике
кристаллические вещества характеризуются правильным расположением составляющих их частиц. Точки, в которых располагаются частицы называются узлы решетки. Линии, которыми можно соединить эти точки образуют пространственный каркас, который называют Кристаллическая решетка.
Запись в тетради, вывесить на доску определение.
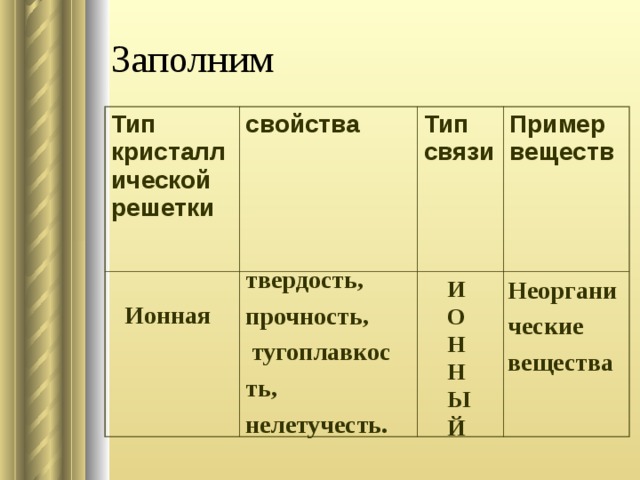
Слайд 7 Оформим работу в виде таблицы, вывесить на доску таблицу.
Учащиеся: запись в тетради
Учитель слайд 8: вспомните виды химической связи, механизм образования, пример
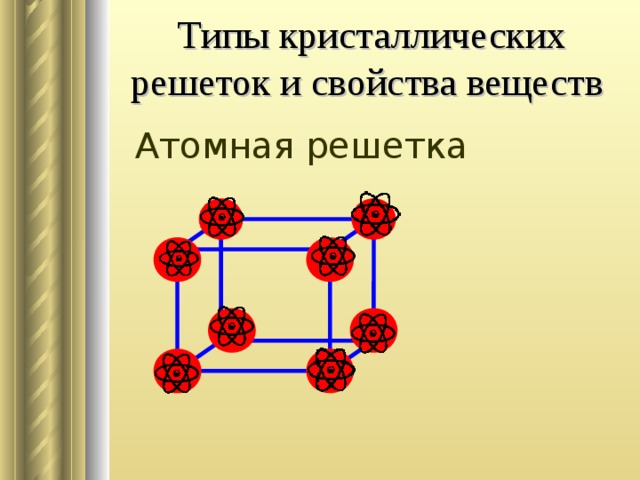
Просмотр фильма: атомная решетка
Учитель слайд 9: в узлах атомных решеток находятся атомы, которые соединены прочными ковалентными связями. При этом вещества имеют высокие температуры плавления, они твердые и прочные, практически нерастворимы. Примерами таких веществ являются алмаз, кристаллический бор, кремний, песок.
Слайд 10: запись опорного конспекта.
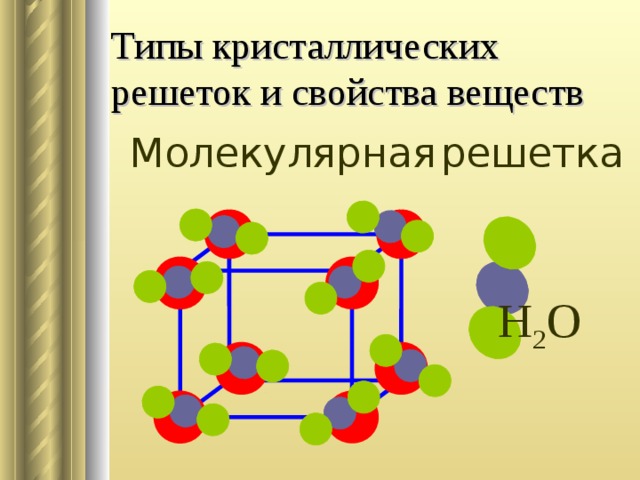
Просмотр фильма молекулярная решетка
Учитель слайд 11: в узлах решетки располагаются молекулы, связь в молекулах может быть полярной и неполярной эти связи довольно прочны, однако между собой молекулы связаны не прочными межмолекулярными силами. Поэтому вещества с молекулярной кристаллической решеткой будут летучие, иметь малую твердость, малые температуры плавления. Примерами являются: благородные газы, вода, органические соединения.
показ опыта сахар можно растопить – низкая температура плавления.
Слайд 12: оформление опорного конспекта
Слайд 13: самостоятельная работа с учебником ионная и металлическая связь.
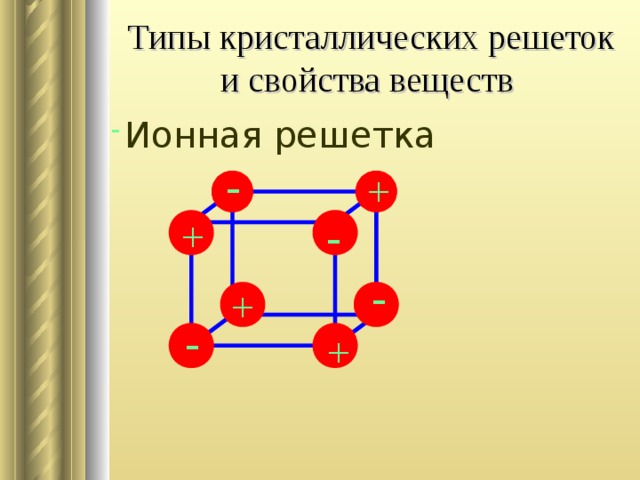
Слайд 14: ионная связь
показ опыта тугоплавкость: расплавить соль
Слайд 15: запись учащимися под диктовку
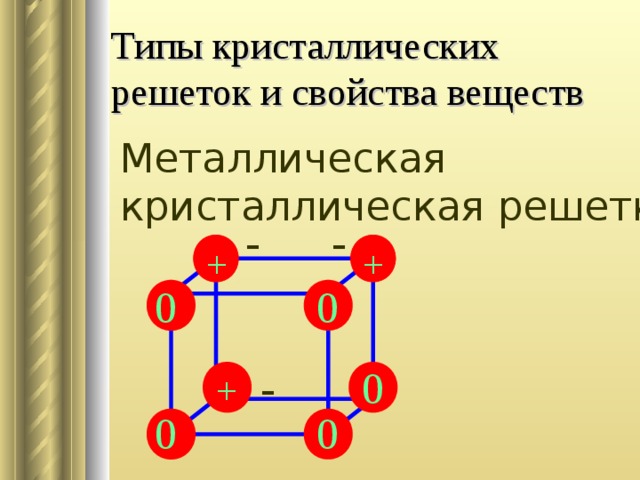
Слайд 16: металлическая связь
Слайд 17: запись в тетради
Закрепление
Слайд 18 устный опрос 1 вопрос, 2 вопрос, 3 вопрос.
Слайд 19 определите соответствие
Ионная CaCl2 Прочность, твердость, электропроводность
Молекулярная I2 Низкая температура плавления, хрупкость
Атомная SiO2 Очень высокие температуры плавления, твердость
Металлическая Fe Ковкость, пластичность, тепло- и электропроводность
Работа с карточками
Укажите тип кристаллической решетки
Аммиак Фторид лития молекулярная ионная
Алмаз Хлорид калия атомная ионная
Диоксид кремния Фторид кальция атомная ионная
Фтороводород Фторид натрия молекулярная ионная
В перечисленных соединениях определите тип химической связи, тип кристаллической решетки и сделайте прогноз об их физических свойствах
N2 Cr Ni SO3 Mg MgO NaI I2
| Найдите аморфные вещества и составьте название вещества стекло Шоколад………………………………………………………с Вода…………………………………………………………….о Жевательная резинка………………………………..т Пластмасса………………………………………….……..е Алюминий…………………………………………………д Смола……………………………………………….……….к Мел……………………………………………….…………..а Пластилин……………………………………………...…л Воск…………………………………………………………..о
Укажите тип кристаллической решетки А). CaCl2 ____________________________________________________ Б). CO2________________________________________________________ B). Al____________________________________ Г). H2O___________________________________
|
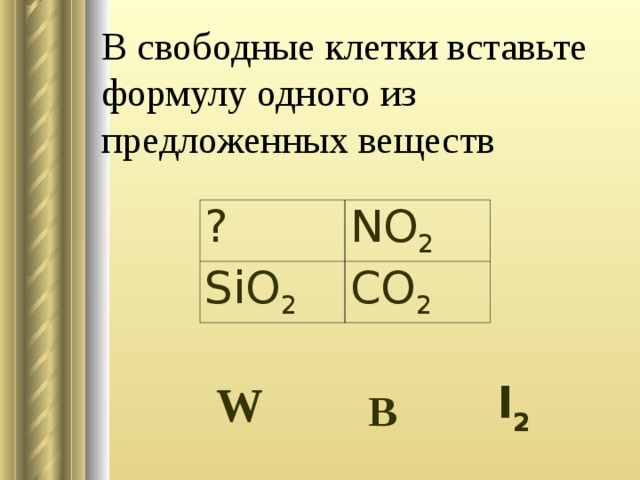
Слайд 20-21 определите нужную формулу
SiF4 F2 NaF
W B I2
Pb N2 Cl2
Итоги урока
Слайд 23 определения, типы
Рефлексия
Что узнал, что не понял
Домашнее задание 22, упр 6